LC-MS-MS法测定人血浆中阿托伐他汀浓度
2011-11-22杨永革许雪廷赵钢涛
姜 楠,杨永革,许雪廷,赵钢涛
(北京军区总医院药理科,北京100700)
·论著·
LC-MS-MS法测定人血浆中阿托伐他汀浓度
姜 楠,杨永革,许雪廷,赵钢涛
(北京军区总医院药理科,北京100700)
目的建立液质联用色谱法(LC-MS-MS)测定人血浆中阿托伐他汀(atorvastatin )浓度。方法采用萃取法处理血浆样品进行LC-MS-MS分析。分析柱为美国Thermo公司Thermo BioBasic-C8柱(2.1 mm×100 mm,5 μm) ;流动相为乙腈(含0.1%甲酸):水(含0.1%甲酸)=70:30;流速0.3 ml/min;质谱条件:电喷雾离子化电离源ESI负离子检测,喷雾电压(SP)3 500 KV,鞘气(SGP)流速10 Arb,辅助气(AGP)流速15 Arb,毛细管温度(TEM)314 ℃;选择反应监测(SRM)分别测定阿托伐他汀和甲苯磺丁脲 558→278 m/z(30 EV)和269→106 m/z(22 EV) 。结果阿托伐他汀在0.1~20 μg/L检测浓度范围内呈良好线性关系(r>0.99),最低定量限(LLOQ)为0.1 μg/L,绝对回收率在70%以上,高中低3种浓度的日内和日间RSD≤15%。结论该方法操作简便、灵敏、准确,适用于临床阿托伐他汀的血药浓度监测及I期临床试验。
阿托伐他汀钙;血药浓度;液质联用色谱法
阿托伐他汀钙为3-羟基-3-甲基-戊二酰辅酶A(HMG-CoA)还原酶抑制剂[1],主要通过抑制HMG-CoA还原酶的合成,从而抑制体内胆固醇的合成,由于细胞内总胆固醇含量的减少,刺激细胞合成低密度脂蛋白(LDL)受体加速,使肝脏表面LDL受体数目增多及活性增强,从而促进LDL、极低密度脂蛋白(VLDL)和VLDL残粒通过受体降解途径代谢,降低血清LDL含量。此外,由于本品抑制了细胞合成胆固醇,干扰了脂蛋白的生成,使血清总胆固醇水平下降,血清甘油三酯水平也有一定程度的降低[2]。其适应证为:①原发性高胆固醇血症和混合型高脂血症。②高胆固醇血症并有动脉粥样硬化危险的病人。化学结构见图。
1 仪器与材料
1.1仪器 质谱仪:Thermo Finnigan TSQ Quantum型液相色谱——三重四极杆质谱联用仪,配有电喷雾离子化源(ESI源);Agilent 1100高效液相色谱系统:G1313A自动进样器;G1312A二元梯度泵;在线脱气机、柱温箱(美国Agilent公司);Finnigan Xcalibur 色谱/质谱数据系统。Sigma1-14型高速离心机(美国Sigma公司);XW-80A微型涡旋混合仪(上海沪西分析仪器有限公司);Sartorius BS110S型电子分析天平(北京赛多利斯仪器系统有限公司)。
1.2材料 阿托伐他汀钙对照品(纯度95.3%,批号100590-200501,中国药品生物制品检定所);甲苯磺丁脲对照品 (纯度100.0%,批号100500-200801,中国药品生物制品检定所)。乙腈、乙酸乙酯(Fisher公司)为进口色谱纯级;甲酸、碳酸钠等试剂均为分析纯级;分析用水为娃哈哈集团生产的蒸馏水。
2 方法与结果
2.1实验条件
2.1.1色谱条件 色谱柱为美国Thermo公司Thermo BioBasic-C8柱(2.1 mm×100 mm,5 μm) ;流动相为乙腈(含0.1%甲酸):水(含0.1%甲酸)=70:30;流速0.3 ml/min;进样量10 μl;柱温为室温。
2.1.2质谱条件 采用气动辅助电喷雾离子化电离源(ESI),负离子方式检测;喷雾电压(SP)3 500 V;加热毛细管温度(TEM)314 ℃;鞘气(SGP)流速10 Arb;辅助气(AGP)流速15 Arb;碰撞气(CID)压力1.5 mTorr;源内碰撞诱导解离(Source CID)能量为10 V;质谱扫描方式为选择反应监测(SRM),分别测定阿托伐他汀和甲苯磺丁脲反应离子m/z 558→278(30 EV)和m/z 269→106(22 EV);扫描时间为0.2 s。
2.2血浆样本的预处理 精密量取血浆样品0.5 ml,置于10 ml具塞玻璃离心管中,加100 μl内标(甲苯磺丁脲乙腈溶液,1 mg/L),混匀,再加100 μl 0.1 M的碳酸钠水溶液混匀,超声2 min,加3 ml乙酸乙酯,在微型混合器上涡流振荡2 min,离心(2 000 r/min)5 min分层,取上清液转移至另一10 ml玻璃离心管中,37 ℃水浴下氮气吹干,120 μl流动相复溶,在微型混合器上涡流振荡1 min,离心(10 000 r/min)10 min,取上清液10 μl进样检测。
2.3标准溶液的配制 ①阿托伐他汀工作溶液:精确称取阿托伐他汀钙对照品10.87 mg(相当于阿托伐他汀10 mg),用乙腈配制成浓度为1 g/L的工作溶液,-70 ℃保存待用,1个月后重新配制。②甲苯磺丁脲工作溶液(内标):精确称取一定量甲苯磺丁脲,用乙腈配制成浓度为1 mg/L的内标溶液,4 ℃保存待用,一个月后重新配制。
用阿托伐他汀钙对照品配成一系列浓度的工作溶液,分别取各浓度工作溶液10 μl于0.5 ml空白血浆中,使阿托伐他汀的血浆终浓度分别为0.1,0.25,0.5,1,2.5,5,10,20 μg/L,余同血浆样品的处理与测定。
2.4线性范围与定量限 将不同浓度系列标准样品测得的阿托伐他汀与内标峰面积比值为纵坐标,阿托伐他汀浓度为横坐标,直线加权回归。结果表明血浆中阿托伐他汀浓度在0.1~20 μg/L范围内浓度与峰面积有良好的线性关系Y=0.072 827 5+0.121 806X(r2=0.992 7)。试验期间制备的标准曲线r2值均在0.99以上。方法的最低检测浓度为0.1 μg/L,其RSD值为10.9%。
2.5特异性考察 按选定的LC/MS/MS条件测得6名健康人的空白血浆;空白血浆+ 阿托伐他汀钙标准样品+内标;受试者口服阿托伐他汀钙片后的血浆样品质量色谱图,见图1。阿托伐他汀与甲苯磺丁脲分别在1.40和1.32 min出峰,由图可见血浆中内源性物质不干扰测定。
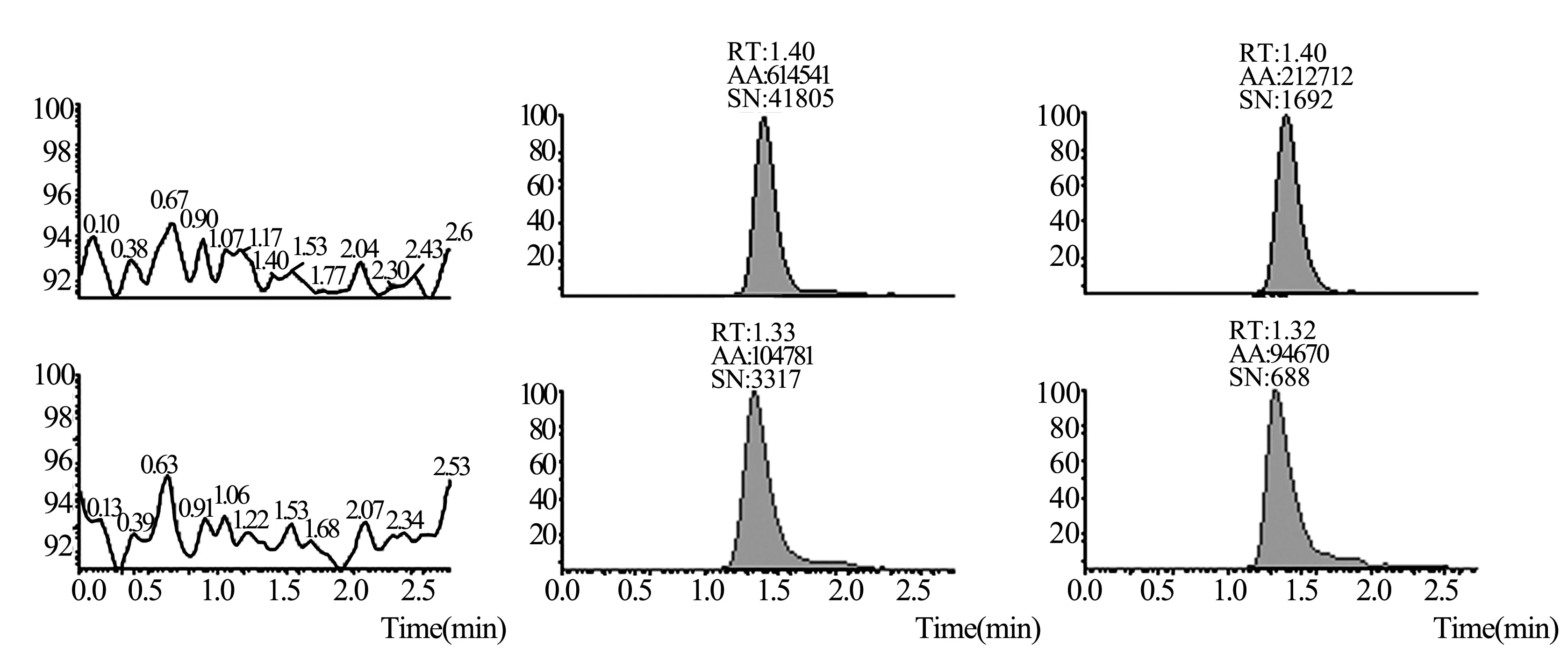
图1 血浆中阿托伐他汀SRM色谱图
2.6精密度与回收率 按阿托伐他汀钙标准曲线制备方法制备质控样品,对0.25,2.5和10 μg/L 3种浓度进行了连续3 d的6份样本分析,以评价方法的日内、日间精密度。同时以流动相代替空白血浆,同样方法配制高、中、低3种浓度(0.25、2.5、10 μg/L)的标准品样本,计算回收率。低、中、高3个浓度的准确度分别为0.248±0.053、2.483±0.202、9.975±0.741μg/L;日内精密度分别为11.10、8.08、2.90%;日间精密度分别为7.30、8.50、7.76%;提取回收率分别为(79.16±7.90)%、(78.07±4.78)%、(72.28±4.53)%。
2.7稳定性试验 将阿托伐他汀标准溶液配制的 (0.25、2.5、10 μg/L) 的血浆样品,按以下操作进行稳定性考察:血浆样品室温放置2 h的稳定性;血浆样品处理后放置8 h的稳定性;室温与-70 ℃交替冻融3次的稳定性;-70 ℃保存30 d的稳定性。每个浓度点测定6份样品与放置0 h的样本进行比较,计算后各浓度变异均小于15%,稳定性符合指导原则。
3 讨论
试验初期,我们考察了酸化或碱化加液-液萃取的方法,提取出的目标化合物浓度较低,最低检测限仅为0.5 μg/L。后发现加入超声方法可以提高提取效率,并且碱性条件下的超声效果优于在酸性条件下超声,最低检测限可以达到0.1 μg/L。这也许是碱性条件下超声不利于阿托伐他汀与血浆蛋白结合,使得游离药物浓度增多所致。本方法还考察了甲基叔丁基醚[3]、乙酸乙酯[4]、正己烷、乙醚等有机溶剂对萃取结果的影响,结果证明醚类试剂提取的空白血浆中的杂质干扰更大一些,因此选择低毒、低成本的乙酸乙酯作为萃取剂。本方法灵敏、准确,可作为阿托伐他汀I期临床研究的试验方法
[1] Plosker GL, Wagstaff AJ. Fluvastatin: a review of its pharmacology and use in the management og hypercholesterolaemia[J]. Drμgs, 1996, 51: 433.
[2] Naoumova RP, Marais AD, Mountney J,etal. Plasma mevalonic acid, an index of cholesterol synthesis in vivo and responsiveness to HMG-CoA reductase inhibitors in familial hypercholesterolaemia[J]. Atherosclerosis, 1996, 119: 203.
[3] 胡晓玲,李环德. UPLC-MS/MS法测定健康人血浆中的阿托伐他汀浓度及药物代谢动力学研究[J].中南药学,2008,6(4):400.
[4] 董 婧, 陈西敬, 宋 捷, 等. 阿托伐他汀大鼠体内药动学及肠肝循环研究[J]. 中国药科大学学报,2008,39(1):55.
2010-05-18
[修回日期] 2010-09-09
DeterminationofAtorvastatininhumanplasmabyLC-MS-MS
Jiang Nan,Yang Yong-Ge,Xu Xue-Ting,Zhao Gang-Tao
(Department of Pharmacy,General Hospital of Beijing Military Command of PLA,Beijing 100700,China)
ObjectiveTo establish a method for determining Atorvastatin in human plasma by LC-MS-MS.MethodsAtorvastatin was extracted for determination by LC-MS-MS. Analytical column was Thermo BioBasic-C8(2.1 mm×100 mm,5 μm). The mobile phase was acetonitrile(0.1%acid):water(0.1%acid)=70:30. Mass spectrum conditions was ESI performing in the SRM mode using target ions m/z 558→278(30EV)(Atorvastatin ), m/z 269→106(22 EV)(tolbutamide), SP 3 500 KV, SGP 10 Arb, AGP 15 Arb, TEM 314 ℃.ResultsThe calibration curve was linear over the range of 0.1~20 μg/L. The LLOQ of Atorvastatin in plasma was 0.1 μg/L. The extracted recovery was>70%. The intra-and inter-dayRSDwere<15%.ConclusionThe method is sensitive, simple and accurate to determinate Atorvastatin plasma concentration and suitable to study phase I clinical test of Atorvastatin.
Atorvastatin; plasma concentration; LC-MS-MS
姜 楠(1977-),女,硕士,主管药师.Tel:(010)66721899,E-mail:jiangnan7757@163.com.
R917
A
1006-0111(2011)01-0015-03
