庆大霉素发酵工艺的研究
2011-10-31陈梁军
陈梁军
(福建生物工程职业技术学院,福建 福州 350002)
庆大霉素发酵工艺的研究
陈梁军
(福建生物工程职业技术学院,福建 福州 350002)
目的通过对庆大霉素发酵条件的优化,提高发酵生产的能力。方法以绛红色小单孢菌2-25为对象,通过单因素试验和四因素三水平(4×3)正交试验筛选出了菌株2-25的最佳培养基配方及培养条件。结果该菌种的最佳发酵条件:5.0%玉米淀粉,3.0%黄豆饼粉,0.6%蛋白胨,0.15%硝酸钾,在33℃、pH 7.8、接种量25%,培养84h,产品质量符合中国药典2005版(CP2005)、美国药典28(USP28)。结论优化发酵条件后菌株2-25发酵水平明显提高。
庆大霉素;绛红色小单孢菌;发酵;正交试验
庆大霉素(Gentamicin)是由绛红色小单孢菌(Micromonmspora purpurea)产生的氨基糖苷类抗生素,对革兰阳性、革兰阴性菌特别是对铜绿假单胞菌和金黄色葡萄球菌有良好的抗菌效能,临床肌内(静脉)注射后吸收迅速、完全,故被广泛应用于消炎退热;同时,发现口服给药在体内难以吸收,在肠道中保持较高浓度,确保其杀菌效果,又被临床用于胃肠道和呼吸道感染。后又发现能促进饲料的利用率,在禽畜体内不留残毒或低残毒[1],于是又被广泛用于畜牧业,生产“绿色食品”。
我国生产的庆大霉素大部分出口。但由于小单孢菌产素率低,发酵用料多,周期长,因此生产成本高。为了提高我国在国际市场的竞争力,改进庆大霉素的生产方法已势在必行。庆大霉素自1963年问世以来,生产徘徊在一定范围水平,且生产周期较长,国内外均在120~140h。庆大霉素生产水平低的原因主要有:①菌种代谢合成能力有限;②孢子发芽率很低,新鲜培养的菌种发芽率仅有15%~20%;③代谢合成过程要求溶氧很高等,一般很难满足[2]。根据绛红色小单孢菌合成氨基糖苷类抗生素和合成抗生素过程中初级代谢与次级代谢的关系,进行正交设计改变培养基的成分和发酵培养条件,通过摇瓶小试,30L发酵中试的基础上,在100m3发酵罐中进行培养,取得突破性进展。发酵周期较原工艺缩短约35%,发酵指数提高约43%,产品质量符合中国药典2005版(CP2005)、美国药典28版(USP28)。
1 材料与方法
1.1 菌种
绛红色小单孢菌2-25由福建省福抗药业股份有限公司保存。
1.2 培养基
斜面及平板分离培养基(%): 麸皮1.5%、琼脂2.0%、碳酸钙0.05%、天门冬酰胺0.01%,磷酸二氢钾0.03%、硫酸镁0.05%、氯化钠0.05%、硝酸钾0.2%和玉米淀粉1.0%,消前pH 6.3~6.5。
一级种子培养基(%):葡萄糖0.2%、玉米淀粉1.2%、玉米粉2.0%、蛋白胨0.3%、黄豆饼粉1.2%、碳酸钙0.7%、氯化钴0.002%、硝酸钾0.1%,消前pH 7.5~7.6。
二级种子培养基(%):葡萄糖0.3%、玉米淀粉2.0%、玉米粉0.5%、蛋白胨0.4%、黄豆饼粉2.0%、碳酸钙0.7%、氯化钴0.001%,硫酸铵0.1%、硝酸钾0.1%,淀粉酶0.01 %和泡敌0.02%,消前pH 7.5~7.6。
酵培养基(%):葡萄糖0.5%、玉米淀粉5.0%、玉米粉1.0%、蛋白胨0.6%、黄豆饼粉3.0%、碳酸钙0.7%、氯化钴0.001%、硫酸铵0.1%、硝酸钾0.15%、淀粉酶0.02%和泡敌0.03%, 消前pH 7.5~7.6。
1.3 培养条件
斜面及平板培养条件:培养温度33℃,相对湿度45~65%,培养4~5d。
种子培养条件:培养温度34℃,相对湿度45~65%,摇瓶装量30mL/250mL三角瓶,摇床转速320r/min,培养48h。
发酵培养条件:培养温度33℃,相对湿度45%~65%,摇瓶装量30mL/250mL三角瓶,摇床转速320r/min,接种量25%,培养4d。
30L小试发酵罐培养条件:培养温度33℃,通气1∶1.5(vvm),罐压0.02Mpa,搅拌转速600 r/min,接种量25%,培养4d。
100m3发酵罐培养条件:培养温度33℃,通气1∶1.2(vvm),罐压0.02Mpa,搅拌转速140 r/min,接种量25%,培养4d。
1.4 发酵条件的优化
1.4.1 初始pH值对抑菌物质产生的影响
在30L发酵罐中采用优化培养基配方配制培养基,将培养液初始pH分别调至6.9、7.2、7.5、7.8、8.1、8.4。摇瓶发酵,测定发酵液生物效价。为排除pH干扰。将终发酵液pH全部调至7.0进行实验。
1.4.2 培养温度对抑菌物质产生的影响
在优化培养基和最适pH下,分别选取了27℃、30℃、33℃、36℃、39℃作为菌株的发酵培养温度,摇瓶发酵。实验方法同上,测发酵液生物效价。
1.4.3 发酵时间对抑菌物质产生的影响
在优化培养基和最适pH及最佳温度下,摇瓶培养。实验方法同上,每12h取发酵液测定生物效价。
1.5 分析方法
1.5.1 总糖和还原糖的测定
斐林试剂法[3]。
1.5.2 氨基氮的测定
甲醛法[3]。
1.5.3 生物效价的测定
按照中国药典2005版(CP2005),抗生素微生物检定法(附录XIA),质量检测按照中国药典2005版规定。
1.6 正交试验设计
将玉米淀粉、蛋白胨、黄豆饼粉和硝酸钾四个因素设3个水平选择无交叉作用的正交表L9(34)[4],进行发酵培养基优化试验。试验设计如表1。

表1 正交试验因素与水平
2 结 果
2.1 初始pH对产抑茵活性物质的影响
分别调节发酵培养基的初始pH为6.9、7.2、7.5、7.8、8.1、8.4,进行发酵培养,测定发酵液生物效价。结果显示该菌株在pH 6.9~8.4均有抑菌物质产生。在pH 7.8时达到最大值,pH超过7.8产抑菌物质量下降。
2.2 培养温度对产抑茵活性物质的影响
以初始pH 7.8的培养基接种2-25菌悬液,分别置于27℃、30℃、33℃、36℃、39℃摇瓶培养,结果在33℃左右,2-25菌株产抑菌物质量最高。
2.3 发酵时间对产抑茵活性物质的影响
以初始pH 7.8的培养基接种2-25菌悬液,分别置于33℃摇瓶培养,每隔12h测定生物效价,结果显示发酵生物效价随着培养液培养时间的延长而增加,84h后,生物效价不再增加,说明2-25菌株在培养到84h时生物效价达最高峰。
2.4 正交试验结果
以玉米淀粉,蛋白胨,黄豆饼粉,硝酸钾四个因素进行正交试验,试验结果见表2。由表中极差可见 RC>RB>RD>RA。即4个因素对发酵影响的强度依次为黄豆饼粉、蛋白胨、硝酸钾、玉米淀粉。其最佳配比为A1B2C1D3。由试验得出菌株2-25的最佳发酵培养基组成为黄豆饼粉3.0%,蛋白胨0.6%,硝酸钾0.15%,,玉米淀粉5.0%。
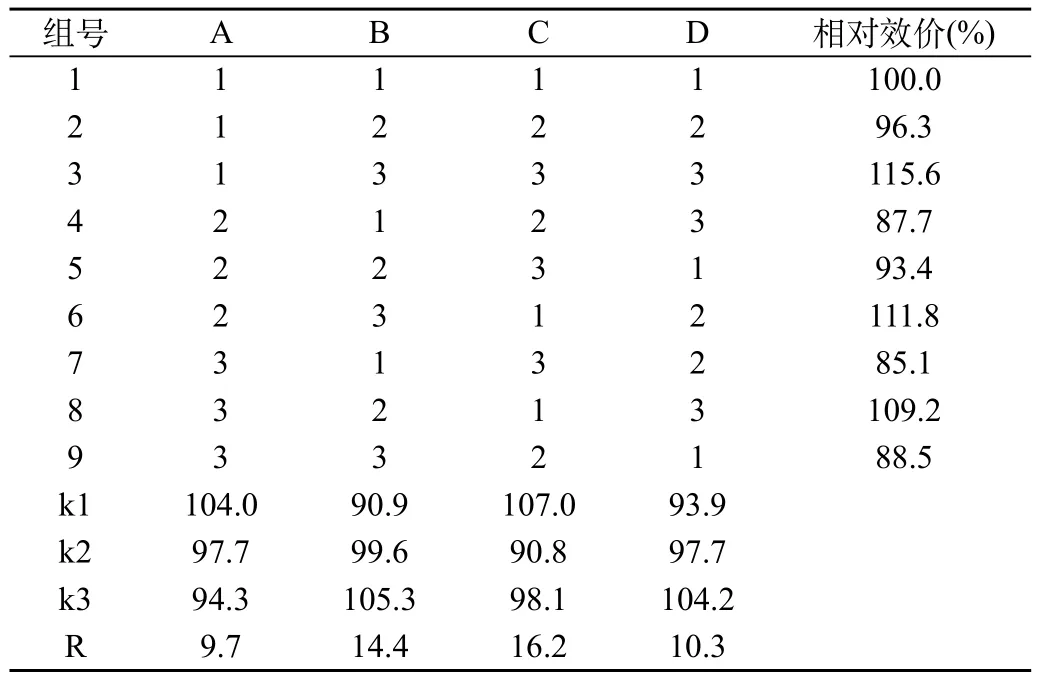
表2 L9(34)正交试验
2.5 验证试验
应用优化后的发酵培养基配方,在100m3发酵罐连续生产60批,发酵周期为84h较原工艺缩短约35%,发酵指数为1.3839较原工艺提高约43%,产品按照中国药典2005版(CP2005)进行组分检测:C1为27.8%,C1a为29.7%,C2a+C2为42.5%,符合CP2005标准(C1应为25%~50%,C1a应为15%~40%,C2a+C2应为20%~50%),也符合美国药典28版(USP28)。
3 讨 论
用正交试验优选得到的发酵培养基达到提高发酵水平的目的,发酵周期较原工艺缩短约35%,发酵指数提高约43%,产品质量符合中国药典2005版(CP2005)、美国药典28(USP28)。本试验就庆大霉素发酵工艺条件和培养基配方进行了初步的筛选,对其高产菌种选育工作有待进一步研究。
[1]沈川,肖希龙.新霉素在动物体内的残留及其测定方法[J].中国兽医杂志,1998,32(2):53-56.
[2]管玉霞,刘树滔.几种氨基酸在庆大霉素生产中的作用[J].中国生物工程杂志,2007,27(12):95-100.
[3]Chen JM,Xu LD.Antibiotic industry analysis [M].Beijing:Chinese Medical Technology Publishing House,1991:109.
[4]夏志兰,喻桃生,周连玉等.灵芝液体发酵条件的优化研究[J].微生物学杂志,2007,27(2):10-15.
Research of Fermentation Technology for Production of Gentamicin
CHEN Liang-jun
(Fujian Biological Engineering Vocational and Technical College, Fuzhou350002, China)
ObjectiveImprove fermentation production ability by optimization of the Gentamicin fermentation condition.MethodsThe optimum fermentation medium and culture condition of Gentamicin 2-25 was obtained by using one-factor experimental design and Four factor three level orthogonal experimental design.ResultsThe optimum fermentation formulation: 5.0% corn starch,3.0% soybean powder,0.6% peptone,0.15% potassium nitrate.It was cultured at 33℃ and pH 7.8 for 84h with 25% of inoculation numbers.The product quality conformed to China Pharmacopoeia 2005 (CP2005) and the United States Pharmacopoeia 28 (USP28).ConclusionAfter optimization,the fermentation level of strains 2-25 was greatly improved.
Gentamicin; Micromonmspora purpurea; Fermentation; Orthogonal experiments
R978.1+2
B
1671-8194(2011)33-0247-03
