米糠白酶角物锌螯合物的制备工艺
2011-10-09王松华孙玉军马玉涵史芳芹
张 强,王松华,孙玉军,马玉涵,史芳芹
(安徽科技学院生命科学学院,安徽蚌埠233100)
米糠白酶角物锌螯合物的制备工艺
张 强,王松华,孙玉军,马玉涵,史芳芹
(安徽科技学院生命科学学院,安徽蚌埠233100)
研究了米糠蛋白酶解物锌螯合物的制备工艺。通过单因素实验分析了米糠蛋白酶解物的制备方法、米糠蛋白酶解物与锌质量比和pH对螯合反应的影响,在此基础上利用正交实验优化螯合物的制备工艺。结果表明,米糠蛋白酶解物锌螯合物的最佳制备工艺为:米糠蛋白酶解物的制备方法为胃蛋白酶结合中性蛋白酶法,米糠蛋白酶解物与锌质量比2∶1,pH 8.0,此条件下螯合物得率和螯合率分别为94.93%和94.85%。
米糠,锌,酶解,螯合物
锌是细胞生长、增殖所必需的微量元素,是许多金属酶的组成成分或一些酶的激活剂,在儿童生长发育中起重要作用。尽管自然界中锌源十分丰富,但锌在人体内的吸收代谢受种种因素的限制,锌缺乏已成为我国及许多发展中国家亟待解决的公共卫生问题[1]。目前的补锌制剂主要有无机锌、有机锌和氨基酸螯合锌。前两类存在稳定性差、受肠道内容物影响大及吸收率低等缺点。第三类与前两类产品相比,具有稳定性好、抗干扰力强、易吸收和生物利用率高等优点,并具有补充微量元素和氨基酸的双重作用,但由于价格较高,限制了其在生产上的应用。早在20世纪70年代,就有研究者发现氨基酸和小肽具有促进锌吸收的作用,而且氨基酸或肽的金属复合体如Fe、Zn和Cr的生物学利用率比无机盐高,无毒副作用[2],因此,研究开发这种生物态锌——蛋白酶解物螯合锌,具有十分重要的意义。目前,大豆蛋白、丝素蛋白、酪蛋白等诸多蛋白酶解物与锌的螯合条件及其螯合物的生物活性方面已受到普遍关注[3-6],但对米糠蛋白酶解物锌螯合物的制备工艺的研究尚未见报道。米糠是糙米碾白过程中被碾下的皮层及少量米胚和碎米的混合物,是一种廉价、低利用率但营养丰富的稻米加工副产品[7],联合国工业发展组织把米糠称为一种未充分利用的原料[8]。因此,本文以米糠为原料,研究其酶解物与锌的螯合工艺,以促进米糠深加工产业的发展,增加农民收入,同时也为生物态锌的研究开发及工业化生产提供有益的借鉴和参考。
1 材料与方法
1.1 材料与仪器
脱脂米糠蛋白 实验室自制;胰蛋白酶、胃蛋白酶和中性蛋白酶 中国医药集团上海化学试剂公司;其他试剂 均为国产分析纯。
HH-4型数显恒温水浴锅 国华电器有限公司;高速冷冻离心机 上海安亭科学仪器厂;Phs-3C型精密pH计 上海精密科学仪器有限公司;真空冷冻干燥机 北京博医康实验仪器有限公司;SHB-B95型循环水式多用真空泵 郑州长城科工贸有限公司;101AS-3型数显恒温干燥箱 上海浦东跃欣科学仪器厂;756MC紫外可见分光光度计 上海精科公司分析仪器总厂。
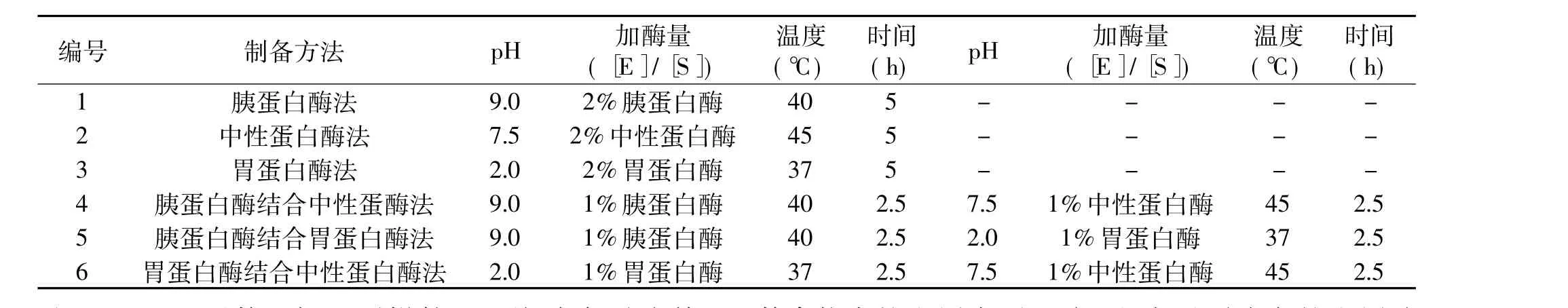
表1 米糠蛋白酶解物的制备
1.2 实验方法
1.2.1 米糠蛋白酶解物的制备 质量分数3%的米糠蛋白悬浮液于90℃恒温水浴锅中热变性处理15m in,冷却后按表1的六种方法水解米糠蛋白(期间用1mol/L的HCl或NaOH维持pH恒定),反应结束后,沸水浴5m in灭酶活,12000 r/m in离心10m in,上清液冷冻干燥,即为米糠蛋白酶解物。
1.2.2 螯合物的制备 米糠蛋白酶解物溶液与氯化锌溶液按一定比例混合→调pH→50℃恒温水浴1h→4000r/min离心20min→沉淀95%乙醇洗涤抽滤→沉淀用少量乙醚洗涤抽滤→80℃热风干燥→螯合物
1.2.3 螯合物得率和螯合率 锌含量按GB8820-1988测定。米糠蛋白酶解物螯合锌盐的能力和效果用螯合率和螯合物得率表示,其计算公式为:
螯合物得率(%)=W/W0×100%
式中:W0:米糠蛋白酶解物与锌的质量和(g);W:米糠蛋白酶解物锌螯合物质量(g)
螯合率(%)=W/W0×100%
式中:W0:反应体系中锌的质量(g);W:螯合物中锌的质量(g)
1.2.4 鳌合物制备条件的优化
1.2.4.1 鳌合物制备的单因素实验 以鳌合物得率和鳌合率为指标分别考察米糠蛋白酶解物的制备方法、pH、米糠蛋白酶解物与锌质量比三个因素对鳌合物制备的影响,其中制备方法六种(表1),pH设定五个梯度(2、4、6、8、10),米糠蛋白酶解物与锌质量比设定五个梯度(2∶1、4∶1、6∶1、8∶1、10∶1)。
1.2.4.2 鳌合物制备的正交实验 单因素实验中,每组实验只考察一个因素,而螯合反应的最佳条件并不是简单地将所有这些单因素实验的最佳结果叠加在一起,还必须通过正交实验考察多因素的叠加效果,故基于以上单因素实验结果,采用L9(33)正交表设计正交实验,各因素水平的设定如表2所示。

表2 正交实验的因素水平表
1.2.5 螯合物的鉴定[9]由于金属硫化物的稳定常数远大于螯合物的稳定常数,当加入硫化钠时,S2-与螯合物中的金属离子反应,生成了更稳定的金属硫化物沉淀,从而使螯合物中的氨基酸或小肽游离出来。可以利用螯合物这一特有的性质来对样品进行定性鉴定。
取纯化后的螯合物0.5g,先用少量盐酸溶解,再加20m L蒸馏水和几滴茚三酮指示剂,煮沸3~5m in,观察颜色变化。另取纯化后的螯合物0.5g,先用少量盐酸溶解,再20m L蒸馏水,再加入过量的固体硫化钠,搅拌,静置,出现白色沉淀。过滤,滤液加几滴茚三酮指示剂,煮沸3~5m in,观察颜色变化。
2 结果与分析
2.1 单因素实验
2.1.1 米糠蛋白酶解物制备方法对螯合反应的影响
不同的米糠蛋白酶解物由于制备时采用的蛋白酶不同,米糠蛋白的水解度不同,得到的米糠蛋白酶解物也就存在较大差异,这直接会影响到螯合物得率和螯合率。在米糠蛋白酶解物与锌质量比为4∶1,pH5.0条件下,米糠蛋白酶解物的制备方法对螯合反应的影响如图1所示。从图1可以看出,米糠蛋白酶解物的制备方法对螯合反应影响较明显,其中胰蛋白酶结合胃蛋白酶法的鳌合物得率和鳌合率最高。

图1 米糠蛋白酶解物制备方法对螯合反应的影响注:图中数字对应的方法见表1。
2.1.2 pH对螯合反应的影响 pH是螯合物制备的重要影响因素。在pH较低的酸性条件下,H+将与金属离子Zn2+竞争供电子基团,不利于螯合物的生成;在pH较高的碱性条件下,OH-与供电子基团争夺金属离子Zn2+而易形成氢氧化锌沉淀。用胰蛋白酶结合胃蛋白酶法制备的米糠蛋白酶解物与Zn2+螯合,米糠蛋白酶解物与锌质量比为4∶1,此条件下pH对螯合反应的影响如图2所示。
从图2可以看出,随着pH的升高,螯合物得率与螯合率逐渐增大,当pH为8.0时,螯合物得率与螯合率均达到最大,再增加pH,螯合物得率与螯合率开始下降。
2.1.3 米糠蛋白酶解物与锌质量比对螯合反应的影响 米糠蛋白酶解物与锌的质量比对螯合反应的影响很大。若比值过大,米糠蛋白酶解物的利用率下降,造成原料浪费;比值过小,螯合反应不显著,生成的螯合物不稳定。用胰蛋白酶结合胃蛋白酶法制备的米糠蛋白酶解物与Zn2+螯合,pH8.0,此条件下米糠蛋白酶解物与锌质量比对螯合反应的影响如图3所示。
由图3可知,对螯合物得率而言,米糠蛋白酶解物与锌的质量比为2∶1时,螯合物得率最大,再增大米糠蛋白酶解物与锌的质量比,螯合物得率明显下降;对螯合率而言,米糠蛋白酶解物与锌的质量比为2∶1和4∶1时均有较大的螯合率,再增大质量比,螯合率变化不明显。

图2 pH对螯合反应的影响
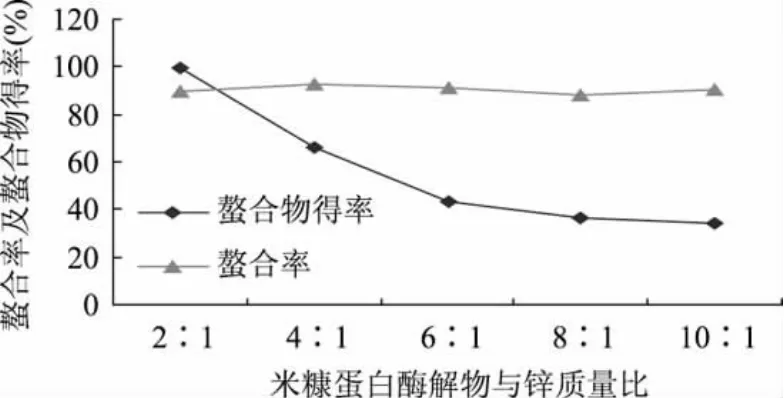
图3 米糠蛋白酶解物与锌质量比对螯合反应的影响
2.2 正交实验
正交实验结果见表3。极差大小可反映各因素对指标影响的程度。由表3的极差分析可看出,影响螯合物得率和螯合率的所选因素的主次顺序均为B>C>A,即米糠蛋白酶解物与锌质量比>pH>米糠蛋白酶解物的制备方法;最佳的螯合工艺条件为A1B1C1,即米糠蛋白酶解物的制备方法为胃蛋白酶结合中性蛋白酶法,米糠蛋白酶解物与锌质量比为2∶1,pH 8.0,此条件下螯合物得率和螯合率均最大,分别为94.93%和94.85%。
2.3 螯合物的鉴定结果
未加硫化钠的螯合物样品水溶液,用茚三酮试剂检测,溶液颜色没有发生改变;加入过量的硫化钠后得到的滤液,用茚三酮试剂检测,溶液变为紫红色,即原样品溶液中没有游离的氨基酸或小肽,加入过量的硫化钠生成了ZnS沉淀以后,有了游离的氨基酸或小肽。这说明待测物质是米糠蛋白酶解物和锌离子形成的一种特殊物质,这种物质就是米糠蛋白酶解物与锌的螯合物。

表3 正交实验结果与分析
3 结论
在本实验条件下米糠蛋白酶解物与锌质量比是影响螯合反应的最主要因素,最佳的螯合工艺条件为:米糠蛋白酶解物的制备方法胃蛋白酶结合中性蛋白酶法,米糠蛋白酶解物与锌质量比2∶1,pH 8.0,此条件下螯合物得率和螯合率分别为94.93%和94.85%。
[1]刘成梅,杨珊珊,刘伟.响应面法优化罗非鱼皮胶原多肽螯合锌的制备工艺[J].食品科学,2008,29(11):189-192.
[2]乔伟,周安国,王之盛,等.小肽促进微量元素吸收的研究进展[J].饲料工业,2006,27(17):12-14.
[3]高素蕴,潘思轶,郭康权.大豆分离蛋白酶解物螯合锌(Ⅱ)的合成与制备[J].食品科学,2003,24(10):117-120.
[4]邱冬玲,胡长利,崔建云.丝素肽与锌螯合工艺条件的研究[J].食品研究与开发,2008,29(7):38-42.
[5]张志,王旭,王强,等.不同因素对酪蛋白酶解产物与锌盐螯合效果的影响[J].食品科学,2009,30(9):129-132.
[6]赵海军,王宝贵,张桂英,等.大豆多肽螯合锌对自然衰老小鼠的作用[J].中国老年学杂志,2009,29(12):1501-1502.
[7]杨草.稻米副产品的综合开发利用[J].中外技术情报,1992(6):5.
[8]陈正行,姚惠源,周素梅.米糠和米糠蛋白开发利用[J].粮食与油脂,2002(4):6-9.
[9]吴茹怡,曾里,曾凡骏.复合氨基酸螯合物鉴定方法的研究[J].食品科技,2006(3):104-107.
Study on preparation technology of rice bran protein hydrolysate chelated w ith zinc
ZHANG Qiang,WANG Song-hua,SUN Yu-jun,MA Yu-han,SHIFang-qin
(Life Science College,Anhui Science and Technology University,Bengbu 233100,China)
Chelation process of rice bran protein hydrolyses w ith the zinc was studied.Three main factors including preparation methods of the rice bran protein hydrolysate,mass ratio of rice bran protein hydrolysate to zinc and pH were investigated by using single factor analysismethod.On this basis,the optimal chelation technology was obtained by orthogonal experim ent.The experim ental results showed that the best technical conditions for preparation of chelate were as follows:pepsin combined w ith neutral protease was used for preparation of rice bran hydrolysate,m ass ratio of rice bran protein hydrolysate to zinc was 2 to 1,pH 8.0,under this conditions the yield rates and chelate ratio was 94.93%and 94.85%respectively.
rice bran;zinc;hydrolysis;chelate
TS210.1
B
1002-0306(2011)06-0281-03
2010-06-04
张强(1979-),男,硕士,讲师,主要从事农产品贮藏与加工方面的研究。
安徽省高校青年科研资助计划项目资助(2006jql197);安徽科技学院生物学校级重点建设学科项目资助(AKXK20102-1)。
