芦丁 /羟丙基 -β-环糊精包合物的表征及其抗氧化能力研究
2011-09-29苏彩娟王金水刘本国陈永生胡立志
苏彩娟,王金水*,刘本国,陈永生,胡立志
(1.河南工业大学粮油食品学院,河南郑州 450052;2.河南科技学院食品学院,河南新乡 453003)
芦丁 /羟丙基 -β-环糊精包合物的表征及其抗氧化能力研究
苏彩娟1,王金水1*,刘本国2,陈永生2,胡立志2
(1.河南工业大学粮油食品学院,河南郑州 450052;2.河南科技学院食品学院,河南新乡 453003)
采用溶液法制备芦丁 /羟丙基 -β-环糊精包合物,以提高芦丁的水溶性,并采用紫外(UV)、红外 (IR)、X-射线衍射 (XRD)等方法对该包合物的结构进行了表征.结果表明:该包合物在 DPPH自由基清除试验、还原力测定和 Rancimat法中都显示出较强的抗氧化能力.
芦丁;羟丙基 -β-环糊精;包合物;抗氧化
0 前言
芦丁 (Rutin)又名芸香苷,是存在于植物中的一种类黄酮化合物,具有抗菌、消炎、抗辐射、抗氧化等多种生物活性,并且可以调节毛细血管壁的渗透性和降低血管的脆性[1-3].芦丁来源广泛,非常适合在功能性食品中添加,但芦丁的水溶性过低,限制了其在食品工业中的应用.羟丙基 -β-环糊精 (HP-β-CD)是β-环糊精的醚化衍生物,较β-环糊精其水溶性大大提高 (>500 g/L,20℃),溶血性更低,具有更高的安全性,甚至可以用于静脉注射,美国食品药品监督局已经批准其在制药和食品中应用[4-5].作者对芦丁 /HP-β-CD包合物的结构进行了表征,并考察其抗氧化活性.
1 材料与方法
1.1 材料与试剂
芦丁:国药集团化学试剂有限公司;羟丙基 -β-环糊精:上海西宝生物科技有限公司;二苯代苦味酰自由基:美国 Sigma公司;其他试剂均为分析纯.
1.2 仪器与设备
TU—1810PC型紫外可见光光度计:北京普析通用仪器有限公司;7200型可见光分光光度计:尤尼柯 (上海)仪器有限公司;TENSOR 27型红外光谱仪:德国Bruker公司;D/MAX 2500V/PC型 X—射线衍射仪:日本理光公司;Alpha1—4冷冻干燥机:德国 CHR IST公司;BS124S电子分析天平:赛多利斯科学仪器北京有限公司;Rancimat743型食用油氧化稳定性测定仪:瑞士万通公司;85—2型恒温磁力搅拌器:上海司乐仪器有限公司.
1.3 试验方法
1.3.1 芦丁 /羟丙基 -β-环糊精包合物的制备
芦丁/HP-β-CD包合物的制备采取溶液法,按照 Pfitzner等[6]和 Chen等[7]的方法,并加以改进.为寻求 HP-β-CD与芦丁的最佳配比,用无水乙醇配制一定摩尔浓度的芦丁溶液,使 HP-β-CD与芦丁的摩尔浓度比分别为 1︰1、2︰1、3︰1、4︰1、5︰1、6︰1.室温下 ,混合溶液用磁力搅拌器搅拌 24 h,然后转移到圆底烧瓶旋转蒸发至干除去乙醇.向烧瓶内加入 100 mL冷水使其中的残留物充分溶解.芦丁在冷水中的溶解度极低(0.0013%).抽滤得透明溶液,芦丁作为残渣留在滤膜上.将透明溶液移入已称重的培养皿中(m1),冷冻干燥得黄色固体即包合物,称量包合物与培养皿的总质量 (m2).计算包合物得率98.0%、88.65%、98.97%、99.10%、99.79%.但HP-β-CD与芦丁的摩尔浓度比太大,会降低芦丁在包合物中的比例,所以采用 HP-β-CD与芦丁的摩尔浓度比 4︰1制备包合物,即称取 0.33 g芦丁用 30 mL无水乙醇溶解,然后加入 2.8 g HP-β-CD制备包合物.
1.3.2 芦丁 /羟丙基 -β-环糊精物理混合物的制备
称取芦丁 0.33 g、HP-β-CD 2.8 g,室温下在烧杯中搅拌混匀,得芦丁与 HP-β-CD的物理混合物.
1.3.3 芦丁 /羟丙基 -β-环糊精包合物的物相表征
1.3.3.1 紫外及红外分析
分别称取芦丁、HP-β-CD、芦丁与 HP-β-CD的物理混合物及包合物各 10 mg,用无水甲醇定容到 10 mL的容量瓶中,适当稀释后,分别在220~500 nm波长范围内进行紫外吸收波长的扫描.取红外灯干燥后的各样品用溴化钾压片后,置于 TENSOR 27型红外光谱仪中记录其红外光谱.1.3.3.2 X-射线衍射分析
取适量的芦丁、HP-β-CD、芦丁与 HP-β-CD的物理混合物及包合物,进行 X-射线衍射,采用 Cu Ka靶,石墨单色器衍射单色化,衍射角扫描范围为 5°~60°.
1.3.4 芦丁 /羟丙基 -β-环糊精包合物的抗氧化能力测定
1.3.4.1 DPPH自由基清除试验
参照文献[8]的方法,分别吸取 2 mL不同浓度的样品溶液,加入 2.0 mL 2×10-4mol/L的DPPH无水乙醇溶液,摇匀后,室温下在黑暗处放置 30 min.以无水乙醇调零,测定 517 nm处的吸光值 A样品.同时,测定 2.0 mL样品溶液与 2.0 mL无水乙醇混合液在 517 nm处的吸光值A空白,再测定 2.0 mL DPPH溶液与 2.0 mL无水乙醇在 517 nm处的吸光值 A对照.
DPPH自由基清除率 (%)=[1-(A样品-A空白)/A对照]×100%.
1.3.4.2 还原力测定
参照文献[9]的方法,不同浓度的样品溶液0.5 mL加入 2.5 mL磷酸盐缓冲液 (pH 6.6,0.2 mol/L)及 2.5 mL 1%K3Fe(CN)6,于 50 ℃水浴中反应 20 min后迅速冷却,加入 2.5 mL 10%的三氯乙酸溶液,3 000g离心 10 min,取上清液 2.5 mL,并加入 2.5 mL蒸馏水及 0.5 mL 0.1%FeCl3溶液,混合均匀,10 min后,测定 700 nm处的吸光值.吸光值越大,则样品的还原力越强.
1.3.4.3 Ranci mat抗氧化能力测定
参考 Proestos等[10]的方法,分别取 3 g猪油至 Rancimat仪的样品管,调节空气流量为 20 L/h,设定温度为 110℃.准确称取相同质量的芦丁、包合物及 BHT,用同体积的无水乙醇溶解,并将其加入到猪油样品中,样品的添加量为 0.02%的油样.以猪油中添加相应量的无水乙醇为空白,测定各样品的诱导时间,并按照下式计算保护系数:PF=IP样品/IP对照.
2 结果与分析
2.1 紫外及红外分析(图 1、图 2)
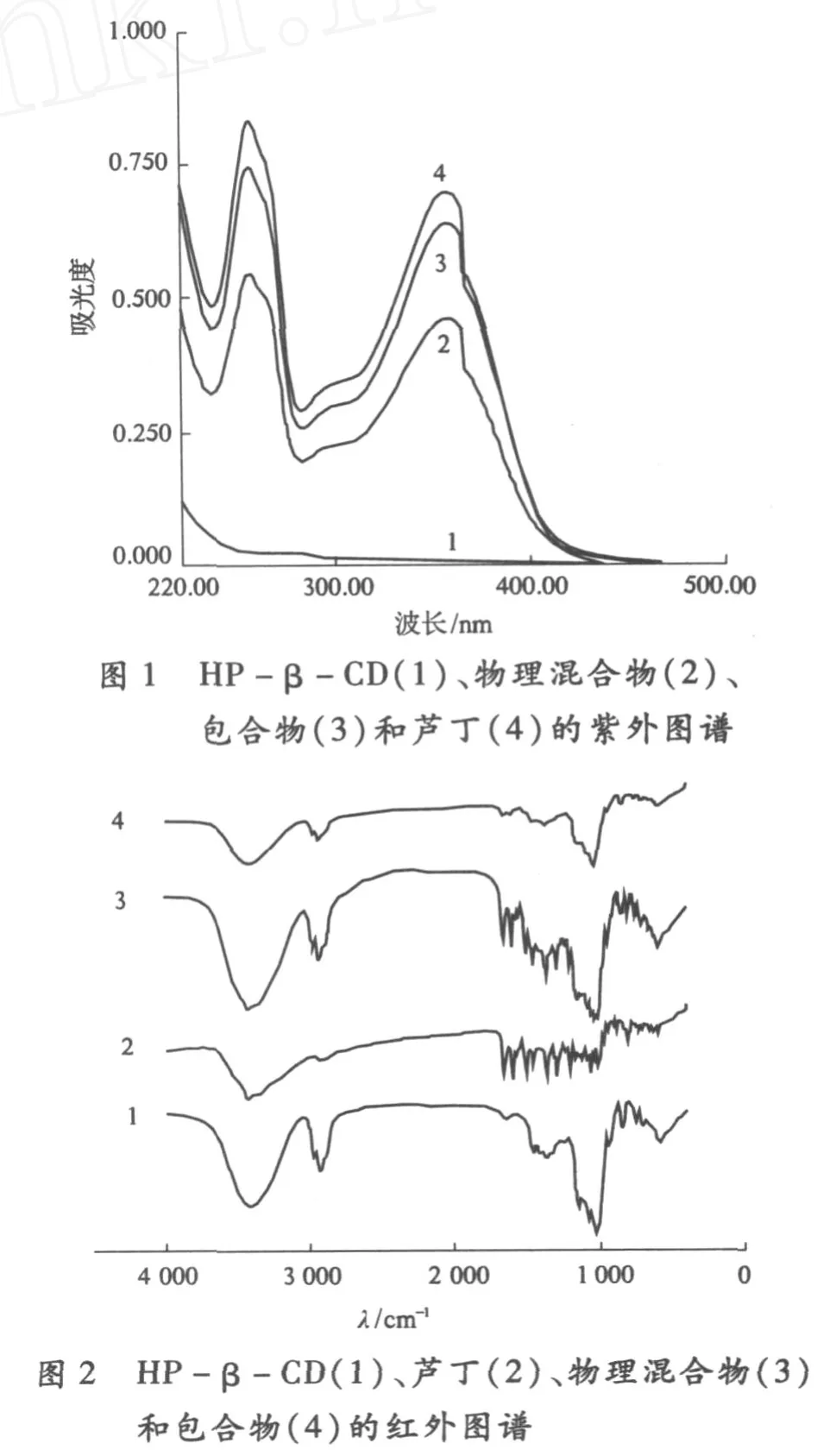
如图 1所示,芦丁与芦丁 /HP-β-CD包合物及它们的物理混合物在紫外吸收峰上没有差异,它们的紫外特征吸收峰都在 256 nm和 358 nm处,而 HP-β-CD在扫描范围内没有特征吸收峰.在图 2中,芦丁 /HP-β-CD包合物与 HP-β-CD的红外图谱非常相似,只是芦丁在 500~1 500 cm-1之间的一些小的吸收峰几乎被 HP-β-CD掩盖.由紫外和红外分析可推断在芦丁 /HP-β-CD包合物形成的过程中,芦丁与 HP-β-CD以非共价键形式相结合.
2.2 X-射线衍射分析
图 3中,芦丁的衍射图表现出许多尖峰表明其为结晶态,而 HP-β-CD无尖峰,为无定形状态.芦丁与 HP-β-CD制成物理混合物后,能在一定程度上使芦丁特征结晶峰减弱,制备成包合物后,由于 HP-β-CD的作用,芦丁的结晶峰消失.通过 X-射线衍射分析可知芦丁在包合物中以无定形状态存在.
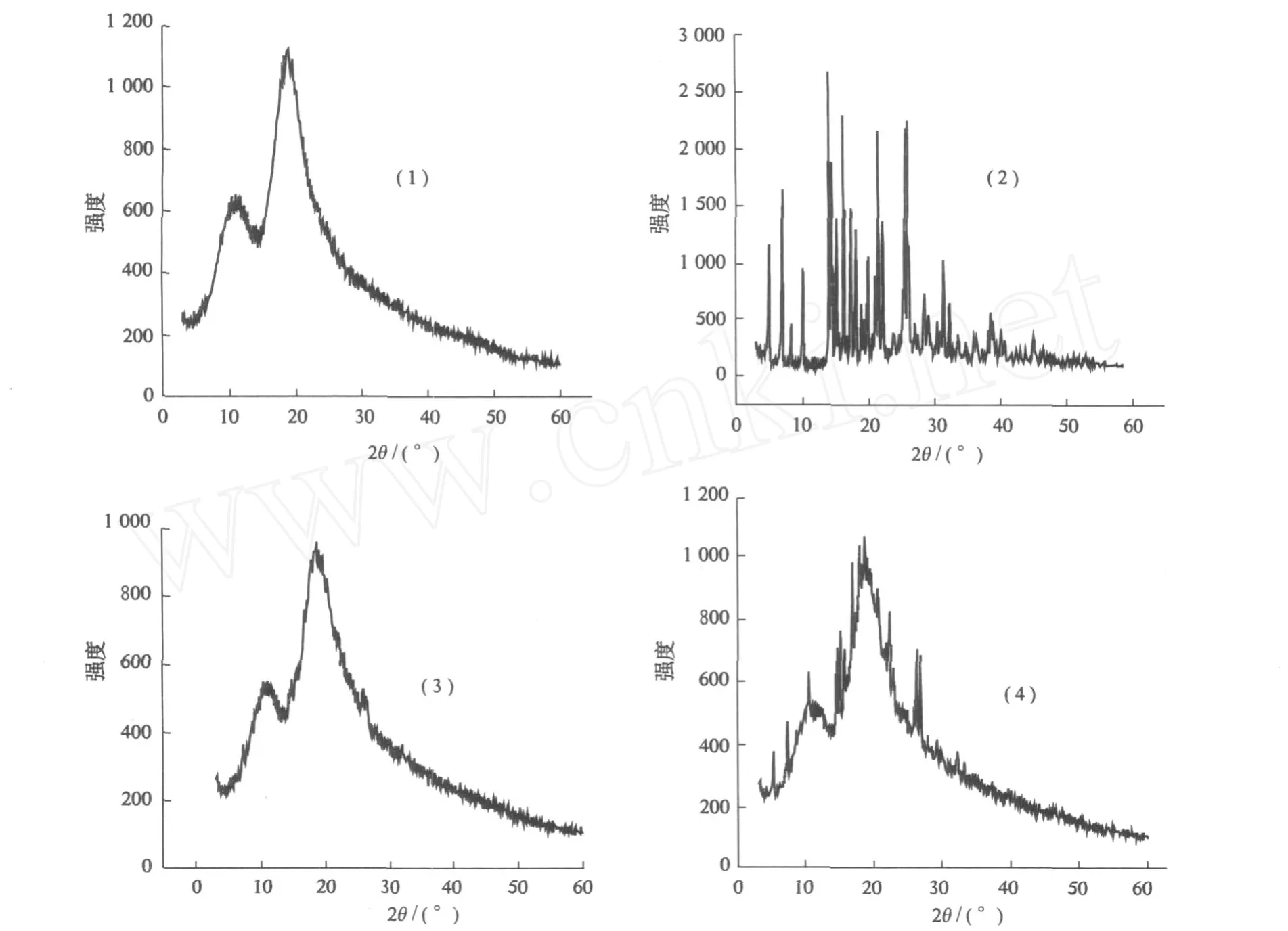
图3 HP-β-CD(1)、芦丁 (2)、包合物 (3)和物理混合物 (4)的 X-射线图谱
2.3 DPPH自由基清除力
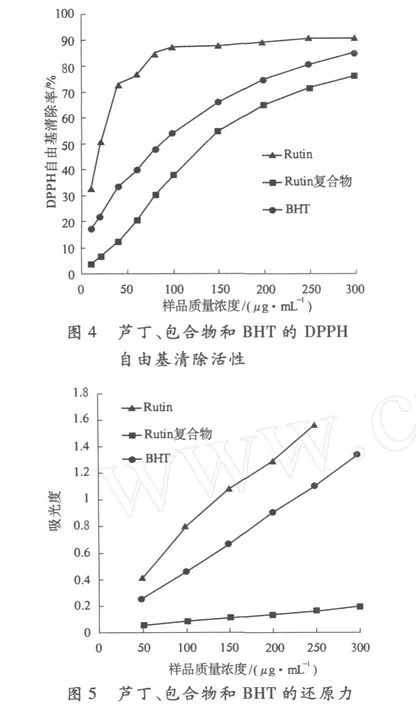
研究表明,自由基与机体许多疾病的发生有关.因此,研究自由基的检测方法并探讨物质对自由基的清除作用具有重要意义[11-12].DPPH(二苯代苦味酰自由基)分析法被广泛用于清除自由基物质性质的研究,DPPH在有机溶剂中是一种稳定的自由基,其在 517 nm附近有强吸收 (呈深紫色).当自由基清除剂存在时,DPPH的孤对电子被配对,其 517 nm吸收消失或减弱,通过测定吸收减弱的程度,可评价自由基清除剂的活性[13].图 4为芦丁及其包合物与常用的食品抗氧化剂 BHT清除DPPH自由基的能力对比.从图 4可以发现,虽然芦丁形成包合物后其清除 DPPH自由基的能力降低,但仍然展现出较强的 DPPH自由基清除能力.
2.4 还原力
食用抗氧化剂抗氧化的测定主要基于不同抗氧化防御体系机理,即活性氧和羟自由基的减少、脂质过氧化的抑制、金属离子的螯合.在大多数情况下,抗氧化作用与氧化链式反应的阶段无关,大多数非酶抗氧化作用 (自由基的清除、脂质过氧化的抑制等)受氧化还原反应的调节[14],因此本研究考察了芦丁及其包合物对铁离子的还原力(700 nm的吸光度越大表明还原力越强).随着样品浓度的上升,芦丁、包合物和 BHT在 700 nm处的吸光度呈线性上升 (r2分别为 0.999、0.995和0.998 7),表明三者均具有较强的还原力 (图 5),但包合物的还原力低于芦丁和BHT.
2.5 Ranci mat法
Rancimat法的基本原理是基于向一定温度的油样中通入一定流量空气,使油样加速氧化,将氧化产生的挥发性小分子 (如醛、酮、酸等)导入装有蒸馏水的瓶中,记录瓶中水的电导率变化情况,并求出诱导时间.诱导时间越长,表明油样抗氧化稳定性越好[15].在图 6中可以看出空白、包合物、芦丁及 BHT的诱导时间分别为:0.84、0.92、1.43、3.81 h.包合物和芦丁的保护系数分别为1.10和 1.70,芦丁经包合后其抗油脂氧化的能力下降.
3 结论
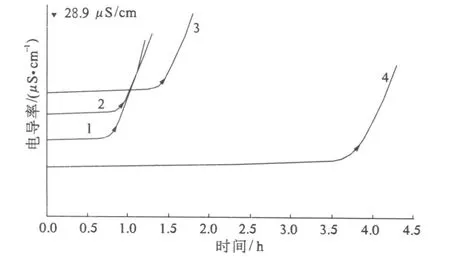
图6 Rancimat试验中空白 (1)、包合物 (2)、芦丁 (3)、BHT(4)的抗氧化活性
芦丁作为食品原料,特别是作为功能性原料在保健食品中具有广阔的应用前景.紫外、红外、X-射线衍射分析表明,通过羟丙基 -β-环糊精包埋后,芦丁的物相发生了重大改变,由于羟丙基-β-环糊精的稀释作用,包合物的抗氧化能力低于芦丁.但芦丁的溶解度和热稳定性却因包合而有显著提高 (另文报道),这将拓宽其在食品工业中的应用范围.
[1] 胡杰,邓宇.芦丁提取工艺的综述[J].中国食品添加剂,2006(5):94-99.
[2] Kreft I,Fabjan N,Yasumoto K.Rutin content in buckwheat(Fagopyrum esculentum Moench)food materials and products[J].Food Chemistry,2006,98(3):508-512.
[3] 牛小花,陈洪源,曹晓钢,等.芦丁的研究新进展[J].天然产物研究与开发,2008,20:156-159.
[4] Yuan C,Jin Z,Li X.Evaluation of complex forming ability hydroxypropyl-β-cyclodextrins[J]. Food Chemistry,2008,108(1):50-55.
[5] Yuan C,Jin Z,Xu X,et al.Preparation and stability of the inclusion complex of astaxanthin with hydroxypropyl-β-cyclodextrin[J].Food Chemistry,2008,109(2):264-268.
[6] Pfitzner I,Francz P I,Biesalski H K.Carotenoid:methyl-β-cyclodextrin formulations:an improved method for supplementation of cultured cells[J]. Bivchim Biophys Acta,2000,1474(2):163-168.
[7] Chen X,Chen R,Guo Z,et al.The preparation and stability of the inclusion complex ofastaxanthin withβ-cyclodextrin[J]. Food Chemistry,2007,101(4):1580-1584.
[8] Sun T,Ho C.Antioxidant activities of buckwheat extracts[J].Food Chemistry,2005,90(4):743-749.
[9] Joseph G S,Jayaprakasha G K,SelviA T,et al.Antiaflatoxigenic and antioxidant activities of Garcinia extracts[J]. International Journal of Food Microbiology, 2005, 101(2):153-160.
[10]Proestos C,Boziaris I S,Nychas G J E,et al.Analysis of flavonoids and phenolic acids in Greek aromatic plants: Investigation of their antioxidant capacity and antimicrobial activity[J].Food Chemistry,2006,95(4):664-671.
[11]Hung TM,Na M,Thuong P T.Antioxidant activity of caffeoyl quinic acid derivatives from the roots ofDipsacus asperWall[J].Journal ofEthnophar macology,2006, 108 (2):228-235.
[12]Hu C,Kitts D D.Studies on the antioxidant activity ofEchinacearoot extract[J].Journal ofAgricultural and Food Chemistry,2000,48(5):1466-1472.
[13]Srivastava A,Harish S R,Shivanandappa.Antioxidant activity of the roots of Decalepis hamiltonii(W ight&Arn)[J].LWT-Food Science and Technology,2006,39(10):224-233.
[14]徐清萍,陶文沂,敖宗华.食醋醇沉上清液的生物活性 [J].食品与生物技术学报,2005,24(4):76-80.
[15]Liu B,Du J,Zeng J,et al.Characterization and antioxidant activity of dihydromyricetinlecithin complex[J]. European Food Research and Technology,2009,230 (2):325-331.
CHARACTER IZATI ON AND ANTI OXIDANTACTI V ITY OF RUTINHYDROXYPROPYL-β-CYCLODEXTR IN INCLUSI ON COMPLEX
SU Cai-juan1,WANG Jin-shui1,L IU Ben-guo2,CHEN Yong-sheng2,HU Li-zhi2
(1.School of Food Science and Technology,Henan University of Technology,Zhengzhou450052,China;2.School of Food Science,Henan Institute of Science and Technology,Xinxiang453003,China)
In the paper,we prepared a rutin-hydroxypropyl-β-cyclodextrin(HP-β-CD)inclusion complex by solution method to i mprove the water solubility of rutin.We also carried out the structure characterization of the inclusion complex by UV spectrometry(UV),infrared spectrometry(I R),X-ray diffractometry(XRD)and so on.The results showed that the inclusion complex had high antioxidant activity in the DPPH radical scavenging assay,the deter mination of reducing power and the Rancimat test.
rutin;hydroxypropyl-β-cyclodextrin;inclusion complex;antioxidant
TS201.2
B
1673-2383(2011)01-0053-05
2010-10-27
国家“十五”科技攻关项目 (2001BA501A04);河南省高校青年骨干教师基金资助项目
苏彩娟 (1985-),女,河南商丘人,硕士研究生,研究方向为食品生物技术.
*通信作者
