二氧化硅负载镍铝水滑石的制备及其催化合成安息香乙醚的研究
2011-09-29王国强谢鲜梅高成云程淑艳
王国强 谢鲜梅 高成云 吴 旭 安 霞 程淑艳
(太原理工大学化学化工学院,太原 030024)
二氧化硅负载镍铝水滑石的制备及其催化合成安息香乙醚的研究
王国强 谢鲜梅*高成云 吴 旭 安 霞 程淑艳
(太原理工大学化学化工学院,太原 030024)
采用共沉淀法制备了以二氧化硅为载体,表面包覆镍铝水滑石的NiAl-LDHs/SiO2复合物,借助XRD、IR及N2吸附-脱附等手段对合成物进行了表征,并将其应用于苯甲醛与乙醇反应生成安息香乙醚反应中进行活性评价。结果表明,复合物中镍铝水滑石与二氧化硅以稳定的Si-O-Al和Si-O-Ni键结合,镍铝水滑石均匀分布于二氧化硅表面,且生成的复合物比表面积较大;当镍铝水滑石负载量为20%时,在反应温度为70℃、反应时间为60 min条件下,NiAl-LDHs/SiO2催化苯甲醛与乙醇反应的苯甲醛转化率为61.8%,安息香乙醚选择性接近100%,其催化效果明显优于单一的NiAl-LDHs。
镍铝水滑石;二氧化硅;安息香乙醚合成;苯甲醛
0 引 言
安息香醚类化合物作为一类光敏剂,在感光树脂体系中有广泛的用途。随着新技术的开发和应用,安息香醚类化合物又在涂料、塑料、印刷和电子等新领域中展现出良好的应用前景。早期安息香醚类化合物是由安息香与相应的醇在干燥氯化氢催化下反应制备,该过程要求无水醇的量很大,反应时间长且收率不稳定[1]。20世纪70年代以来,国外专利文献报道以三氯化磷、三氯化铝、亚硫酰氯、三氯氧磷、光气、氯甲酸三氯甲酯等为催化剂并以乙酸叔丁酯为醚化剂的安息香醚类化合物合成方法,但仍无法解决原料价格昂贵且合成反应污染环境的弊端[2]。此后,有研究者[3]利用氰盐催化,选用相对低廉的苯甲醛为原料合成安息香醚类化合物,但氰盐有毒,不符合环境友好型发展的要求。
水滑石和类水滑石主体一般由两种金属的氢氧化物构成,因此又称为层状双羟基复合金属氢氧化物(layered double hydroxide简写为LDH)[4]。其层板上羟基八面体中的阳离子和层间阴离子的可调变性,在很大程度上调变其酸碱性,从而影响其催化性能。本课题研究小组曾采用共沉淀法制备出NiAl-LDHs,并将其应用于苯甲醛与乙醇反应生成安息香乙醚反应中,得到了较好的结果,但苯甲醛转化率较低,仅为43.7%左右[5]。经分析其原因在于催化剂合成过程中易团聚结块,且制得的催化剂比表面积较小,活性组分利用率较低,因此,在催化反应中利用率受到限制。一般通过负载可以有效提高活性组分的分散性,增加比表面积。非晶态的SiO2以其较大的比表面和稳定的结构,及其表面大量羟基的存在可以与金属离子形成稳定的M-O-Si(M代表金属阳离子)的共价结构而被广泛作为载体。但水滑石负载于SiO2的研究报道甚少,本研究采用共沉淀法合成了NiAl-LDHs/SiO2复合物,提高催化剂的比表面积和活性组分的分散性,在催化苯甲醛与乙醇反应中苯甲醛转化率明显提高。
1 实验部分
1.1 复合物的制备
按美国专利US5637636报道的方法合成大孔容的二氧化硅[6],并将其加入到 Ni(NO3)2、Al(NO3)3无水乙醇溶液中,在不断的剧烈搅拌下,浸渍吸附一定时间后,逐滴加入质量分数为1%的NH3·H2O溶液至所需 pH 值(6.5~7.0),滴加完毕继续搅拌 0.5 h,得到的浆液置于不锈钢反应釜中,密封后在110℃水热处理6 h,然后抽滤、洗涤,于80℃下烘干,研磨待用。
1.2 镍铝水滑石的制备
按一定比例将 1.0 mol·L-1Ni(NO3)2、0.5 mol·L-1Al(NO3)3溶液混合,在不断的强烈搅拌下,以1.0 mL·min-1的速度滴加NaOH和Na2CO3溶液,至pH值为 5.0~5.5,滴加完毕继续搅拌 0.5 h 得到的沉淀与母液置于不锈钢反应釜中,密封后在110℃水热处理6 h,然后抽滤、洗涤,于80℃下烘干,研磨待用。
1.3 表 征
XRD分析:日本Rigaku公司D/Max2500型X-射线衍射仪,Cu 靶 Kα 射线 (波长 λ=0.15418 nm),石墨单色器,靶电压40 kV,靶电流100 mA,扫描速率 8°·min-1,扫描范围 5°~65°,闪烁计数器记录强度。FTIR分析:日本岛津傅立叶红外光谱分析仪FTIR 8400,波数测定范围 400~4500 cm-1。 比表面积平均孔径及孔容测定:美国Micromeritics ASAP 2020型自动吸附仪,样品在测定前程序升温至373 K抽真空预处理5 h,吸附剂为高纯氮。SEM分析:使用日本JSM-6700F扫描电子显微镜对催化剂形貌进行观察。GC分析:北京北分瑞利SP-2100气相色谱,分析条件为:毛细管色谱柱OV-101(0.2 mm×0.25 μm×50 m),载气为 N2,柱流量 1.0 mL·min-1,补充气 N2301.0 mL·min-1;采用程序升温 50~210 ℃,50℃停留5 min,210℃停留5 min,升温速率5℃·min-1;汽化室 240 ℃,FID 270 ℃,进样量 0.2 μL,分流比为 1∶100。
1.4 安息香乙醚的合成
催化剂的活性评价在自制的微型反应装置上进行。将装有回流装置的三口烧瓶固定在集热式恒温磁力搅拌器上,加入一定量的苯甲醛、乙醇及催化剂(预先在80℃下用N2气吹扫2 h),固定反应温度70℃,常压下反应,定时取样进行GC分析,以外标法进行定量。
2 结果与讨论
2.1 结构分析
通过研究可知,水滑石的成核过程中涉及到均相成核和异相成核的竞争,按照晶体学理论,均相成核的自由能大于异相成核的自由能,所以一般情况优先异相成核。在本研究条件下控制成核过程中沉淀剂加入速度并强烈搅拌,若条件控制得当,水滑石会在二氧化硅表面异相成核,并沿其表面生长,形成均匀的包覆层。研究中详细考察了金属离子浓度、载体用量、氨水浓度、滴加速度、反应温度等因素对合成物的影响,得到制备复合物的适宜条件为 Ni2+浓度为 0.1 mol·L-1,Al3+浓度为 0.05 mol·L-1,负载量为20%,氨水浓度为质量分数1%,反应温度在常温条件下,pH 值为 6.5~7.0。图 1 中(c)为在适宜条件下合成复合物的XRD图。图1中(a)为载体二氧化硅和(b)为NiAl-LDHs的XRD衍射图。由图可见,复合物NiAl-LDHs/SiO2的XRD图与NiAl-LDHs的图的特征峰位置基本相同,而且峰形和强度也基本一致,这一点证明在载体表面形成了晶型良好的NiAl-LDHs。张泽江等[7]认为表面包覆SiO2的LDHs会出现较宽的无定形颗粒的吸收峰,而本实验所合成的复合物却无此吸收峰,这说明了采用本实验方法可在二氧化硅表面形成晶型完整的NiAl-LDHs。
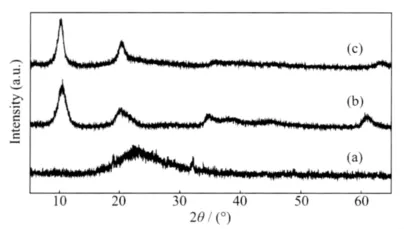
图1 二氧化硅(a)、NiAl-LDHs(b)和复合物NiAl-LDHs/SiO2(c)的 XRD 图Fig.1 XRD patterns for SiO2(a),NiAl-LDHs(b)and composite NiAl-LDHs/SiO2(c)
2.2 FTIR分析
图2是SiO2浸渍金属离子前后样品的IR图,从图2(a)可以看出在1 350 cm-1出现Si-OH键的伸缩振动峰953 cm-1出现Si-OH的弯曲振动峰,由(b)可知,吸附金属离子之后这俩尖峰消失,表明金属离子与Si-OH结合,连接到二氧化硅表面形成新的Si-O-Al,Si-O-Ni键,在(1 020~1 224)cm-1出现的吸收峰较为宽大。图3是(a)NiAl-LDHs和(b)复合物的IR图,从图3中可知,在400~800 cm-1a和b存在相同的强吸收峰,这是镍铝水滑石中的Ni-O,Al-O键的特征吸收峰,说明在负载过程中形成了水滑石包覆层。比较图3中a、b可知,在载体SiO2中存在460 cm-1处有Si-O-Si的摇摆振动峰和1 120 cm-1处Si-O-Si的伸缩振动峰在复合物中同时存在,说明在没有破坏载体结构的前提下生成了类水滑石包覆层。
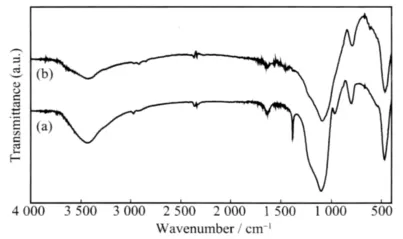
图2 载体二氧化硅(a)和浸渍金属离子后二氧化硅(b)的IR谱图Fig.2 FTIR spectra for SiO2(a)the SiO2after stirring(b)
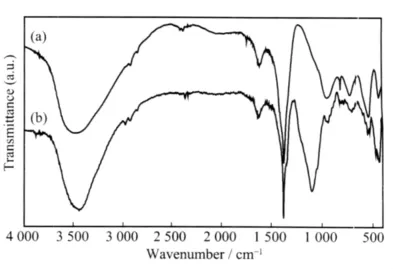
图 3 NiAl-LDHs(a)和复合物 NiAl-LDHs/SiO2(b)的IR图Fig.3 FTIR spectra for NiAl-LDHs(a)and the composite NiAl-LDHs/SiO2(b)
2.3 复合物的BET表征及孔径分析
将 SiO2、NiAl-LDHs 和 NiAl-LDHs/SiO2复 合 物进行BET测试比较,结果如表1所示:

表1 SiO2、NiAl-LDHs和复合物的比表面积及孔结构性质Table 1 BET specific surface area and pore structure of SiO2,NiAl-LDHs and composite
表 1 是 SiO2、NiAl-LDHs 和 NiAl-LDHs/SiO2复合物的比表面积及孔结构性质。从表1可知,用BET法测得NiAl-LDHs/SiO2的比表面积为375 m2·g-1,大于载体的比表面积 295 m2·g-1,也远大于NiAl-LDHs的比表面积14 m2·g-1。在相对压力p/p0=0.99 时,测得复合物 NiAl-LDHs/SiO2的孔容为 1.36 cm3·g-1, 大于载体 SiO2孔容 1.13 cm3·g-1和 NiAl-LDHs的孔容 0.045 cm3·g-1。复合物比表面积和孔容增加的原因可能是样品表面粗糙度增加,以及新生成的水滑石因具有层状结构而呈现较发达的二维孔系。图4是样品NiAl-LDHs/SiO2复合物的吸附等温线。 由图 4 可以看出,在 p/p0=0.8~1.0 之间出现了H3型滞后环对应于契形孔或由平板状颗粒堆积形成的孔。图5是SiO2和NiAl-LDHs/SiO2的孔径分布,用BJH法分析两者的孔径大小,发现载体SiO2孔道在2~42 nm的比较宽的范围内分布,而NiAl-LDHs/SiO2的孔径分布明显变窄,孔道基本分布在2~32 nm这个范围内。这是由于在孔径尺寸较大的内孔表面上形成了LDHs微晶而使其孔径减小。
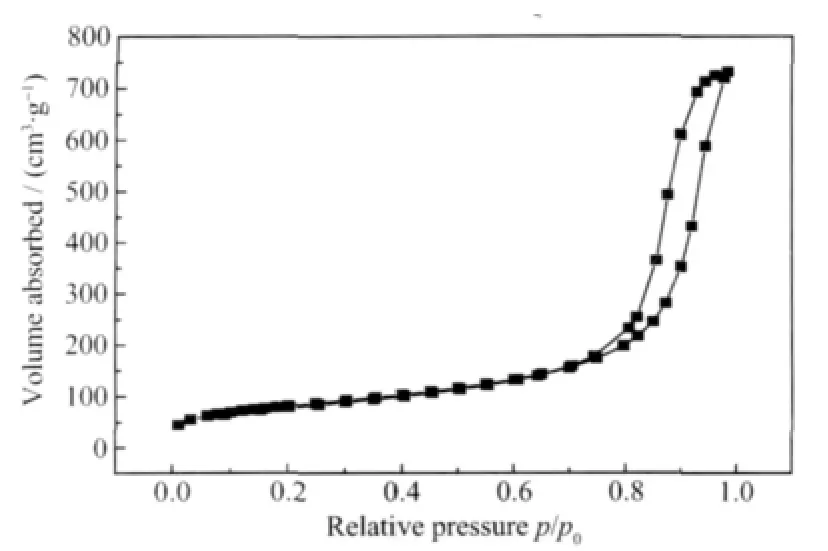
图4 NiAl-LDHs/SiO2的N2吸附-脱附曲线Fig.4 N2adsorption-desorption isotherm of NiAl-LDHs/SiO2
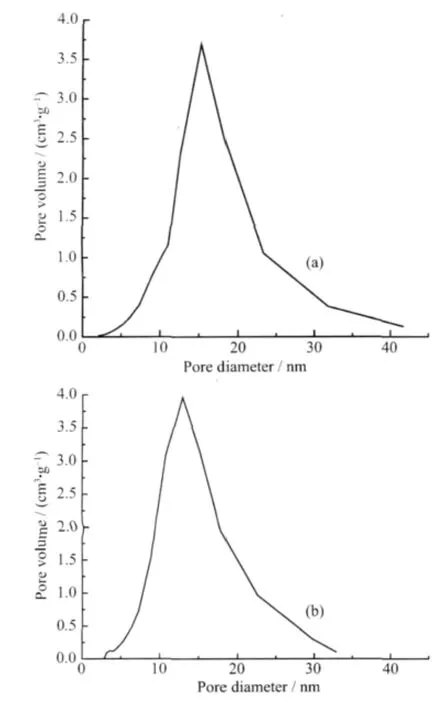
图5 SiO2(a)和NiAl-LDHs/SiO2(b)的孔径分布Fig.5 Pore diameter distribution of SiO2(a)and NiAl-LDHs/SiO2(b)
2.4 SEM分析
图6的a和b分别是载体SiO2和NiAl-LDHs/SiO2复合物的SEM照片。从图6a中可以看到,二氧化硅的表面颗粒比较光滑,颗粒尺寸约为35~55 nm,且小尺寸颗粒较多,图b是包覆NiAl-LDHs的复合物的SEM照片,可以明显看出颗粒表面仍然比较光滑,颗粒的平均尺寸变大,平均尺寸约为45~65 nm。对比包覆产物和载体SiO2,可知颗粒平均厚了10 nm。由图6可知包覆水滑石前后颗粒形貌没有明显变化,但包覆后颗粒大小有所增大,可知负载过程并未破坏SiO2的结构,NiAl-HTLcs在SiO2表面形成了均匀的包覆层。

图6 SiO2(a)和 NiAl-LDHs/SiO2复合物(b)的 SEM 照片Fig.6 SEM images of SiO2(a)and composite NiAl-LDHs/SiO2(b)
2.5 包覆机理
根据SiO2表面羟基与金属离子能形成配位键的机理,在SiO2浸渍于金属盐溶液的过程中,Ni2+离子和Al3+离子首先与二氧化硅表面的羟基形成配位键锚定在SiO2表面,它们之间形成了Si-O-Al和Si-O-Ni键,接着加入的氨水作为沉淀剂,在一定pH值下与锚定在SiO2表面的Ni2+离子和Al3+离子以基点生成连续的NiAl-LDHs膜,二氧化硅表面可能会发生以下反应[8-12](以Mn+表示Ni2+或Al3+):


式中k1和k2分别是反应(1)和(2)的平衡常数。从式(5)可知SiO2表面锚定的Mn+离子浓度取决于SiO2表面羟基浓度及溶液中Mn+离子浓度和浸渍液体的pH值;当采用硝酸镍、硝酸铝混合溶液浸渍二氧化硅载体时,载体表面的羟基浓度越大,Surface-SiOM(n-1)+浓度也越大,越多的金属离子会锚定于载体表面,不随干燥、焙烧过程的进行而变化,镍硅之间产生了强的作用力。当溶液中缓慢加入氨水溶液,使溶液中的H+浓度减小,也使方程式(1)、(2)反应平衡向右进行,生成更多的Surface-SiOM(n-1)+,同时随着碱液的不断加入,锚定在SiO2表面的Ni2+、Al3+与OH-形成六配位的八面体网状结构,即在SiO2表面形成了NiAl-LDHs的包覆层,复合物制备完成。其制备过程结构示意图为图7。
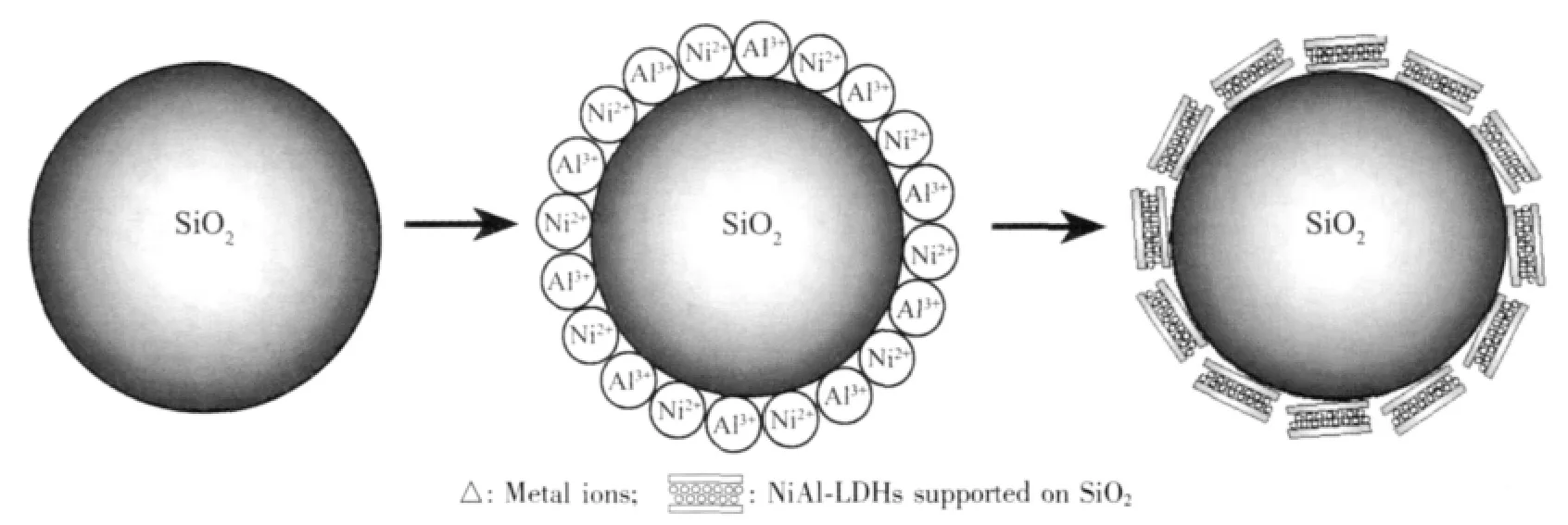
图7 合成NiAl-LDHs/SiO2的过程示意图Fig.7 Schematics of NiAl-LDHs/SiO2synthesis
2.6 负载量对催化结果的影响
NiAl-LDHs负载量通过在相同的溶液中加入不同量的二氧化硅载体来控制。将不同包覆量的催化剂应用于催化苯甲醛与乙醇生成安息香乙醚的反应,结果见表2。结果显示:随着负载量的增加,苯甲醛的转化率出现先增加而后降低的现象。当负载NiAl-LDHs的质量分数为20%时,此时复合物比表面积达最大值375 m2·g-1,苯甲醛的转化率达到61.8%。这可能是NiAl-LDHs在载体表面分布比较均匀,活性组分分散度较好,活性位也最大化地暴露在表面;而负载量超过30%时,复合物的比表面降低到265 m2·g-1,主要原因是负载量过高时,NiAl-LDHs在载体表面出现团聚,使活性组分的分散度降低,导致催化剂活性降低。
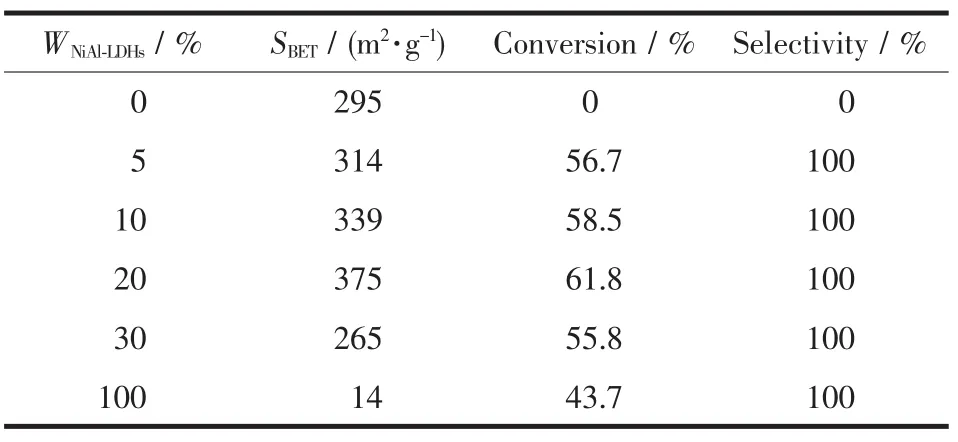
表2 NiAl-LDHs负载量对催化结果的影响Table 2 Influence of NiAl-LDHs loading amount on catalysis
2.7 不同催化剂对反应的影响
图8是载体二氧化硅(a)、NiAl-LDHs(b)和负载量分别为 30%(c)、10%(d)、20%(e)的复合物对苯甲醛转化率的影响。从图8可以看出,在相同的反应条件下,将不同催化剂应用于催化苯甲醛与乙醇生成安息香乙醚的反应,二氧化硅载体对苯甲醛的转化率近似为0%,对反应近乎没有影响,NiAl-LDHs对苯甲醛的转化率为43.7%。NiAl-LDHs负载到二氧化硅上形成的复合物在负载量为10%、20%、30%对苯甲醛的转化率分别为 58.5%、61.8%、55.8%,可能是由于NiAl-HTLc分散于具有较大比表面积的二氧化硅,使得活性组分更多的暴露在表面上,提高了苯甲醛的转化率。这也说明复合物的形成在一定程度上提高了活性组分的利用率。
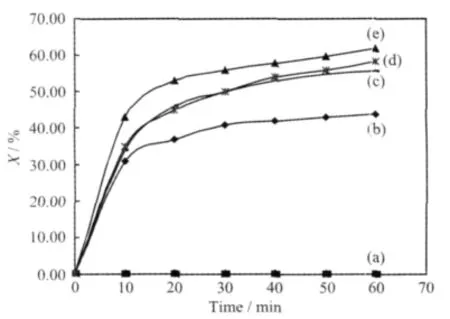
图8 不同催化剂对苯甲醛的转化率的影响Fig.8 Effect of the different catalysts on the conversion of benzaldehyde with reaction time
3 结 论
(1)采用共沉淀法在SiO2表面包覆生成了NiAl-LDHs,制备了NiAl-LDHs/SiO2复合物,通过分析包覆机理为:SiO2表面的羟基先与镍铝阳离子反应在二氧化硅表面形成Si-O-Al和Si-O-Ni键,而后以这些金属离子为锚点,通过控制加入的碱量和速度,并控制合成体系的 pH=6.5~7.0,可制备单一物相的NiAl-LDHs/SiO2复合物。
(2)苯甲醛与乙醇反应生成安息香乙醚反应中,当NiAl-LDHs负载质量分数为20%时,复合物NiAl-LDHs/SiO2表现出较高的催化活性,苯甲醛的转化率达61.8%,安息香乙醚的选择性接近100%,相同条件下,明显优于单一NiAl-LDHs的催化效果。
[1]LI Zhong-Jie(李仲杰),LI Si-Ji(李四季).Chinese J.Northwest Uni.(Xibei Daxue Xuebao),1980,4:52-57
[2]NAN Zhi-Xiang(南志祥),LI Zhong-Jie(李仲杰).Chem.Reag.(Huaxue Shiji),1992,14(2):117-118
[3]LI Xun(李勋).Fine and Specialty Chem.(Jingxi Yu Zhuanyong Huaxuepin),2001,6:21
[4]LUO Qing-Song(罗青松),LI Lei(李蕾),DUAN Xue(段雪),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2001,17(6):835-842
[5]Xie X M,Yan K,Li J P,et al.Catal.Commun.,2008,9(6):1128-1131
[6]Simon C,Ianp M.US Patent,5637636.1997-06-10
[7]ZHANG Ze-Jiang(张泽江),MEI Xiu-Juan(梅秀娟),XU Cheng-Hua(徐 成 华),et al.Science in China B(Zhongguo Kexue B Ji:Huaxue),2004,34(6):454-459
[8]SHI Li-Hong(史利红),LI De-Bao(李德宝),HOU Bo(侯博),et al.Chin.J.Catal.(Cuihua Xuebao),2007,28(11):999-1002
[9]Zhang Y,Hanayama K,Tsubaki N.Catal.Commun.,2006,7(5):251-254
[10]Duan X L,Yuan D R,Sun Z H,et al.J.Cryst.Growth,2003,252(1/2/3):4-8
[11]Li G S,Li L P,Smith R L,et al.J.Mol.Sruct.,2001,560(123):87-93
[12]MAO Xian-Bing(毛纤冰),LI Dian-Qing(李殿卿),ZHANG Fa-Zhi(张法智),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2004,20(5):596-601
[13]You K J,Chang C T,Liaw B J,et al.Appl.Catal.A:Gen.,2009,361(1/2):65-71
[14]Vijaikumar S,Dhakshinamoorthy A,Pitchumani K.Appl.Catal.A:Gen.,2008,340(1):25-32
[15]Kishore D,Rodrigues A E.Appl.Catal.A:Gen.,2008,345(1):104-111
NiAl-LDHs/SiO2Composite:Preparation and Application in Benzoin Ethyl Ether Synthesis
WANG Guo-QiangXIE Xian-Mei*GAO Cheng-Yun WU Xu AN XiaCHENG Shu-Yan
(College of Chemistry and Chemical Engineering,Taiyuan University of Technology,Taiyuan 030024,China)
A surface-covered NiAl-LDHs composite NiAl-LDHs/SiO2was prepared by coprecipitation method using silicon dioxide as supporter.The composite was characterized using X-ray diffraction (XRD),Fourier transform infrared(FTIR)and N2-adsorption/desorption measurement,and its catalytic performance was evaluated in terms of benzoin ethyl ether synthesis by reaction between benzaldehyde and methanol.The results show that the NiAl-LDHs and SiO2are combined each other through the stable chemical bond of Si-O-Al and Si-O-Ni in the composite.NiAl-LDHs is distributed uniformly on the surface of SiO2,and the composite has high specific surface area.Additionally,the synthesis of benzoin ethyl ether was performed with NiAl-LDHs/SiO2of 20%LDHs loadings as the catalyst at 70℃for 60 min.The results show that conversion rate of benzaldehyde could reach 61.8%with the selectivity of benzoin ethyl ether nearly 100%and that NiAl-LDHs/SiO2has higher catalytic activity than single NiAl-LDHs.
NiAl-LDHs;silicon dioxide;the synthesis of benzoin ethyl ether;benzaldehyde
O643.3;TQ426.6
:A
:1001-4861(2011)05-0917-06
2010-11-15。收修改稿日期:2010-12-30。
国家自然科学基金(No.50872086);山西省自然科学基金(No.2008011018)资助项目。
*通讯联系人。 E-mail:xxmsxty@sina.com
