卤化法制备高纯钛过程中杂质Cr的行为研究
2011-09-27李武斌
韩 涛,曾 英,李武斌,王 舟
(贵州大学材料与冶金学院,贵州 贵阳 550003)
卤化法制备高纯钛过程中杂质Cr的行为研究
韩 涛,曾 英,李武斌,王 舟
(贵州大学材料与冶金学院,贵州 贵阳 550003)
对卤化法制备高纯钛过程中杂质Cr的行为进行了热力学分析。实验条件下,在卤化源区(823~1 023 K),杂质Cr能与卤化剂反应,生成CrI2与CrI3;在沉积区(1 373~1 473 K),CrI2不能分解,CrI3能够分解,杂质Cr主要来自于CrI3的分解携入。
高纯钛;卤化法;杂质;Cr;热力学
金属钛具有优良的使用性能、抗腐蚀性以及特殊的材料强度等优越性,广泛用于航空、航天、化工、石油、冶金、轻工、电力、海水淡化、舰艇和日常生活器具等领域,被誉为现代金属。近年来,随着航空航天、电子信息等高科技产业的快速发展,高纯钛的用量越来越多,而集成电路快速的高度集成,对作为溅射为目标用于硅半导体集成电路中的高纯钛,在纯度上有了更高的要求[1]。
高纯钛中杂质的存在,会引起诸多问题,如超大规模集成电路的控制电极、扩散阻挡层及配线材料中的重金属杂质(Fe、Ni、Cu、Cr等)、碱金属杂质(Na、K等)以及放射性元素(U、Th等)会分别导致产品漏电系数增大、界面特性下降、软件程序失误等一系列问题[2~3],因此提纯金属钛以制备高纯钛,并且尽力提高高纯钛的纯度具有重要的意义。
本文对卤化法制备的高纯钛样品进行断面扫描电镜分析,通过辉光放电质谱仪(GDMS)进行痕量和超痕量杂质元素检测,检测出重金属杂质元素Cr超量,以此对Cr在卤化法制备高纯钛过程中的行为进行热力学分析。
1 实验
1.1 实验原理
实验采用卤化法制取高纯钛,其基本原理是利用钛在低温和高温下与卤化剂的可逆反应分离杂质,并以化学气相沉积的方式在基底材料上附着而得到高纯钛。实验中,以粗钛为原料,碘作为主卤化剂,采用特殊的工艺设备,首先使粗钛与卤素在卤化源区反应得到气态钛卤盐,然后控制反应条件,使得气态钛卤盐在适宜条件下发生热裂解,然后在高温基底上沉积而得到高纯钛[4~6]。
1.2 实验原料及设备
实验使用的原料有海绵钛(Ti>99.0%)、工业钛丝(直径5 mm,Cr>0.001%)、自制卤化剂(主要成分为碘)。所采用的工艺设备主要由炉体(能保证炉体内有一低温区和一高温区)、平台、抽真空系统、控制系统等组成。
2 实验样品分析
对实验所制得的高纯钛进行断面扫描电镜分析,如图1。

图1 样品断面电镜扫描图
从图1a中可看出,高纯钛的晶体形状为柱状,这种形状是纯金属结晶中的常见晶形。图1b则为图1a的晶间局部放大,可以看到晶体间的缝隙,此缝隙也是晶间杂质的存留区域。
经过分析,图1b晶间缝隙中杂质Cr的含量较高,为120×10-6,其右侧晶柱钛的纯度完全达到4N5级高纯钛3.00×10-6的标准。
3 Cr的反应热力学分析及结果讨论
通过热力学分析,找到杂质Cr的携入途径,并从温度上对杂质Cr的进入加以控制[7]。
3.1 分析方法[8]
反应物及产物的标准摩尔定压热容为:

范特霍夫方程为:

式(a)和式(b)经过一系列的数学变换可以得到任意温度下与T的关系,即:

式中:△H0、I为积分常数,△a、△b、△c可由式(a)中的a、b、c查表后求出。
由此可以计算出各杂质元素的卤化与裂解反应在实验操作温度下的值,从而判断反应在设定温度下是否可以发生。
3.2 Cr的碘化物合成热力学分析及结果讨论
实验碘化源区温度控制在550~750℃之间。
Cr的碘化物合成反应为:
反应相关的热力学数据见表1[9]。

表1 相关的热力学数据
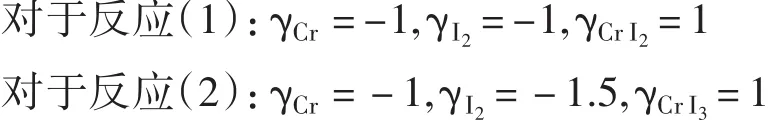

利用以上两式,对于反应(1)可得:

对于反应(2)可得:
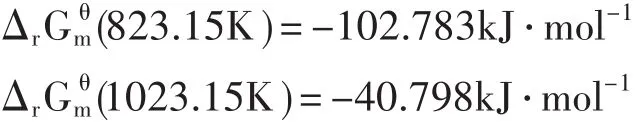
从计算结果中可以看出,在碘化源区温度(823.15~1023.15 K)下,CrI2与CrI3都能够顺利生成。
3.3 Cr的碘化物分解热力学分析及结果讨论
Cr的碘化物分解反应为:

利用表1的热力学数据,对于反应(3)可得:

对于反应(4)可得:

通过上面的数据可以求出反应(3)、(4)的分解温度,反应(3)为T>1915K,反应(4)为T>1390K。
通过上面的分析可简单的确定反应(3)、(4)的分解温度,可知CrI2的分解温度较高,CrI3的分解温度较为适中。为进一步确认CrI2与CrI3的分解温度,通过lgKp与1/T的关系来进行分析。
因为Cr做为高纯钛中的一种杂质元素,因此对于CrI2、CrI3来说,并不希望它在纯钛沉积温度区分解沉积出Cr,所以就要求反应(3)、(4)的lgKp有较大的负值[10]。lgKp与有如下关系:
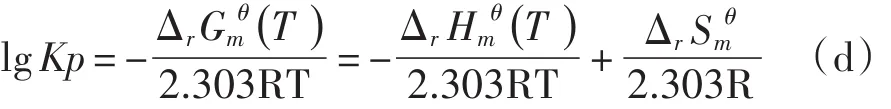
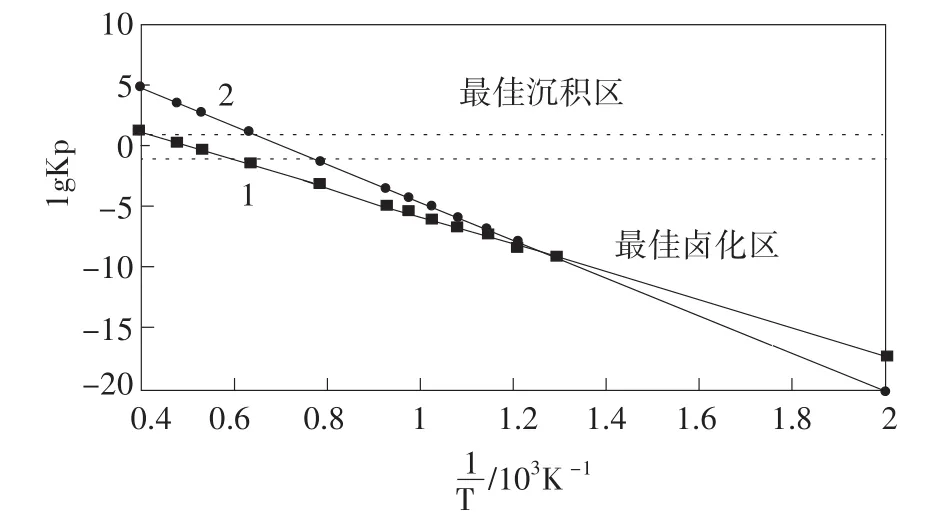
图2 lgKp与1/T的关系曲线
利用表1数据以及上式,可得到反应(3)、(4)的lgKp与1/T关系图,见图2。
图2中曲线1代表反应(3),曲线2代表反应(4)。根据转换百分数与平衡常数的关系可知,当lgKp=1时,反应的转换效率有90%以上,所以取图2中的上虚线为lgKp=1,下虚线为lgKp=-1。由于lg⁃Kp正值较大,则反应正向进行,lgKp负值较大,则反应不会正向进行。因此取lgKp≥1以上的区域为最佳沉积区,lgKp≤-1的区域为最佳卤化区。由图2中1、2曲线可以看出,两条曲线都通过最佳卤化区,因此在卤化源区温度范围内CrI2、CrI3都能够生成,这与前面的分析一致。由图2也可以看出,两条曲线都通过最佳沉积区,但曲线2的分解温度明显低于曲线1的分解温度,这与之前的分析也一致。由图2可得出CrI3的分解温度,结合之前的分析,可得出CrI3的沉积温度在1 400-1 600 K左右,这也是生产过程中需要避免的温度区间。而对于CrI2,由之前的分析以及图2都可以看出CrI2的沉积温度都较高。
4 结论
(1)在实验卤化源区温度下,Cr能与卤化剂反应,生成 CrI2与CrI3。
(2)从CrI2与CrI3的分解温度看来,在实验沉积区温度范围内,由于CrI2分解温度较高,CrI3的分解温度合适,因此,杂质Cr主要来自于CrI3的分解携入。
(3)制备过程中沉积区温度应尽力避免在1400~1 600 K,以抑制杂质CrI3分解从而导致的Cr杂质携入。所以,严格控制操作区间的反应温度,对抑制杂质元素的携入有重要的影响。
[1]刘正红,陈志强.高纯钛的应用及其生产方法[J].稀有金属快报,2008,27(2):4.
[2]吴全兴.高纯钛的制取[J].加工技术,1996,(5):14-16.
[3]李 哲,郭让民.高纯钛的制备及发展方向[J].钛工业进展,1997,(3):23-24.
[4]李有观.用碘化物精炼高纯钛[J].世界有色金属,2003,(12):25-27.
[5]新藤裕一朗.张唯敏,译.高纯度钛的制造技术与其应用[J].国外金属加工,2000,(3):25-28.
[6]李惠萍.高纯度钛[J].上海钢研,2003,(1):60-61.
[7]郭让民,李 哲.碘化钛的电子束熔炼提纯效果分析[J].稀有金属材料与工程,1996,25(6):44-45.
[8]杜清枝,杨继舜.物理化学[M].重庆:重庆大学出版社,2005.25-82.
[9]梁英教,车荫昌.无机物热力学数据手册[M].辽宁:东北大学出版社,1993.
[10]王福贞,马文存.气相沉积应用技术[M].北京:机械工业出版社,2007.7-9.
Abstract:Thermodynamic analysis of impurity of Cr in the process of high purity titanium preparation by halogen process was made.Under the experiment conditions,impurity of Cr can react with halogen agent,to generate CrI2and CrI3in the halide source area(823~1023K).In the deposition area(1373~1473K),CrI3can decompose,but CrI2can not decompose.Impurity of Cr is mainly come from the process of thermal decomposition of CrI3.
Key words:high purity titanium;halogen process;impurity;Cr;thermodynamics
Study on impurity behavior of Cr in the process of high purity titanium preparation by halogen process
HAN Tao,ZENG Ying,LI Wu-bin,WANG Zhou
TF823
A
1672-6103(2011)01-0073-03
韩 涛(1986—),男,贵州贵阳人,硕士研究生,研究方向:有色金属冶金。
2010-06-04
