白杨素衍生物的合成及生理活性研究进展
2011-09-24王秋亚王烨娟高锦红
王秋亚,王烨娟,高锦红
(渭南师范学院化学化工系,陕西渭南 714000)
白杨素衍生物的合成及生理活性研究进展
王秋亚,王烨娟,高锦红
(渭南师范学院化学化工系,陕西渭南 714000)
黄酮类化合物白杨素具有抗氧化、抗肿瘤、抗癌、抗病毒、抗高血压、抗糖尿病、抗菌、抗过敏等广泛的生理活性.近年来,许多国内外学者对其衍生物的合成及生理活性进行了研究,以期开发出活性更高、更具有临床应用价值的药物.本文着重对各类白杨素衍生物的合成及生理活性研究进展进行综述.
白杨素;白杨素衍生物;合成;生理活性;研究进展
Abstract:A review is provided of the research progress of synthesis and biological activity of chrysin.It is pointed out that chrysin as a kind of flavonoids has biological activities such as anti-oxidant,anti-tumor,anti-cancer,anti-virus,anti-hypertension,anti-diabetic,anti-bacterial,anti-allergy and so on.In recent years,many scholars at home and abroad focused on the synthesis and biological activities of its derivatives so as to develop more active drugs for clinic.
Keywords:chrysin;chrysin derivative;synthesis;biological activities;research progress

图1 白杨素的结构Fig.1 Structure of chrysin
白杨素(chrysin),又名白杨黄素,化学名为5,7-二羟基黄酮(结构见图1),来源于紫葳科植物木蝴蝶的种子、茎皮,松科植物山白松的心木,芒松的心木等,在蜂胶中含量较高.白杨素具有抗氧化、抗肿瘤、抗癌、抗病毒、抗高血压、抗糖尿病、抗菌、抗过敏等广泛药理生理活性[1],而且该类化合物在植物中分布广泛,毒性比较低,因此是新药开发研究中一个非常重要的资源.近年来许多国内外学者对白杨素衍生物的合成方法和生理活性进行了研究,以期开发出活性更高、更具有临床应用价值的药物.本文则对其衍生物的合成和生理活性进行了综述,以促进其进一步的研究和应用.
1 白杨素磺化物、硝化物的合成及生理活性
为改善白杨素的水溶性,史娟等人[2]在波兰的 Pusz等人研究的基础上,对白杨素进行了磺化,得到了5,7-二羟基黄酮-6-磺酸钠和5,7-二羟基黄酮-8-磺酸钠.由于这两种磺化物的溶解度和极性几乎相同,常用的柱层析及重结晶方法难以使其分离,史娟等人采用先络合后解聚方式对其进行了分离(图2).

图2 白杨素磺酸钠的合成与纯化Fig.2 Syntheses and isolation-purification of sodium chrysin sulfonates
此外,史娟和谭大金等人[2-3]以白杨素-6-磺酸根作为配体使其与 Zn(Ⅱ)、Cd(Ⅱ)、Ba(Ⅱ)、Cu(Ⅱ)、Ca(Ⅱ)作用得到5种白杨素-6-磺酸根的配位化合物:白杨素双锌配位化合物[Zn(C15H8O7S)(DMSO)]2·H2O、白杨素四核镉配位化合物[{Cd(C15H8O7S)(H2O)(DMSO)}3{Cd(C15H8O7S)(H2O)2}]·3DMSO·H2O、白杨素磺酸钡配位聚合物[Ba(C15H8O7S)2]n、白杨素磺酸铜配位化合物[Cu(C15H8O7S)(3H2O)]、白杨素磺酸四核钙配位化合物[Ca(C15H8O7S)(H2O)(DMSO)]3Ca(C15H8O7S)(DMSO)2.
众所周知,药物分子与DNA的作用方式,对于从分子水平上了解抗癌药物的抗癌机理、设计开发新型抗癌药物以及在活体中筛选药物具有重要价值.为此,谭大金等人[3]采用紫外、荧光和黏度手段研究了NaL、Zn2L2及Ca4L4与小牛胸腺DNA的作用.结果发现,白杨素-6-磺酸根的Zn(Ⅱ)、Ca(Ⅱ)配合物及其钠盐与DNA的作用有所不同,可能是金属离子Zn(Ⅱ)、Ca(Ⅱ)与白杨素-6-磺酸根形成配合物后增加了分子的平面性,影响了药物分子与DNA之间的相互作用.
徐阳炎等[4]以间苯三酚为原料合成了8-硝基白杨素(图3),并通过实验研究发现低、中、高剂量8-硝基白杨素均能明显抑制肿瘤的生长和肿瘤转移结节数.

图3 8-硝基白杨素的合成Fig.3 Synthetic route of 8-nitrochrysin
2 白杨素烷基化、酯化衍生物的合成及生理活性
刘毅等人[5]将烷基引入到白杨素衍生物A环的7位,并通过体外四甲基偶氮唑盐(MTT)法检测到所合成的含烷氧基白杨素衍生物对HL-60、HT-29和SGC-7901细胞增殖具有不同程度的抑制作用.赵菲菲等人[6]以白杨素、氯化苄为原料合成了7-苄氧基白杨素.文献[7]对白杨素7-位羟基烷基化后(图4),发现部分衍生物具有降低链尿佐菌素所致糖尿病大鼠血糖的作用,而白杨素本身未出现降糖作用.

图4 白杨素烷基衍生物的合成Fig.4 Syntheses of chrysin alkyl derivatives
Shin J S等人[7]还以白杨素为原料通过两种方式(图5和图6),合成了8种白杨素酯化衍生物,并通过给小鼠注射链尿佐菌素实验和紧急毒性实验,表明化合物12、16和18具有显著的降血糖作用,其降糖作用高于母体化合物白杨素,但低于7-位丙基、丁基和辛基取代的白杨素衍生物(即化合物4、5、6).

图5 白杨素酯化衍生物的合成Fig.5 Syntheses of chrysin acetyl derivatives

图6 白杨素酰化衍生物的合成Fig.6 Syntheses of chrysin acyl derivatives
5,7-二甲氧基白杨素由郑兴等合成[8],董琳等[9]采用MTT比色法和细胞计数法等一系列实验证实,5,7-二甲氧基白杨素(dMChR)具有显著地抑制人急性髓性白血病(HL-60)细胞的增殖效应.dMChR通过活化PPARγ、促进PTEN蛋白抑制Akt蛋白磷酸化,诱导人急性髓性白血病细胞生长的抑制和凋亡,其作用强于先导化合物ChR.
3 白杨素羟甲基化、氟甲基化衍生物的合成及生理活性
陈莉莉等人[1]以白杨素为先导化合物,对其进行了羟甲基化结构修饰,得到了6种衍生物(图7),并采用荧光技术,利用光谱探针EB研究了这些白杨素衍生物与CT-DNA的作用.结果表明:白杨素羟甲基化衍生物对DNA的亲和力明显强于白杨素,并且这些化合物可以显著延长断头后小鼠喘息时间、亚硝酸钠中毒小鼠存活时间,以及心肌特异性缺氧小鼠存活时间,说明这些化合物均具有一定的抗缺氧作用,其中化合物a,即5,7-二羟基-6,8-二羟甲基黄酮的抗缺氧效果最好.
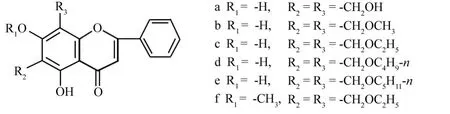
图7 白杨素羟甲基化衍生物的结构Fig.7 Structures of chrysin hydroxymethyl derivatives
许雪梅等人[10],为了获得高效、低毒的新型抗肿瘤先导化合物,通过改良的Baker-Venkataraman重排法,以间苯三酚为原料,合成α-卤代邻羟基苯乙酮,然后与对(三氟甲基)苯甲醛反应,将三氟甲基分别引入到白杨素衍生物B环的2、3、4位,初步药理活性研究表明:所合成的含三氟甲基白杨素衍生物对 HL-60、HT-29细胞增殖具有不同程度的抑制作用,抗癌活性强于阳性对照药5-氟尿嘧啶(5-Fu).
康颖等[11]以白杨素(ChR)为先导化合物,首先选择性地用二氟甲氧基取代白杨素的7位羟基,合成7-二氟甲氧基-5-羟基白杨素衍生物ChR1,再将一系列烷氧基取代ChR1的5位羟基,合成了一系列7-二氟甲氧基-5-烷氧基白杨素衍生物ChR2(图8).并采用MTT比色法测定了白杨素及白杨素衍生物对人胃癌细胞株SGC-7901的增殖抑制作用,发现在白杨素7位引入二氟甲氧基可以明显增强ChR类化合物对SGC-7901细胞增殖的抑制作用;在此基础上烯丙氧基的5位取代获得的7-二氟甲氧基-5-烯丙基白杨素(ADFMChR)具有更强的抑制人胃癌细胞增殖的活性.许金华等人[12]用人肺癌A549细胞裸鼠移植瘤模型治疗实验评价ADFMChR治疗肺癌的有效性.结果表明白杨素衍生物ADFMChR具有较强的抑制人肺癌A549裸鼠异种移植瘤的作用.

图8 7-二氟甲氧基-5-烷氧基白杨素衍生物的合成Fig.8 Synthetic route of 7-difluoromethoxy-5-substutited-alkoxyl chrysin derivatives
郑兴等[8]还以白杨素为原料,合成了6,8-二(三氟甲基)-5-羟基-7-乙酰氧基白杨素(图9).

图9 6,8-二(三氟甲基)-5-羟基-7-乙酰氧基白杨素的合成Fig.9 Synthetic route of 6,8-ditrifluoromethyl-5-hydroxy-7-acetoxychrysin
邹晓青等[13]证明了白杨素及白杨素乙酰化、卤化、三氟甲基化衍生物对体外培养人胃癌(SGC-7901)细胞,人急性粒细胞性白血病(HL-60)细胞和 HT-29细胞具有抑制增殖作用,其中以6,8-二(三氟甲基)-5-羟基-7-乙酰基白杨素作用最强.另外,6,8-二(三氟甲基)-5-羟基-7-乙酰基白杨素对小鼠Lewis肺癌皮下移植原发瘤及自发性肺转移具有抑制作用,呈剂量依赖关系,具有抗肿瘤作用.
4 白杨素偶联杂环及一氧化氮供体衍生物的合成及生理活性
Suresh B K等[14]制备了三个系列的白杨素O7-偶联杂环白杨素衍生物(图10),并通过对所制备的目标化合物进行革兰氏阳性菌和阴性菌的抑制试验检测了它们的抑菌活性,结果显示大部分衍生物的抗菌活性都强于母体化合物白杨素.

图10 O7-偶联杂环白杨素衍生物的合成Fig.10 Synthetic route of 7-position O coupled to heterocyclic moiety of chrysin derivatives
彭圣明等[15]以白杨素为原料,将不同类型的NO供体通过不同的中间链与白杨素偶联,得到不同类型的新化合物,其中NO供体包括有机硝酸酯类化合物、呋喃氮氧化合物、N-羟基胍类化合物三类.
白杨素偶联硝酸酯类一氧化氮供体衍生物的合成分两种途径:Ⅰ类目标化合物和Ⅱ类目标化合物的合成路线分别见图11和图12.

图11 Ⅰ类目标化合物的合成路线Fig.11 Synthetic route of the first kind of target compounds
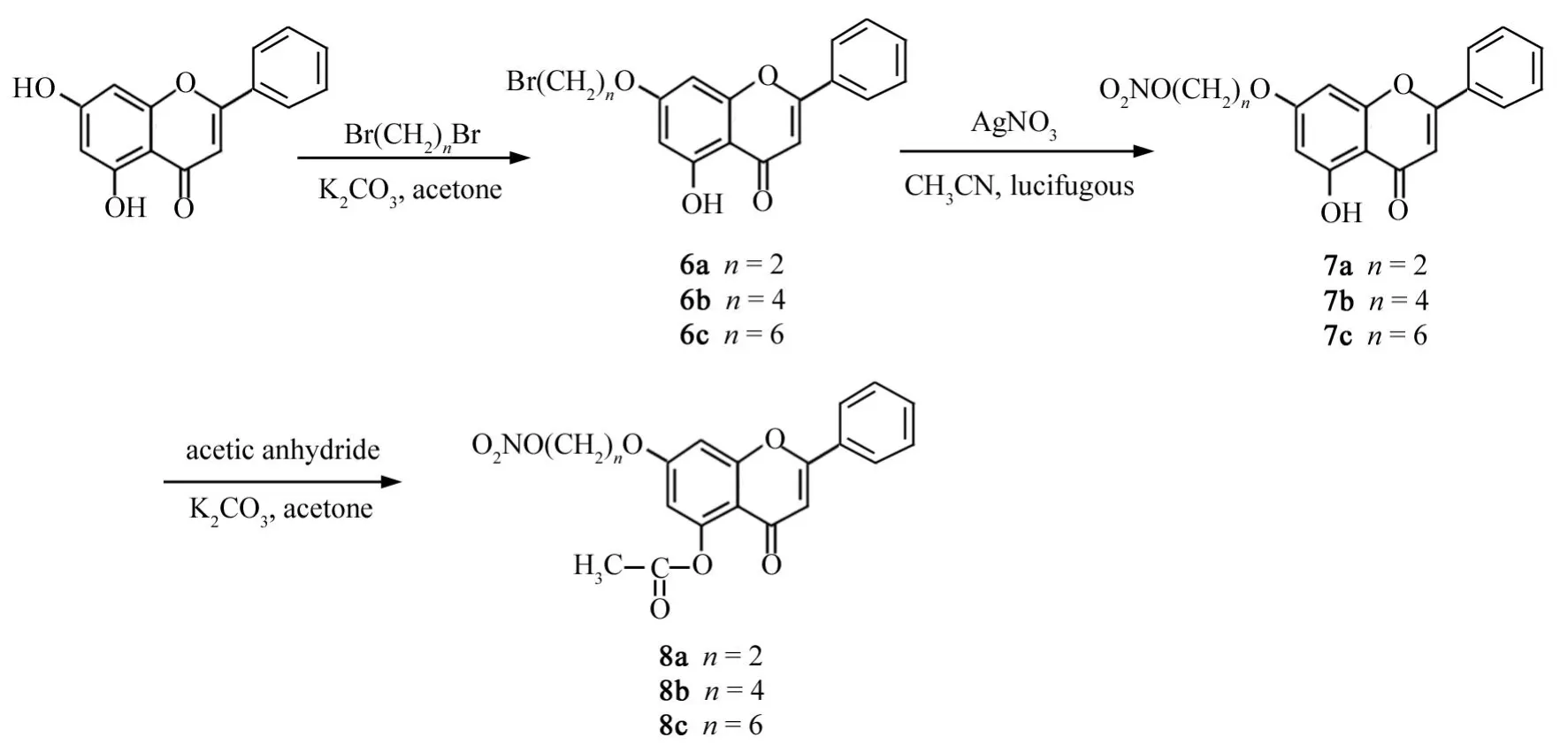
图12 Ⅱ类目标化合物(7a~7c和8a~8c)的合成路线Fig.12 Synthetic route of the second kind of target compounds
白杨素偶联呋喃氮氧化物类一氧化氮供体衍生物的合成分两种途径:Ⅲ类目标化合物和Ⅳ类目标化合物的合成路线如图13和图14所示.

图13 Ⅲ类目标化合物(15a、15b、16a、16b)的合成路线Fig.13 Synthetic route of the third kind of target compounds

图14 Ⅳ类目标化合物(17、18)的合成路线Fig.14 Synthetic route of the fourth kind of target compounds
白杨素偶联N-羟基胍类一氧化氮供体衍生物(Ⅴ类目标化合物)的合成路线见图15.

图15 Ⅴ类目标化合物的合成路线Fig.15 Synthetic route of the fifth kind of target compound
彭圣明等采用体外化学酶体系的活性筛选模型,通过体外α-葡萄糖苷酶抑制活性实验,测定目标化合物对α-葡萄糖苷酶的抑制活性,结果表明:目标化合物对α-D-葡萄糖苷酶活性的抑制率与化合物存在剂量呈依赖关系,抑制率随着药物浓度的增大而升高.他们还通过体外四甲基偶氮唑盐(MTT)实验来测定目标化合物对人脐静脉内皮细胞株(HUVECs-12)的毒性和细胞的增殖活性,结果表明:在适当的浓度下所有目标化合物对HUVECs-12均未产生细胞毒性作用,其中部分目标化合物对 HUVECs-12还具有一定的促细胞增殖作用. 通过体内鸡胚绒毛尿囊膜(CAM)实验 ,表明 5a、5b、5c、7a、7b、7c、15a、15b、16a、16b、17 表现出较强的促进CAM新生血管生成作用.
总之,彭圣明等所合成的化合物中7b、15a、15b、16b和17既具有较强的α-葡萄糖苷酶抑制活性,又表现出较强的促进CAM新生血管生成作用.这5个化合物将在开发糖尿病及其血管并发症药物方面具有很好的前景,值得深入研究.
5 白杨素磷酰化衍生物的合成及生理活性
李文锋等[16]分两个途径对白杨素进行了含磷改造,一是利用Atherton-Todd反应对白杨素直接磷酰化改造,合成出6种化合物(图16),其中四种为新化合物;二是首次将磷酰化氨基酸引入到白杨素结构中,将N-磷酰化氨基酸与白杨素7位羟基脱水成酯,合成出5种新的化合物(图17).他们在以前研究的基础上,将所合成的部分白杨素含磷衍生物与溶菌酶进行弱相互作用研究.结果表明:白杨素含磷衍生物与溶菌酶具有更强的亲和力,并且引入磷化氨基酸的白杨素衍生物7~11与溶菌酶的结合能力比直接引入磷酰基的1~6更强.

图16 白杨素磷酰化衍生物的结构式Fig.16 Structures of chrysin phosphoryl derivatives

图17 N-磷酰化氨基酸与白杨素7-位羟基酯化衍生物的结构式Fig.17 Structures of chrysin N-phosphoryl amino acid ester derivatives
陈晓岚等人[17]利用磷酰化反应将磷酰化氨基酸酯引入到白杨素中,合成了一种新型的白杨素-7-氨基磷酸酯衍生物,其活性试验正在测试中,合成路线见图18.
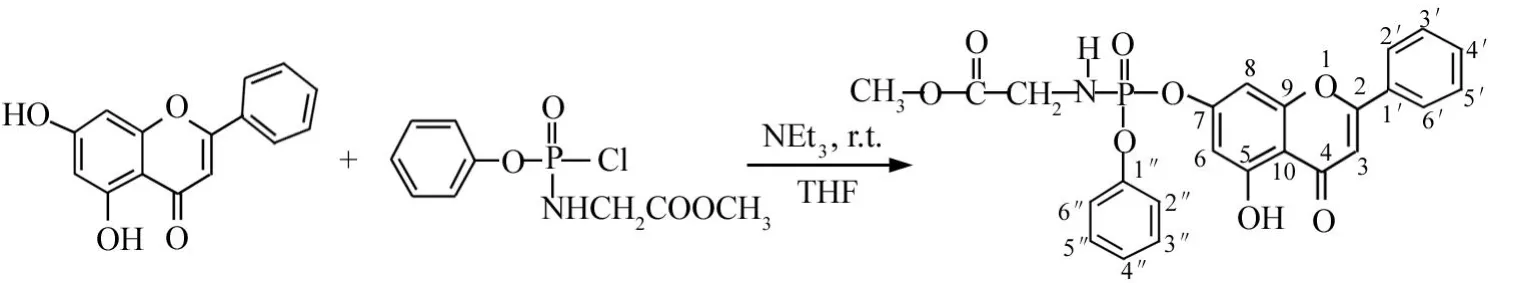
图18 白杨素-7-氨基磷酸酯衍生物的合成路线Fig.18 Synthetic route of chrysin-7-phosphoramidate derivative
张婷等人[18]合成了白杨素四乙基二磷酸酯(图19),并经过一系列试验发现,白杨素和白杨素四乙基二磷酸酯处理后的宫颈癌Hela细胞软琼脂的集落形成率大大降低,能诱导并促进宫颈癌Hela细胞发生分化,且白杨素四乙基二磷酸酯在作用效果方面较白杨素明显;另外,它们还可以诱导宫颈癌 Hela细胞核基质成分改变,且以后者处理作用明显.
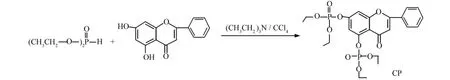
图19 四乙基白杨素二磷酸酯的合成路线Fig.19 Synthetic route of chrysin tetraethyl bis-phosphoric ester
6 白杨素氨基化衍生物的合成及生理活性
乔玉林等[19]以白杨素为起始物通过硝化、还原等反应得到了一系列白杨素6、8位氨基取代的衍生物(图20),并对这些衍生物进行了α-葡萄糖苷酶的抑制活性实验.结果显示,6-氨基白杨素的活性相对于白杨素有很大程度的改进,6,8-二氨基白杨素是6-氨基白杨素活性的1/34,而8-氨基白杨素活性则完全消失.

图20 白杨素6,8-位氨基取代衍生物的合成路线Fig.20 Synthetic route of chrysin amino derivatives
7 前景展望
研究表明天然黄酮类化合物中抗肿瘤活性最高的化合物是5,7-二羟基黄酮即白杨素.从20世纪80年代起,人们便开始了白杨素的结构修饰及衍生物的化学合成研究.近年来,国内外对白杨素及其衍生物的研究报道日益增多,且已获得一些有良好活性的该类化合物,其临床应用前景也逐渐显露,可是至今仍未见有此类药物研发上市.虽然白杨素具有抗氧化、抗病毒、抗高血压、抗肿瘤、抗过敏等作用,但因其肠道吸收甚少和5,7位羟基被迅速羰基化代谢导致活性降低的原因,从而影响了白杨素的临床应用.相信随着对白杨素及其衍生物的进一步研究,一定能发现活性更好、专一性更强、生物利用度更高的白杨素衍生物.
[1]陈莉莉.黄酮体羟甲基化衍生物合成及其药理作用究[D].陕西师范大学,2007.
[2]史娟.白杨素-6-磺酸根与金属离子自组装作用及晶体结构研究[D].陕西师范大学,2006.
[3]谭大金,贺云,邱李,等.白杨素-6-磺酸钠及其Zn(Ⅱ)、Ca(Ⅱ)配位化合物与NDA作用的研究[J].化学研究与应用,2007,19(5):502-504.
[4]徐阳炎,郑兴,朱炳阳,等.8-硝基白杨素的合成及其抗肿瘤作用[J].南华大学学报医学版,2004,32(3):283-285.
[5]刘毅,赵菲菲,郑兴,等.7-烷氧白杨素衍生物合成及其抗癌活性研究[J].南华大学学报医学版,2009,37(5):517-531.
[6]赵菲菲,许雪梅,郑兴,等.7-苄氧白杨素急性毒性实验[J].南华大学学报医学版,2009,37(1):8-9.
[7]SHIN J S,KIM K S,KIM M B,et al.Synthesis and hypoglycemic effect of chrysin derivatives[J].Bioorg Med Chem Lett,1999,9:869-874.
[8]ZHENG Xing,MENG Wei Dong,XU Yang Yan,et al.Synthesis and anticancer effect of chrysin derivatives[J].Bioorg Med Chem Lett,2003,13(5):881-884.
[9]董琳.5,7-二甲氧基白杨素诱导人急性髓性白血病细胞生长抑制和凋亡作用的实验研究[D].南华大学,2007.
[10]许雪梅,赵菲菲,郑兴,等.B环三氟甲基取代的白杨素衍生物合成及其抗癌活性[J].南华大学学报医学版,2009,37(2):129-131.
[11]康颖,郑兴,徐阳炎,等.7-二氟亚甲基-5-取代烷氧基黄酮类化合物的合成及其对人胃癌细胞增殖的抑制作用[J].美国中华临床医学杂志,2006,8(1):63-65.
[12]许金华,谭翔文,秦勇,等.5-烯丙基-7-二氟亚甲基白杨素对人肺癌A549细胞裸鼠移植瘤生长的影响[J].中国实验动物学报,2009,17(5):373-376.
[13]邹晓青,郑兴,曹建国,等.6,8-二(三氟甲基)-5-羟基-7-乙酰基白杨素的抗肿瘤作用[J].中国药理学通报,2004,20(4):453-457.
[14]SURESH BABU K,HARI BABU T,SRINIVAS P V,et al.Synthesis and biological evaluation of novel C(7)modified chrysin analogues as antibacterial agents[J].Bioorg Med Chem Lett,2006,16:221-224.
[15]彭圣明.白杨素偶联一氧化氮供体衍生物的合成及α-葡萄糖苷酶抑制和促血管生成活性研究[D].湘潭大学,2009.
[16]李文锋.白杨素含磷衍生物的合成及与溶菌酶弱相互作用研究[D].郑州大学,2007.
[17]陈晓岚,张守仁,屈凌波,等.新型白杨素-7-氨基磷酸酯衍生物的合成与波谱学研究[J].波谱学杂志,2009,26(2):240-241.
[18]张婷,陈晓岚,屈凌波,等.白杨素和它的四乙基二磷酸酯对人宫颈癌Hela细胞增殖和核基质蛋白影响的研究[J].药物生物技术,2005,12(5):312-316.
[19]GAO Hong,KAWABATA J.α-Glucosidase inhibition of 6-hydroxyflavones.Part 3:Synthesis and evaluation of 2,3,4-trihydroxybenzoyl-containing flavonoid analogs and 6-aminoflavones asα-glucosidase inhibitors[J].Bioorg Med Chem,2005,13:1661-1671.
Research progress of synthesis and biological activities of chrysin derivatives
WANG Qiu-ya,WAN G Ye-juan,GAO Jin-hong
(Department of Chemistry and Chemical Engineering,Weinan Teachers University,Weinan714000,Shaanxi,China)
O 625.15
A
1008-1011(2011)01-0096-08
2010-08-29.
渭南师范学院重点科研资助项目(10YKF015)和渭南师范学院专项科研资助项目(08YKZ002).
王秋亚(1978-),女,讲师,主要从事有机合成及结构分析研究.E-mail:wqiuya1978@163.com.
