新型重金属离子捕集剂的合成及其对废水中铜离子的捕集作用
2011-09-24刘代琴苏纯华余训民关洪亮
张 余,刘代琴,苏纯华,余训民,关洪亮
(武汉工程大学环境与城市建设学院,湖北武汉 430073)
新型重金属离子捕集剂的合成及其对废水中铜离子的捕集作用
张 余,刘代琴,苏纯华,余训民*,关洪亮
(武汉工程大学环境与城市建设学院,湖北武汉 430073)
以活化硅胶为载体,γ-氯丙基三甲氧基硅烷为偶联剂,由乙二胺和二硫化碳合成了新型的具有螯合功能的氨基硫代甲酸聚合物(EPCR).研究了 EPCR用量、p H值、反应时间、温度等对乙二胺四乙酸(EDTA)配合Cu2+溶液中Cu2+去除率的影响,确定了最佳去除条件.结果表明,EPCR对 Cu2+的最大吸附量为34.10 mmol/g,最高去除率可达99.68%.吸附铜离子后的捕集剂经稀硫酸洗脱后可再利用,去除效率仍然在99%以上,洗脱的铜可回收利用.
重金属离子;捕集剂;铜离子;废水处理
Abstract:A new type of heavy metal ion trapping agent poly(amino thiocarbamate)with cheating function(coded as EPCR)was synthesized from ethylenediamine and carbon disulfide in the presence of activated silica gel as the support andγ-chloropropyl-trimethoxy silane as the coupling agent.The influence of EPCR dosage,p H value,reaction time,and temperature on the removal rate of Cu2+ions in Cu2+-ethylenediamine tetraacetic acid(EDTA)complex solution was examined,and the optimized condition for removing Cu2+was established.Results show that EPCR had a maximum adsorption capacity of 34.10 mmol/g for Cu2+ions,and Cu2+was removed at a highest rate of 99.68%.Used EPCR after adsorbing Cu2+ions could be recycled by elution in diluted sulfuric acid,and the removal efficiency was maintained at 99%.Besides,the eluted copper could also be reused.
Keywords:heavy metals ion;trapping agent;copper ion;wastewater treatment
用传统的化学沉淀法处理含重金属离子废水,药剂用量大、操作复杂、易造成二次污染.近年来,国内外开展了应用具有螯合功能的有机重金属离子捕集剂去除废水中的重金属离子,并进行其资源化回收利用方面的研究,取得了可喜成效[1-9].这类捕集剂具有操作简单、生成的污泥不产生二次污染等优点.本文作者合成了具有螯合功能的聚硅酸二甲氧基丙基硅氧基乙二胺硫代甲酸EPCR,它能与一些重金属离子如Cu2+等发生螯合反应,生成稳定的絮状沉淀,从而达到去除重金属离子的目的.作者以含Cu2+的模拟废水为例,研究了EPCR对Cu2+的捕集效果.
1 实验部分
1.1 试剂与仪器
硅胶 G(A R),γ-氯丙基三甲氧基硅烷(工业级),乙二胺(A R),二硫化碳(A R),氢氧化钠(A R),甲苯(A R),无水乙醇(A R),丙酮(A R),硝酸(A R),氯化铜(A R)等.
Quanta 200扫描电镜+X射线能谱(荷兰 FEI);红外光谱仪(美国,Perkin Elmer);p HS-3C型精密p H计(上海精密仪器有限公司),ICP-MS(美国瓦里安公司ICP-MS710).
1.2 实验方法
EPCR的合成:以硅胶、γ-氯丙基三甲氧基硅烷、乙二胺、二硫化碳为原料,在一定条件下,合成了具有螯合功能的聚硅酸二甲氧基丙基硅氧基乙二胺基硫代甲酸(EPCR).对EPCR样品进行了红外光谱测定,结果表明:N-H的伸缩振动吸收为3 307.24 cm-1;-NH2的伸缩振动吸收为1 628.41 cm-1;2 957.00 cm-1附近的峰为-CH2的伸缩振动吸收;1 495 cm-1处出现的峰为胺基硫代甲酸类化合物中的S=C-N键伸缩振动吸收,介于C-N单键吸收(1 300 cm-1)和C=N双键吸收(1 600 cm-1)之间,具有大π键特征;C-S键的红外特征吸收为980.99 cm-1,小于C S键的特征吸收(1 501~1 200 cm-1),805.36 cm-1附近的峰为S=C-S-基团的吸收峰.IR数据充分说明合成得到了EPCR.
沉淀原理:EPCR结构中的氮、硫均含有孤对电子,在一定的温度和p H值条件下,能够与Cu2+形成稳定的螯合物而沉淀.EPCR与Cu2+形成的螯合物的IR谱图与 EPCR的 IR谱图相比较,发生了明显变化:S=C-N键伸缩振动吸收峰由1 495 cm-1变至1481.90 cm-1;C-S键的红外特征吸收峰由980.99 cm-1处移到957.35 cm-1处;S=C-S-基团的吸收峰由805.36 cm-1处移到791.81 cm-1附近.该含铜螯合物在p H≤0时很不稳定,Cu2+很快从捕集剂上解离下来.因此,在改变p H值的条件下,可使含Cu2+废水的治理达到 GB8978-1996中的一级排放标准,同时可回收沉淀中的铜,达到铜资源化利用的目的.
废水处理及分析方法:称取460 mg EPCR,配制成460 mg/L EPCR的钠盐溶液备用,配制含Cu2+100 mg/L的 EDTA配合物溶液.分别取50 mL的含Cu2+模拟废水,装入7个100 mL的烧杯中,在不同条件下投加 EPCRNa溶液,以200 r/min的速率进行搅拌,反应一定时间后,静置20 min,用0.45μm的滤膜过滤,采用ICP-MS测定清液中残余铜的浓度.废水中Cu2+的去除率ηCu由(1)式计算.

EPCRNa吸附铜的量QCu(mg/g)根据(2)式计算.

式(1)和(2)中:c0为原废水中铜离子浓度(mg/L);ct为t时刻后废水中残余铜的浓度(mg/L);V为所取的废水样的体积(L);m为EPCRNa的质量(g).
2 结果与讨论
2.1 p H值对铜离子去除率的影响
在不同p H值的7个烧杯中,分别加入4 mL EPCRNa溶液,25℃时反应所得的实验结果见图1.由图1可知,当p H值由2增大到4时,Cu2+的去除率直线上升,到p H=5时,Cu2+的去除率为99.24%,p H值继续升高对Cu2+的去除率影响不大.p H值小于5时,由于酸效应,Cu2+的去除效果会下降,酸性越强,去除效果越差.当p H值增大到6时,Cu2+的去除率为99.65%,p H值再增大,Cu2+的去除率增加得不明显,p H=7,ηCu=99.75%.
2.2 EPCRNa的用量对Cu2+去除率的影响
固定7个烧杯的p H=7时,25℃时测得不同EPCRNa投入量对废水中Cu2+去除率的实验结果见图2.由图2可知,当 EPCRNa用量为5 mL时,铜离子的去除率达99.63%,再增加 EPCRNa用量,对铜离子的去除率增加很小.

图1 p H对铜离子去除率的影响Fig.1 The p H influence on Cu2+removal rate
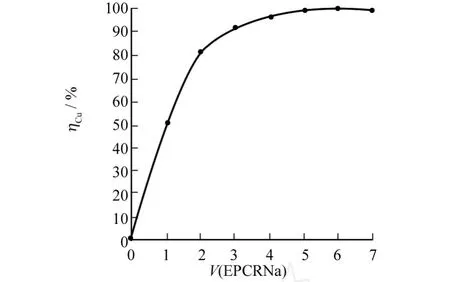
图2 EPCRNa的用量对Cu2+去除率的影响Fig.2 The influence of the EPCRNa dosage on Cu2+removal rate
2.3 反应时间对Cu2+去除率的影响
固定7个烧杯的p H值为7,以不同时间投加5 mL EPCRNa,25℃时所得的实验结果见图3.由图3可知,吸附达到平衡的时间为2.5 min,Cu2+的去除率达到99.68%,再增加反应时间,对Cu2+的去除率影响很小.
2.4 温度对Cu2+去除率的影响
根据上述得出的最优条件,测得不同反应温度对Cu2+去除率ηCu的实验结果(表1).由表1可知,反应温度对Cu2+的去除率影响不大.考察不同温度下 EPCRNa对沉淀分配比 D=Qe/ce[9]的影响,以lgD对103×1/T作图,如图4所示.吸附符合温度系数法公式[9]:lgD=-ΔH/(2.303R T)+ΔS/(2.303R),由图中直线斜率和截距求得ΔH=-13.20 kJ/mol,ΔS=36.94 J/(mol·K).再由ΔG=ΔH-TΔS求得在298.15 K时ΔG=-24.21 kJ/mol.因为ΔG<0,故沉淀是正向自发进行的.

表1 反应温度对Cu2+去除率ηCu的影响Table 1 The effect of temperature on removal rate of Cu2+
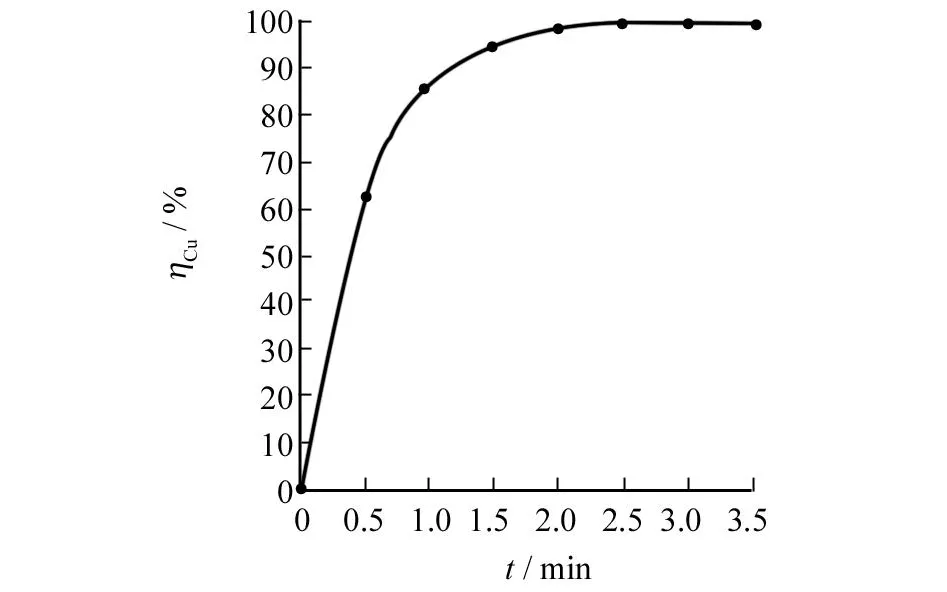
图3 搅拌时间对Cu2+去除率的影响Fig.3 The effect of the string time on Cu2+removal rate

图4 温度对沉淀效果的影响Fig.4 The effect of temperature on static adsorption
2.5 沉淀吸附动力学方程
配制浓度为30 mg/L、40 mg/L、50 mg/L、75 mg/L、80 mg/L、100 mg/L 和 110 mg/L 的 EPCRNa溶液,各取50 mL加到7个200 mL的烧杯中,分别加入50 mL含Cu2+100 mg/L的EDTA络合物溶液,按上述最佳条件处理各含铜废水,结果见表2.由表1可知,常温下EPCRNa对Cu2+的最大沉淀量为2.167 0 g/g.人们常用Freundlich和Langmuir方程来描述等温吸附,Freundlich等温吸附方程为:

式(3)中:Qe为平衡吸附量(g/g);K为与吸附剂、吸附质种类及温度有关的系数;n为与温度有关的常数,n>1,可根据实验确定;ce为吸附平衡时溶质的浓度(mg/L).将式(3)取对数得:


表2 等温吸附实验结果Table 2 The result of adsorption isotherms
根据表2的数据,对式(4)进行拟合得到:

式(5)的相关系数为0.999 4,说明吸附沉淀符合Freundlich规律.由式(5)得:n=3.628 4,K=1 674.17 mg/L.因1/n介于0.1~0.5之间,说明沉淀反应容易进行.Langmuir等温吸附方程为:

式(6)中,b为与温度有关的常数,Q0为理论(极限)吸附容量.根据表2的实验数据,对式(6)进行拟合得到:

式(7)的相关系数为0.994 5,表明吸附沉淀符合Langmuir等温吸附模式.由式(7)得理论吸附容量 Q0=2.171 1 g/g,与实验得到的 Qe=2.167 0 g/g较接近;1/(Q0b)=0.099 8,则b=4.615 2 mg/L.
2.6 反应速率及活化能
根据Langmuir提出的速率方程[9]:

其中,Qt和Qe分别为某时刻和达到平衡时的吸附量,k为表观速率常数.根据2.3中的数据,由-ln(1-F)对 t作图得一直线(图5).在298.15 K时,k=2.096 1 min-1.EPCRNa与Cu2+的沉淀符合一级反应速率方程:-ln(1-F)=2.096 1t. 同理得到 T=283.15、293.15、303.15和313.15 K时的表观速率常数 k分别为1.603 2、1.875 7、2.177 1和2.504 1 min-1.根据公式:k=Aexp(-Ea/R T),由logk对1/T作图得一直线,求得表观活化能 Ea为10.99 kJ/mol.由于 Ea比较低,十分有利于沉淀反应的快速进行.

图5 -ln(1-F)与时间 t的关系Fig.5 The relation between-ln(1-F)andt
2.7 EPCRNa的洗脱
EPCRNa吸附Cu2+后,以20%硫酸洗脱,洗脱后的 EPCRNa重复使用实验结果见表3.

表3 回收 EPCRNa对Cu2+吸附效率的比较Table 3 Comparison of Cu2+adsorption capacity to reclaim EPCRNa
实验结果表明,多次重复使用EPCRNa,其吸附效率仍然可达99%.EPCRNa重复使用10次,沉淀效率仅下降0.62%.洗脱的铜可以回收制备硫酸铜.
2.8 捕集机理
EPCR-带有黄原羧酸官能团,其双键S原子上的电子流动性较大,具有较强的给电子能力,对重金属阳离子有较强的捕集能力,生成的重金属盐如铜盐、银盐等都不溶于水,易于从废水中分离出来,从而可达到处理含重金属离子废水的目的.EPCR-与重金属离子Mn+发生螯合反应生成难溶的沉淀物,其反应机理如下:

上述反应的机理从IR光谱图和XPS能谱图上可得到证实.
3 结论
1)EPCRNa处理重金属废水时,投加量少,易操作,吸附形成的沉淀易于沉降分离,去除率高.相对于传统的化学沉淀法来讲,后续处理简便,可节省处理费用.
2)研究结果表明:每克Cu2+需要0.46 g的 EPCRNa处理剂,搅拌时间为2.5 min,p H值为中性,去除率为99.63%;EPCRNa对Cu2+的最大吸附容量为34.10 mmol/g.
3)用20%的硫酸解吸 EPCRNa捕集的重金属铜,经洗脱后,EPCRNa重复使用10次,其处理效率仍在99%以上;从洗脱液中可回收铜,进行资源化利用,具有良好的经济价值.
[1]蒋建国,王伟,赵翔龙,等.重金属螯合剂在废水治理中的应用研究[J].环境科学,1999,1:65-67.
[2]KREISL ER L.Method for recovering and separating metals from waste streams.US 5908559[P].1999.
[3]SALMEN K S,KOWALSKI A S,ZEIHER E H K,et al.Composition and method for simultaneously precipitating metal ions from semiconductor wastewater and enhancing micro filter operation.US 6258277[P].2001.
[4]王碧,许桂丽,胡星琪.含羟肟酸侧基高分子重金属捕集剂处理含铅废水的研究[J].化学研究与应用,2008,20(5):561-564.
[5]郭晓滨,李晓池,王晓刚.重金属螯合剂在含铜废水处理中的应用[J].西安科技学院学报,2003,23(4):421-424.
[6]郑怀礼,陈春艳,岳虎秀,等.重金属离子捕集剂DTCEDA的合成及其应用[J].环境化学,2006,25(6):765-767.
[7]王进喜,常青,章敏,等.PEA-TGA复配絮凝除浊、去铜的研究[J].环境科学与管理,2006,31(6):51-53.
[8]胡钰倩,余训民,孙家寿,等.冶炼废水无害化和资源化的研究[J].武汉工程大学学报,2007,29(2):34-40.
[9]HU Li Song,HU Yu Qian,YU Xun Min,et al.Removal and reclamation of copper ions by PSEP chelae resin[R].Twelfth international symposium on water rock interaction,New York:Academic Press,2007:1567-1571.
Synthesis of a heavy metal ion trapping agent and it application in treatment of copper-containing w astew ater
ZHANG Yu,LIU Dai-qin,SU Chun-hua,YU Xun-min*,GUAN Hong-liang
(College of Environment and Civil Construction,Wuhan Institute ofTechnology,Wuhan430074,Hubei,China)
X 703.1
A
1008-1011(2011)01-0069-05
2010-09-20.
湖北省科技攻关项目(2007AA101C70)和武汉工程大学研究生研究创新基金资助项目.
张余(1985-),女,硕士生,主要从事水污染控制与废物资源综合利用研究.*
xym856917@163.com.
