锂离子电池正极材料Li(1-2x)MgxMnPO4/C的合成与表征
2011-09-24赵艳艳张玉荣
赵艳艳,张玉荣
(福州大学化学化工学院,福建福州 350108)
锂离子电池正极材料Li(1-2x)MgxMnPO4/C的合成与表征
赵艳艳,张玉荣*
(福州大学化学化工学院,福建福州 350108)
采用溶胶凝胶法合成前驱体,再在空气气氛中分别于400℃、500℃和600℃下焙烧,得到锂离子电池正极材料Li(1-2x)MgxMnPO4/C(0≤x≤0.1);利用X射线衍射分析、环境扫描电镜分析、恒流充放电、阻抗测试等分析了产物的结构、形貌和电化学性能.结果表明,合成的Li(1-2x)MgxMnPO4/C颗粒呈球形,具有橄榄石结构;引入镁不改变其晶型,但使得其电化学性能得到改善.起始组成为 x=0.03的样品的放电容量最高、循环性能最好;经空气气氛中400℃下焙烧后,其在2.8~4.4 V范围内、0.02 C下的放电容量达到128 mAh·g-1,经100次循环后容量保持在72 mAh·g-1.
锂离子电池;正极材料;LiMnPO4;合成;表征
Abstract:Li(1-2x)MgxMnPO4/C composite cathode materials for lithium ion batteries were synthesized by preparing precursorsviasol-gel method and follow-up heat-treatment at 400℃,500℃and 600℃in air.The crystal structure and morphology of the products were investigated by means of X-ray diffraction and environmental scanning electron microscopy.The electrochemical performance of the products was measured by conducting galvanostatic charge-discharge test and alternating current impedance test.Results show that as-synthesized Li(1-2x)MgxMnPO4/C particulates have uniform spherical shape and consist of pure olivine-structured phase.The introduction of Mg had no effect on the crystal structure of LiMnPO4/C but contributed to improve the electrochemical performance.The sample with initial composition ofx=0.03 possessed the best electrochemical performance;it had a discharge capacity of 128 mAh·g-1after being heated at 400℃in air and tested at 0.02 C rate,and the discharge capacity was maintained at 72 mAh·g-1after 100 cycles.
Keywords:lithium ion batteries;cathode material;LiMnPO4;synthesis;characterization
在锂离子电池正极材料中,橄榄石结构的LiFePO4已经获得了商业使用.但其相对低的电压平台(3.4 V)使其能量密度较低限制了其发展应用.与LiFePO4具有相同结构的LiMnPO4,相对于Li+/Li的电极电势为4.1V[1],远高于LiFePO4的电压平台,且位于现有电解液体系的电化学稳定窗口,这就使这种材料具有潜在的高能密度的优点.然而,由于LiMnPO4材料导电性极差[2],被认为是绝缘体,致使合成能够可逆充放电的LiMnPO4非常困难,限制了其发展应用.目前,关于化学活性的LiMnPO4的报道并不多.Li等[3]和Thierry等[4]对可充放电的LiMnPO4进行了研究,通过碳包覆提高了材料的电化学性能,获得了比较理想的容量.Natalia等[5]和Delacourt等[6]通过不同方法合成了LiMnPO4纯相并对材料的电化学性能进行了研究.文献[7-10]通过不同的途径得到了LiMnPO4纯相,重点研究了这种材料在较高温度下的电化学性能.另外根据文献[11-12]的研究可知掺Mg后,LiFePO4的电导率得到了很大的提高,因此本研究通过掺碳并结合球磨的方法,用溶胶-凝胶法合成前驱体,在空气气氛中焙烧得到能进行可逆充放电的Li(1-2x)MgxMnPO4/C材料,并初步探讨了该材料在室温下的电化学性能.
1 实验部分
1.1 试剂和仪器
硝酸为化学纯试剂,导电碳和乙炔黑为工业纯.二水合醋酸锂、四水合醋酸锰、四水合醋酸镁、磷酸二氢铵、柠檬酸、蔗糖均为分析纯试剂.SENCO R系列旋转蒸发仪(上海申生科技有限公司);DZF-6020型真空干燥箱(上海博迅实业有限公司);ZKX-2B型真空手套箱(南京大学仪器厂);Philips X’pert Pro X射线衍射仪(荷兰Philips公司);Philips-FEI XL30 ESEM-TMP环境扫描电镜(荷兰 Philips公司);CS800型红外碳硫测试仪(德国 Eltar公司);ZAHNER Elektrik Thales IM6电化学工作站(德国).
1.2 正极材料Li(1-2x)MgxMnPO4/C的合成
根据化学式Li(1-2x)MgxMnPO4/C,按一定的化学计量比准确称取一定量的四水合醋酸锰、二水合醋酸锂、四水合醋酸镁、磷酸二氢铵和柠檬酸,分别溶于适量的去离子水中配成溶液.将醋酸锰溶液、醋酸锂溶液和醋酸镁溶液混合均匀并加入相当于产物质量分数为5%的碳的蔗糖,往混合溶液中加入柠檬酸溶液和磷酸二氢铵溶液,混合溶液用硝酸调节p H值至2左右,搅拌均匀.将搅拌均匀的溶液在70℃左右的水浴下旋转蒸发成凝胶,将凝胶在120℃下真空干燥后在空气气氛中于300℃预烧5 h得前驱体,将前驱体加入一定量的导电碳球磨研细、压饼后分别在空气气氛中于400℃、500℃和600℃下焙烧3 h,随炉冷却至室温,研细,得到产物Li(1-2x)MgxMnPO4/C.
1.3 产物的表征
将合成的正极材料干燥研细后在X射线粉末衍射仪上以Cu Kα靶作为辐射源对合成的样品进行物相分析,用环境扫描电镜对合成的样品进行形貌分析,用红外碳硫测试仪对合成材料中的碳的含量进行分析.
1.4 电池的组装与电化学测试
将正极材料(活性物质)、乙炔黑及聚偏二氟乙烯(PVDF)以80∶10∶10的质量比混合并研磨均匀后,加入适量的有机溶剂N,N-二甲基甲酰胺(DMF),研磨成糊状物后均匀涂覆于铝箔上,在120℃下真空干燥12 h制成正极片.以金属锂片(纯度大于 99.9%)作为负极,1 mol·L-1的LiPF6/EC+DMC+EMC(体积比1∶1∶1)有机溶剂为电解液,微孔聚丙烯膜(Celgard 2300)为隔膜,在充满氩气的手套箱中封装成CR2025型扣式电池.用LANDCT2001A电池测试系统测试样品的充放电性能,充放电电压范围为2.8~4.4 V,充放电倍率为0.02 C.阻抗测试是将装好的电池在IM6电化学工作站上进行,测试的频率范围为0.10~8.00×106Hz.
2 结果与讨论
2.1 结构分析
图1是400℃焙烧得到的Li0.94Mg0.03MnPO4/C的ESEM图.由图1可以看出,样品颗粒呈球形,分布比较均匀,样品颗粒细小,但存在明显团聚现象.小颗粒有比较大的比表面积,这样将有利于提高材料的比容量和循环性能.这点可以由下面的电化学性能得到验证.

图1 400℃焙烧得到的Li0.94Mg0.03MnPO4/C的ESEM图Fig.1 ESEM images of Li0.94Mg0.03MnPO4/C synthesized at 400℃
图2是合成样品的X射线粉末衍射(XRD)图.将衍射数据与LiMnPO4的标准图谱(卡片号PDF33-0803)对照可以看出产品均为橄榄石结构的纯相,空间群属于 Pmnb,图中没有观察到杂质峰,说明微量的Mg2+掺杂并没有改变LiMnPO4的橄榄石型晶体结构.此外,图中未观察到碳的任何晶相衍射峰,说明样品中的碳为无定形结构.另外从图2中的A可以看出产品的衍射峰随着温度的升高而增强,表明随着烧结温度的升高,产品的结晶度越来越高.
2.2 Li(1-2x)MgxMnPO4/C的电化学性能分析
通过红外碳硫测试仪对合成的材料中的碳含量进行测试,结果发现在空气气氛中400℃、500℃和600℃下焙烧得到的样品的碳含量分别为10.2%,9.4%和8.9%,即随着温度的升高样品中的碳含量越来越低,这是因为在空气气氛中焙烧,随着温度的升高有更多的碳被空气中的氧气氧化成CO2.
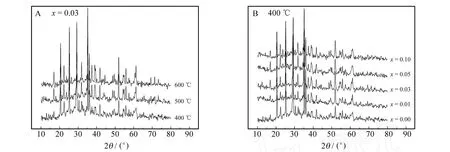
图2 Li(1-2x)MgxMnPO4/C样品的XRD图Fig.2 XRD patterns of Li(1-2x)MgxMnPO4/C
图3为样品在0.02 C下的循环性能图.由图3中的A可以看出,当 x=0时,在空气气氛中400℃下焙烧得到样品的首次放电容量最高为123 mAh·g-1,500℃和600℃下烧结所得样品的首次放电容量分别为82 mAh·g-1和73 mAh·g-1,经过50次循环后400℃、500℃和600℃焙烧所得样品的容量分别保持在42 mAh·g-1、27 mAh·g-1和21 mAh·g-1,由此可以看出随着循环的进行容量都出现不同程度的衰减,同时还可以看出,400℃下焙烧得到的样品具有最高的放电容量和最好的循环性能,这主要是由于400℃下焙烧得到的样品颗粒最小、含碳量最高,材料的导电性最强,从而有利于材料容量的发挥和循环性能的改善.
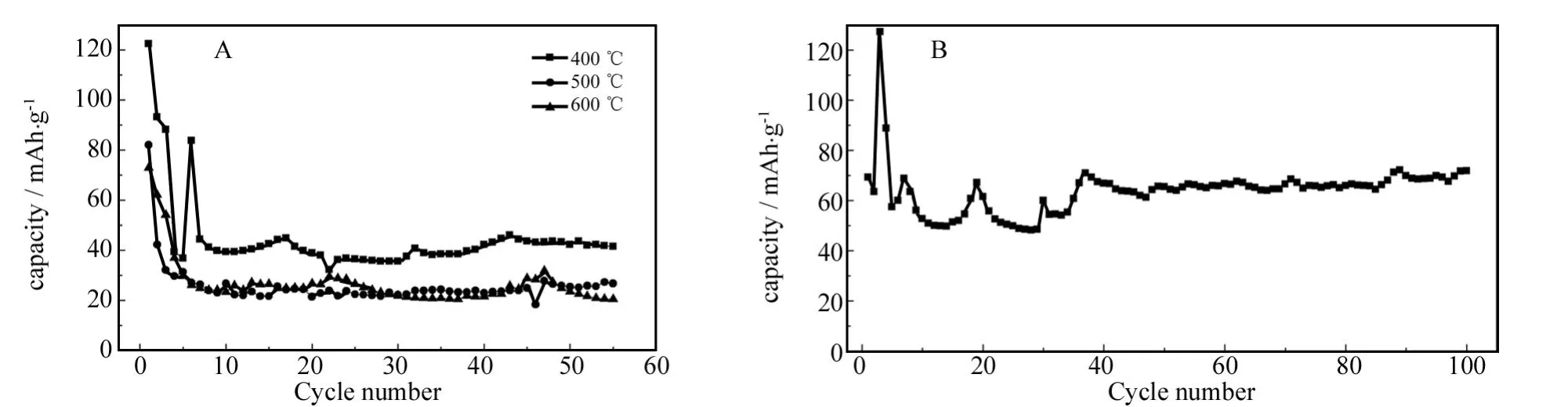
图3 Li(1-2x)MgxMnPO4/C样品的循环性能图Fig.3 Cycling performance of Li(1-2x)MgxMnPO4/C
为了研究Mg掺入量对材料充放电性能的影响,作者在空气气氛中400℃下焙烧得到了不同掺杂比例的Li(1-2x)MgxMnPO4/C样品,并以这些材料为正极材料组装成电池进行了充放电测试.结果表明,当掺杂量 x分别为0,0.01,0.03,0.05和0.10时,放电容量分别为123 mAh·g-1,61 mAh·g-1,128 mAh·g-1,76 mAh·g-1和92 mAh·g-1.由实验结果可以看出Mg掺入过少(x=0.01)和过多(x=0.10)对材料的电化学性能没有明显改善,合适比例Mg的掺入才能有效提高材料的电化学性能.其中 x=0.03的样品的放电容量最高,循环性能最好,其放电容量最高达128 mAh·g-1,循环100次后仍保持在72 mAh·g-1(见图3中的B),这说明适量的Mg的掺入确实有效提高了材料的电化学性能,这可能是因为Mg2+与Li+电负性相近,更有助于Mg2+掺入LiMnPO4晶格中,这种体相掺杂增加了晶格的无序化程度,引起了材料的缺陷,易于Li+的嵌入与脱出.
为探究Mg掺入对材料的影响,作者对起始组成为 x=0和 x=0.03的两样品与锂片组装的电池在充放电测试前的阻抗进行测试,结果如图4中的A所示.由该图可见交流阻抗图谱由两部分组成,高频区的半圆对应于电荷传输阻抗和钝化膜阻抗,低频段的斜线是由锂离子在电极中的扩散引起的.由图4A还可以看出,掺杂适量的Mg之后所得的Li0.94Mg0.03MnPO4/C样品的阻抗明显降低,这可能是由于Mg进入晶格后占据锂离子的位置,更有利于锂离子的扩散所致,因此Li0.94Mg0.03MnPO4/C材料在充放电过程中极化程度比较小,比容量比较高,循环性能也更好.图4中的B为以Li0.94Mg0.03MnPO4/C为正极材料组装的电池随着循环的进行阻抗的变化图,由图可以看出随着循环的进行阻抗明显增大,这可能是因为随着循环的进行正负极上SEI膜的厚度不断增加,使得两极的阻抗增加,因此电池的阻抗随着循环次数的增大而增加,导致电池的循环容量衰减.
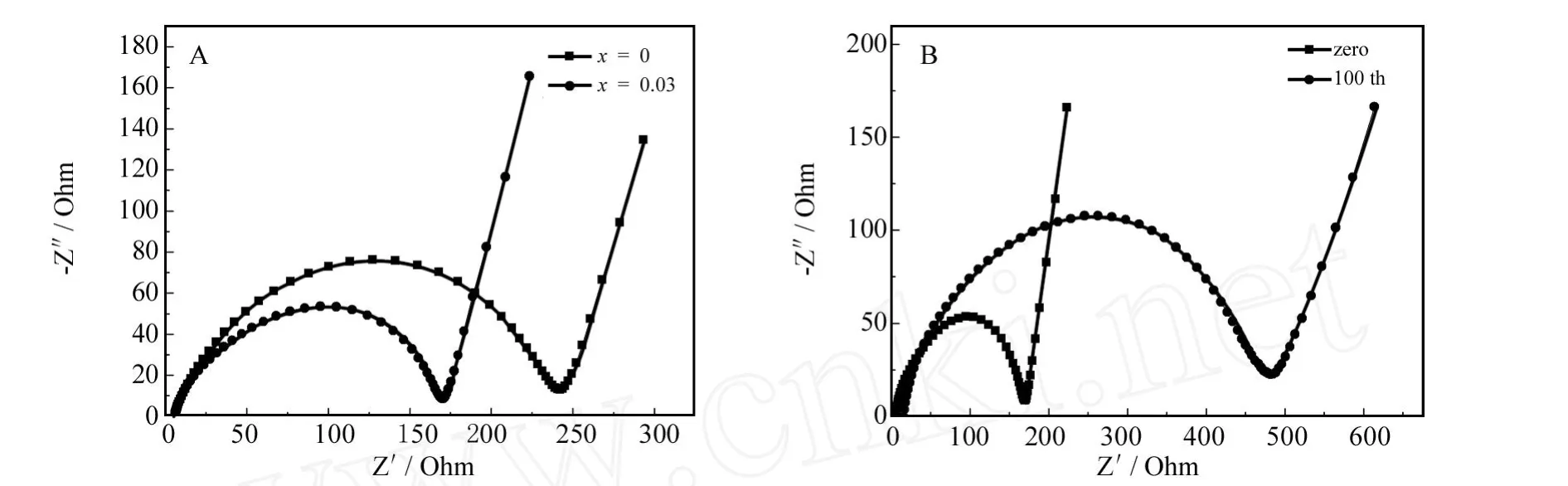
图4 Li(1-2x)MgxMnPO4/C样品的交流阻抗谱图Fig.4 EIS plots of Li(1-2x)MgxMnPO4/C
图5为在空气气氛中400℃焙烧得到的Li0.94Mg0.03MnPO4/C样品在不同放电倍率下的循环性能图.由该图可以看出,在不同的放电倍率下材料均表现出良好的循环性能,随着放电倍率的提高,电化学极化程度加剧,可逆的放电容量也在下降,在1/40 C,1/20 C,1/10 C下的最大放电比容量分别为84 mAh·g-1、83 mAh·g-1和71 mAh·g-1.但由图5可以看出材料在高倍率下的可逆放电容量还不是很高,如在2 C放电倍率下放电容量为20 mAh·g-1,仅为理论容量的12%,因此材料的电化学性能还有待提高.如进一步改善溶胶凝胶法合成的条件,进一步优化凝胶化处理过程并使产品颗粒更为细小均匀,则有望进一步提高Li(1-2x)MgxMnPO4/C材料的电化学性能.
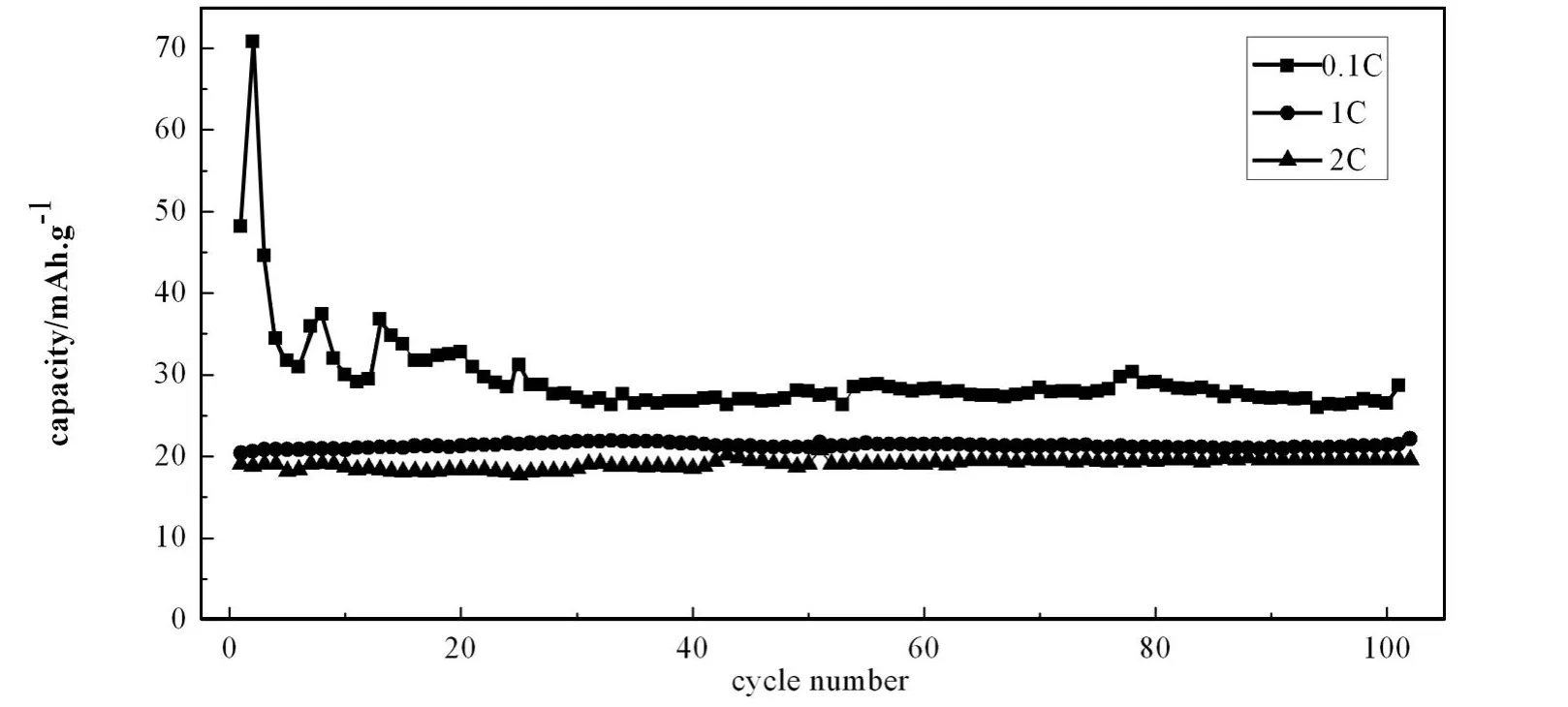
图5 Li0.94Mg0.03MnPO4/C样品的倍率循环性能图Fig.5 Cycling performance of Li0.94Mg0.03MnPO4/C at different C rate
3 结论
采用溶胶-凝胶法空气气氛中分别在400℃、500℃和600℃焙烧得到了橄榄石结构的锂离子电池正极材料Li(1-2x)MgxMnPO4/C(0≤x≤0.1),通过Mg掺杂来改善材料的电化学性能.恒流充放电测试结果表明Mg的加入确实改善了材料的电化学性能,其中空气气氛中400℃焙烧得到的起始组成为x=0.03的样品电化学性能最好,在2.8~4.4 V的范围内,在0.02 C下的放电容量达到了128 mAh·g-1,经过100次循环后容量扔保持在72 mAh·g-1,但样品在高倍率放电时的容量还有待提高.
[1]PADHI A K,NAJUNDASWAMY K S,GOODENOUGH J B.Phospho-olivines as positive materials for rechargeable lithium batteries[J].Electrochem Soc,1997,144(4):1188-1194.
[2]YAMADA A,HOSOYA M,CHUNG C S,et al.Olivine-type cathodes achievements and problems[J].J Power Sources,2003(119/121):232-238.
[3]LI Guo Hua,AZUMA H,TOHDA M.LiMnPO4as the cathode for lithium batteries[J].Electrochem Soc,2002,5(6):135-137.
[4]THIERRY D,KWON N H,BOWEN P,et al.Effect of particle size on LiMnPO4cathodes[J].J Power Sources,2007,174(2):949-953.
[5]BRAMNIK N N,HELMUT E.Precursor-based synthesis and electrochemical performance of LiMnPO4[J].J Alloys Comp,2008,464(1):259-264.
[6]DELACOURT C,POIZOT P,MORCRETTE M.One step low-temperature route for the preparation of electrochemically active LiMnPO4powder[J].Chem Mater,2004,16(1):93-99.
[7]BAKENOV Z,TANIGUCHI I.Electrochemical performance of nanocomposite LiMnPO4/C cathode materials for lithium batteries[J].Electrochem Commun,2010,12(1):75-78.
[8]WANG De Yu,BUQA H,CROUZET M,et al.High-performance,nano-structured LiMnPO4synthesizedviaa polyol method[J].J Power Sources,2009,189(1):624-628.
[9]NAM L D,ZHUMABAYB,IZUMI T.Preparation of carbon coated LiMnPO4powders by combination of spray pyrolysis with DRAY ball-milling followed by heat treatment[J].Advanced Powder Technol,2010,21(2):187-196.
[10]BAKENOV Z,IZUMI T.Physical and electrochemical properties of LiMnPO4/C composite cathode prepared with different conductive carbons[J].J Power Sources,2010,195(21):7445-7451.
[11]CHUNG S Y,BLOKING J T,CHIANG Y M.Electronically conductive phospho-olivines as lithium storage electrodes[J].Nat Mater,2002(1):123-128.
[12]WANG G X,BEWLAY S L,KONSTANTINOV K,et al.Physical and electrochemical properties of doped lithium iron phosphate electrodes[J].Electrochimica ACTA,2004,50(2/3):443-447.
Synthesis and characterization of cathode material
Li(1-2x)MgxMnPO4/C for lithium ion batteries
ZHAO Yan-yan,ZHANG Yu-rong*
(College of Chemistry and Chemical Engineering,Fuzhou University,Fuzhou350108,Fujian,China)
TB 332
A
1008-1011(2011)01-0017-05
2010-09-02.
福建省自然科学基金计划资助项目(2008JO2009);福州大学科技发展基金资助项目(2006-XQ-07).
赵艳艳(1985-),女,硕士生,研究方向为固体无机材料.*
.
