茵连痛风颗粒的质量标准研究
2011-08-10李新液徐玲玲上海中医药大学附属岳阳中西医结合医院药剂科上海市200437
李新液,徐玲玲,徐 熠,年 华(上海中医药大学附属岳阳中西医结合医院药剂科,上海市 200437)
茵连痛风颗粒为上海中医药大学附属岳阳中西医结合医院的自制复方制剂,由茵陈、连钱草、伸筋草组成,具有清热、利湿、通络的功效。用于治疗慢性痛风、关节炎,几十年的临床应用显示,疗效显著。处方中所含绿原酸、阿魏酸等成分对慢性关节炎具有一定的治疗效果[1]。为了有效控制该制剂的品质,有必要对茵连痛风颗粒的质量标准进行进一步的研究探讨。故本试验采用薄层色谱(TLC)法对组成药物进行定性鉴别;采用紫外分光光度法对处方中的主要成分总香豆素和总黄酮的含量进行测定,以期能有效控制制剂质量。
1 仪器与试药
UV-2450紫外-可见分光光度计(日本岛津公司);80-1离心机(上海手术器械厂);BransonB5200S-DT超声提取器(必能信超声(上海)有限公司);HHS电热数字显示恒温水浴锅(上海浦东荣丰科学仪器有限公司)。
芦丁、阿魏酸、滨蒿内酯对照品和连线草、茵陈对照药材(中国药品生物制品检定所,批号分别为0080-9705、0773-9910、1511-200001、121109-200401、950-200204);茵陈、连钱草、伸筋草药材均购自上海康桥中药饮片有限公司,由上海中药质量监督检验室叶愈青副主任药师鉴定为真品;茵连痛风颗粒(上海中医药大学附属岳阳中西医结合医院药剂科制 剂 室 ,批 号 :081001、081101、090722、090901、091001、091101、100401、100501、100601);三氯化铝、氢氧化钠、亚硝酸钠、甲醇、乙醇等试剂均为分析纯。
2 方法与结果
2.1 定性鉴别
2.1.1 茵陈的TLC鉴别 取茵连痛风颗粒10 g,研细,加乙醇20 mL,水浴加热回流30 min,放冷,滤过,滤液蒸干,残渣加水10 mL使溶解,用醋酸乙酯振摇萃取2次,每次20 mL,合并醋酸乙酯液,蒸干,残渣加乙醇1 mL使溶解,作为供试品溶液;将除茵陈外的所有药材按处方比例制成阴性样品,同法制成阴性对照溶液;另取茵陈对照药材5 g,加水50 mL,煎煮1 h,放冷,滤过,滤液用醋酸乙酯振摇萃取2次,每次20 mL,合并醋酸乙酯液,蒸干,残渣加乙醇1 mL使溶解,作为对照药材溶液。照TLC法[2]试验,吸取上述溶液各5 μL,分别点于同一聚酰胺薄膜上,以醋酸为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与对照药材色谱相应位置上,显相同颜色的荧光斑点;阴性对照无干扰。茵陈的TLC见图1。
2.1.2 连钱草的TLC鉴别 取本品粉末5 g,加70%甲醇50 mL,加热回流1 h,滤过,滤液蒸干,残渣用石油醚(30~60℃)5 mL浸渍3 min,弃去石油醚,挥干,残渣加甲醇2 mL使溶解,作为供试品溶液;另取不含连钱草的各处方药材,按组方比例制成阴性样品,同法制成阴性对照溶液;另取连钱草对照药材2.5 g,同法制成对照药材溶液。照TLC法[2]试验,吸取上述溶液各2 μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-甲酸(8∶9∶0.5)为展开剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液,于105℃加热数分钟,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点;阴性对照无干扰。连钱草的TLC见图2。
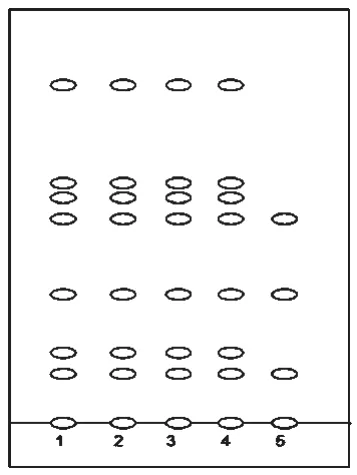
图1 茵陈的TLC1.茵陈对照药材;2~4.供试品(批号:100401、100501、100601);5.缺茵陈阴性样品Fig1 TLC of Artemisiae Scopariae Herba1.Artemisiae Scopariae Herba reference substance;2~4.test samples (batch number: 100401,100501,100601);5.negative sample without Artemisiae Scopariae Herba
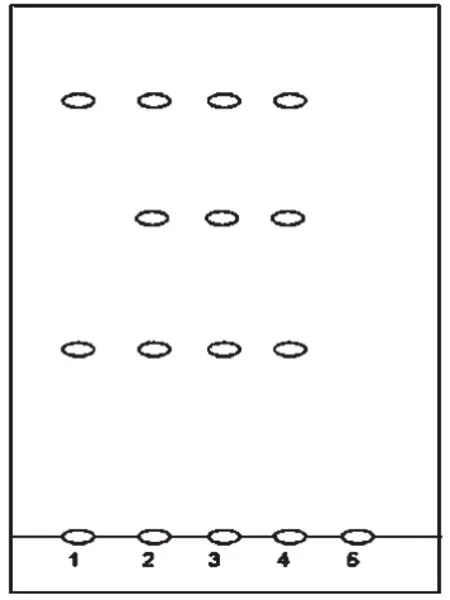
图2 连钱草的TLC1.连钱草对照药材;2~4.供试品(批号:100401、100501、100601);5.缺连钱草阴性样品Fig2 TLC of Glechoma longituba1.Glechomae Herba reference substance;2~4.test samples(batch number:100401,100501,100601);5.negative sample without G.longituba
2.1.3 伸筋草的TLC鉴别 取茵连痛风颗粒3 g,加10 mL蒸馏水使溶解,用醋酸乙酯-甲酸(9.5∶0.5)振摇提取2次,每次20 mL,合并提取液,蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液;另取缺伸筋草的所有药材按处方比例制成阴性样品,同法制成阴性对照溶液;另取阿魏酸对照品,加甲醇制成每1 mL含1 mg的对照品溶液。照TLC法[2]试验,吸取上述溶液各5 μL,分别点于同一硅胶G薄层板上,以苯-醋酸乙酯-甲酸(8∶2∶0.2)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点;阴性对照无干扰。伸筋草的TLC见图3。
2.2 总香豆素的含量测定
2.2.1 供试品溶液的制备 精密称取茵连痛风颗粒2.5 g,加70%乙醇15 mL,回流提取0.5 h,滤过,静置2 h,取上清液1 mL,稀释125倍,精密量取5 mL,置25 mL量瓶中,加70%乙醇至刻度,摇匀,即得。
2.2.2 对照品溶液的制备 精密称取经五氧化二磷减压干燥24 h的滨蒿内酯对照品适量,加70%乙醇制成每1 mL含0.067 mg的溶液,作为对照品溶液。
2.2.3 测定波长的考察 取滨蒿内酯对照品溶液、供试品溶液各适量,于200~600 nm波长范围内进行扫描,结果对照品和供试品溶液均在345 nm波长左右有最大吸收,且相互无干扰,故选用345 nm作为检测波长。紫外吸收光谱见图4。
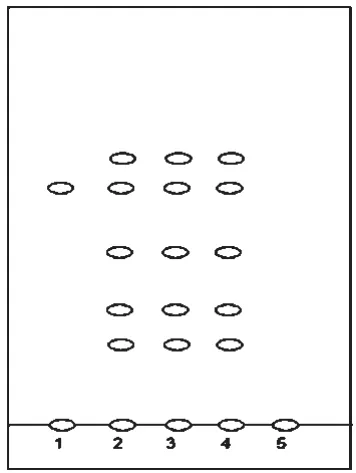
图3 伸筋草的TLC1.阿魏酸对照品;2~4.供试品(批号:100401、100501、100601);5.缺伸筋草阴性样品Fig3 TLC of Lycopodium japonicum1.ferulic acid control;2~4.test samples(batch number:100401,100501,100601);5.negative sample without L.japonicum
2.2.4 线性关系考察 分别精密量取对照品溶液1.0、2.0、3.0、4.0、5.0、6.0 mL,置25 mL容量瓶中,加70%乙醇至刻度,摇匀。以70%乙醇作为空白对照。以滨蒿内酯检测浓度(X)为横坐标,吸光度(Y)为纵坐标,制备标准曲线,得回归方程为Y=0.058X-0.002(r=0.999 9,n=6)。结果表明,滨蒿内酯检测浓度在2.68~21.44 μg·mL-1范围内与吸光度呈良好的线性关系。
2.2.5 稳定性试验 取供试品溶液适量,分别于0、0.5、1.0、2.0、3.0、4.0 h测定吸光度。结果,RSD=1.14%(n=6),表明在4 h内供试品溶液较稳定。
2.2.6 精密度试验 精密吸取同一对照品溶液,在345 nm波长处重复测定6次。结果,RSD=0.24%(n=6),表明仪器精密度良好。
2.2.7 重复性试验 取同一批茵连痛风颗粒适量,研细,取6份,按“2.2.1”项下方法制备供试品溶液,分别在345 nm波长处测定吸光度。结果,RSD=1.61%(n=6),表明方法重复性良好。
2.2.8 加样回收率试验 取已知含量的样品适量,共9份,精密称定,各精密加入样品含量80%、100%、120%的滨蒿内酯对照品,按供试品溶液的制备方法制备,分别测定吸光度,计算加样回收率,结果见表1。
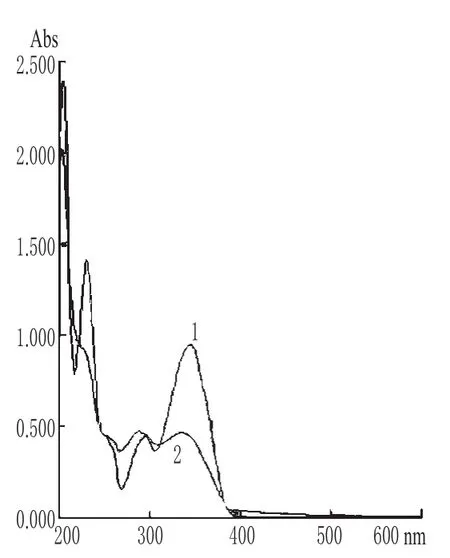
图4 紫外吸收光谱(Ⅰ)1.滨蒿内酯对照品;2.茵连痛风颗粒Fig4 UV absorbance spectrum(Ⅰ)1.escoparone control;2.Yinlian tongfeng granules
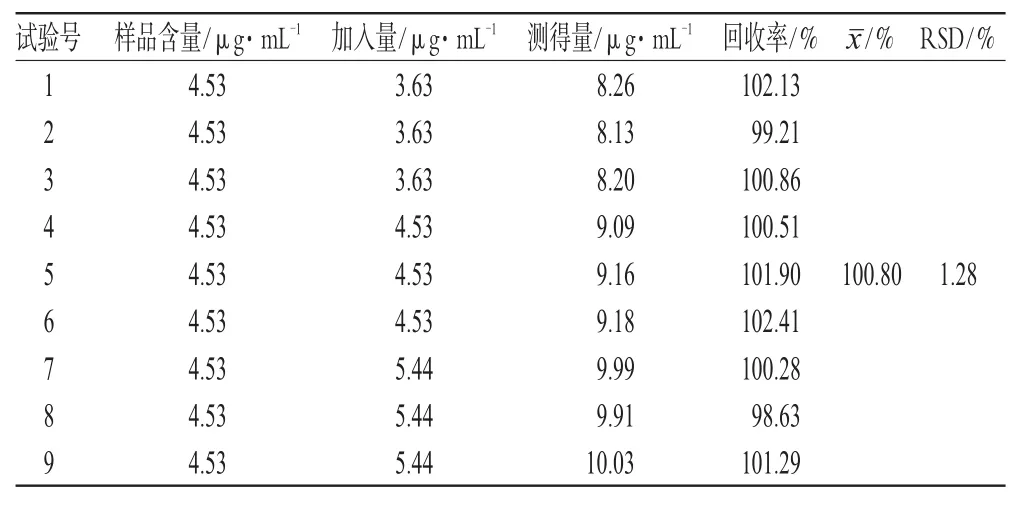
表1 加样回收率试验结果(n=9)Tab 1Results of recovery test(n=9)
2.2.9 样品含量测定 取5批茵连痛风颗粒适量,按“2.2.1”项下方法制备供试品溶液,分别在345 nm波长处测定吸光度,计算总香豆素含量,结果见表2。
2.3 总黄酮的含量测定
2.3.1 供试品溶液的制备 精密称取茵连痛风颗粒1 g,置三角烧瓶中,加20 mL水溶解,加入95%乙醇34 mL,静置2 h,离心,取上清液,即得。
2.3.2 对照品溶液的制备 精密称取120℃干燥至恒重的芦丁对照品10.40 mg,置50 mL容量瓶中,加甲醇15 mL,超声20 min使其溶解,放冷,加甲醇至刻度,即得。
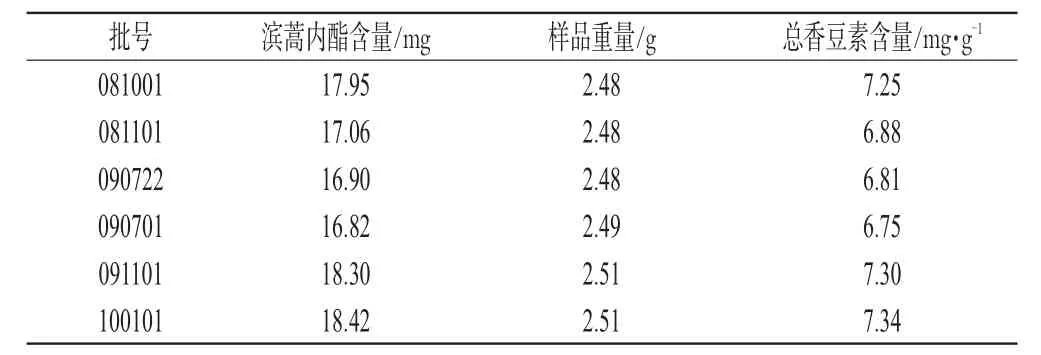
表2 总香豆素的含量测定结果(n=3)Tab2 Results of content determination of total coumarin(n=3)
2.3.3 测定波长的考察 取芦丁对照品溶液、供试品溶液各适量,于200~600 nm波长范围内进行扫描。结果,对照品和供试品溶液均在513 nm波长左右有最大吸收,且相互无干扰,故选用513 nm作为检测波长。紫外吸收光谱见图5。
2.3.4 线性关系考察 分别精密量取对照品溶液0、1.0、2.0、3.0、4.0、5.0、6.0 mL,置20 mL容量瓶中,分别加 6.0、5.0、4.0、3.0、2.0、1.0、0 mL蒸馏水,再各加入5%亚硝酸钠溶液1 mL,放置6 min后加三氯化铝试液1 mL,放 置 6 min,再 加10%氢氧化钠溶液10 mL,定容,放置15 min,以第一管作为空白组,在513 nm波长处测定吸光度。以芦丁检测浓度(X)为横坐标,吸光度(Y)为纵坐标,制备标准曲线,得回归方程为Y=0.008 791X+0.005 8(r=0.999 3)。结果表明,芦丁检测浓度在10~60 μg·mL-1范围内与吸光度呈良好的线性关系。
2.3.5 稳定性试验 精密量取供试品溶液适量,按“2.3.4”项下方法,显色15 min后每隔5 min测定其吸光度。结果,RSD=0.47%(n=8),表明显色后在45 min内基本稳定。
2.3.6 精密度试验 精密吸取对照品溶液4.0 mL,按“2.3.4”项下方法操作并重复测定5次。结果,平均吸光度为0.361,RSD=0.58%(n=5),表明仪器精密度良好。
2.3.7 重复性试验 精密量取同一批次茵连痛风颗粒适量,共6份,按“2.3.1”项下方法制备供试品溶液,照“2.3.4”项下方法操作并测定吸光度。结果,RSD=0.38%(n=6),表明该方法重复性良好。
2.3.8 加样回收率试验 称取已知含量的茵连痛风颗粒样品适量,精密称定,按“2.3.1”项下方法制备供试品溶液,各取9份供试品溶液1 mL,置20 mL容量瓶中,分别加入高、中、低浓度的芦丁对照品溶液各3份,照“2.3.4”项下方法测定吸光度,并测定加样回收率,结果见表3。
2.3.9 样品含量测定 精密称取不同批次的茵连痛风颗粒适量,共5份,精密称定,按“2.3.1”项下方法制备供试品溶液,照“2.3.4”项下方法测定吸光度,计算总黄酮含量,结果见表4。

图5 紫外吸收光谱(Ⅱ)1.芦丁对照品;2.茵连痛风颗粒(显色);3.茵连痛风颗粒(未显色)Fig5 UV absorbance spectrum(Ⅱ)1.rutin control;2.Yinlian tongfeng granules(coloration);3.Yinlian tongfeng granules(non-coloration)
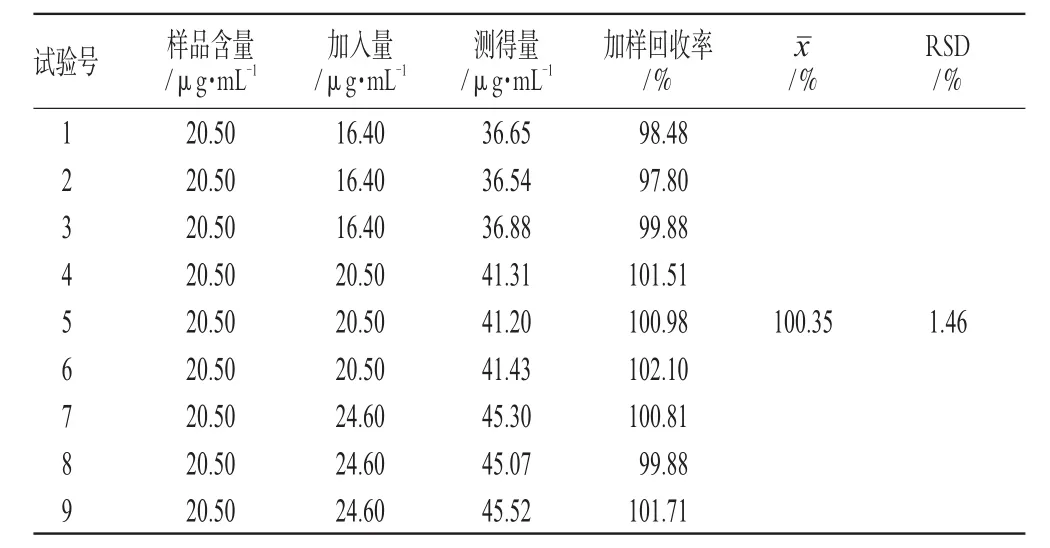
表3 加样回收率试验结果(n=9)Tab3 Results of recovery tests(n=9)
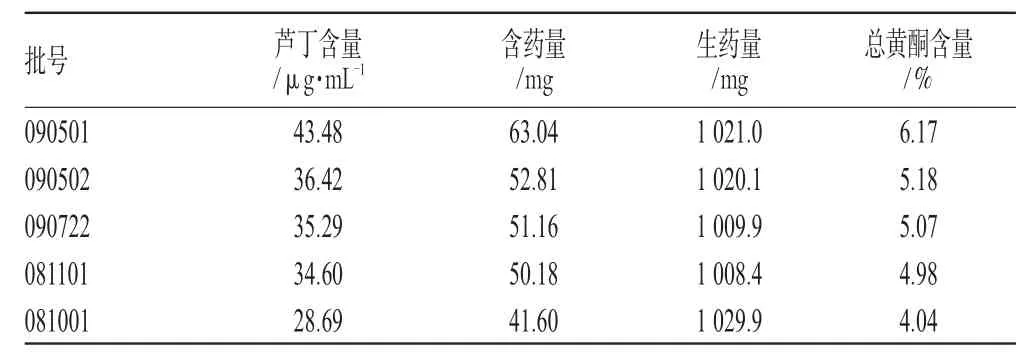
表4 总黄酮含量测定结果(n=3)Tab4 Results of content determination of total flavonoids(n=3)
3 讨论
本试验采用专属性较强的TLC法对处方各药味进行定性鉴别,采用紫外分光光度法对主要成分进行含量测定,可以有效地保证该制剂用药的有效性及可靠性。
方中总香豆素具有一定的利尿抗炎[3]、抗氧化[4]的作用;黄酮类成分具有抗菌、抗炎、抗肝脏毒性、降压等生物活性[5,6]。故对其进行含量测定,可以快速、简便、有效地对痛风颗粒中的抗炎成分进行质量控制,从而保证制剂疗效,达到质量控制标准。
在总香豆素含量测定试验中,分别考察了30%、50%、70%和95%乙醇含量对试验的影响。结果显示,70%乙醇的提取效果较优。再对提取时间进行考察,结果显示,0.5 h的回流时间提取的总香豆素含量较高。
在总黄酮含量测定试验中,曾对显色剂中的氢氧化钠加入量进行考察。结果表明,加入10 mL氢氧化钠溶液进行显色的效果较好,且在45 min内具有良好的显色效果。茵连痛风颗粒不同批次间的最高和最低含量相差倍数为2.07倍,故建议在控制制剂质量时,测定其投料总黄酮含量。
[1]徐 熠,徐玲玲.中医药治疗痛风的研究进展[J].中国药房,2010,21(23):2 195.
[2]国家药典委员会编.中华人民共和国药典[S].2010年版.北京:中国医药科技出版社,2010:附录34.
[3]中华本草编委会.中华本草[M].上海:上海科学技术出版社,1999:6 732-6 733.
[4]王 倩,王 丰,薛 松,等.茵陈中7-甲氧基香豆素的分离与含量测定[J].沈阳药科大学学报,2003,20(1):12.
[5]祝德秋,罗启剑,崔 岚,等.连钱草-小蓟混合粉中总黄酮的含量测定[J].华西药学杂志,2003,18(6):477.
[6]徐国钧.中国药材学[M].北京:中国医药科技出版社,2000:31.
