脊髓炎性脱髓鞘病疼痛症状的病因分析及治疗对策
2011-08-09石磊阎桂琴宋建聪周衡
石磊,阎桂琴,宋建聪,周衡
脊髓炎性脱髓鞘病属于中枢神经系统免疫性疾病的范畴,即自身免疫介导的脊髓炎。感染后免疫反应紊乱而非感染源的直接作用似乎是决定性因素。其病理改变为脊髓内传导束脱髓鞘或坏死。据相关报道,对于各种脊髓损伤,疼痛综合征是继运动功能障碍、性功能障碍之后居第3位影响患者生活质量的因素[1]。疼痛可以加重患者痛苦,降低生活质量,延缓康复进程。
1 资料与方法
1.1 一般资料 首都医科大学附属北京天坛医院神经内科于2000年1月~2010年12月收治的伴有疼痛的脊髓炎性脱髓鞘病患者271例,占同期住院治疗的脊髓炎性脱髓鞘病患者的62.0%。其中男性65例(24.0%),女性206例(76.0%);年龄14~50岁,平均29.1岁;病程2周~1年;首次发病233例,复发38例;急性起病229例,亚急性起病42例;肢体无力268例,感觉障碍259例,二便障碍204例。本组患者均行脊髓MRI检查,其中253例行脊髓增强扫描检查,其中颈段207例(76.4%),胸段49例(18.1%),腰段9例(3.3%),颈胸交界区6例(2.2%);单个病灶239例(88.2%),2个以上病灶32例(11.8%),存在增强病灶者187例(69.0%)。
1.2 疼痛情况 在本组患者中,Lhermitte征和神经根痛的发生率较高,有74例患者(27.3%)存在2种以上疼痛类型。见表1。
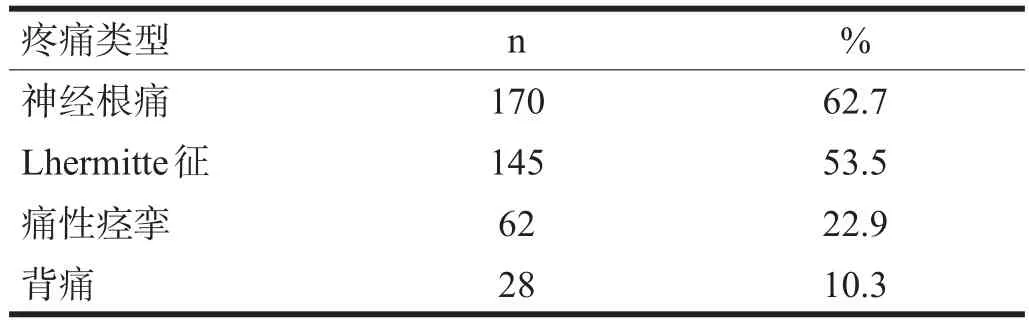
表1 脊髓炎性脱髓鞘病患者疼痛分类
所有患者在开始治疗的前1 d依据视觉模拟评分(visual analogue scale,VAS)进行疼痛评定,其中轻度疼痛(VAS 1~3分)52例(19.2%)、中度疼痛(VAS 3~7分)186例(68.6%)、重度疼痛(VAS 7~10分)33例(12.2%)。VAS平均(6.5±0.9)分。
1.3 治疗 依据患者疼痛症状的不同类型及程度,我们给予患者具有针对性的治疗方案。
1.3.1 激素 本组患者脊髓炎性脱髓鞘病诊断明确。根据病情差异,并征得患者同意,其中260例患者给予激素治疗,分别给予地塞米松和甲基强的松龙静脉冲击治疗。方案1:地塞米松起始剂量20mg/d,疗程10~14d,之后减至地塞米松10mg/d静脉滴注,1周后改为泼尼松50mg/d顿服,每周递减10mg,直至停药;方案2:甲基强的松龙起始剂量1000mg/d静脉滴注,每3d剂量减半,至甲基强的松龙60mg/d改口服顿服;此后每5 d减12mg,直至停药;方案3:甲基强的松龙起始剂量500mg/d静脉滴注,疗程5 d,之后减至甲基强的松龙60mg/d口服顿服,此后每5 d递减12mg,直至停药。
1.3.2 卡马西平 对痛性痉挛、Lhermitte征的患者给予卡马西平口服,起始剂量100mg,每日2次,无效则逐步增加剂量,最大剂量600mg/d。
1.3.3 巴氯酚 对单用卡马西平疗效不满意或者因出现不良反应不能耐受卡马西平的患者,给予巴氯酚口服,起始剂量5mg,每日2次。无效则逐步增加剂量,最大剂量30mg/d。
1.3.5 非甾体类解热镇痛剂 对于以肩背痛、内脏痛为主要表现的患者,给予非甾体类解热镇痛药物口服,主要包括双氯芬酸钠、布洛芬等。
2 结果
经治疗,228例(84.1%)疼痛症状有不同程度缓解。不同疼痛类型的缓解率见表2。
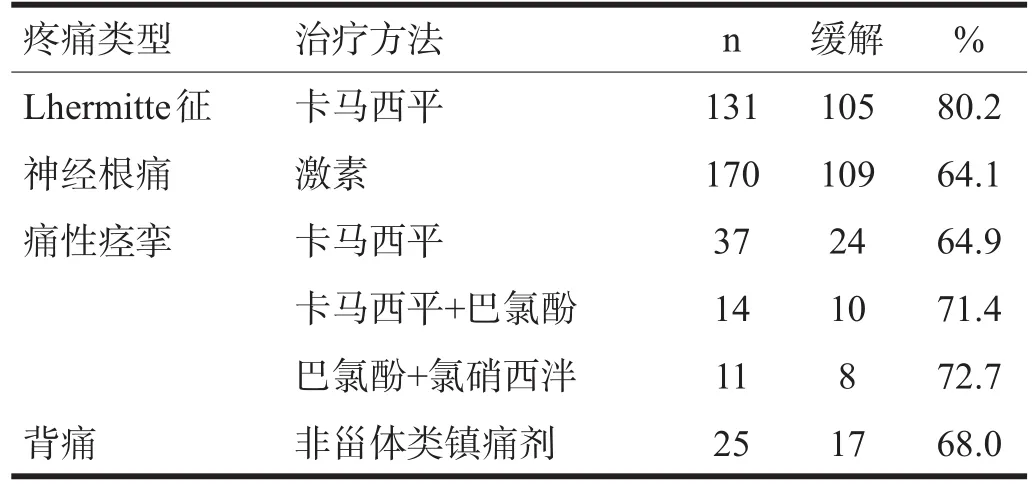
表2 不同疼痛类型的疗效(n)
治疗2周后VAS评分:疼痛完全缓解49例(18.1%),轻度疼痛(VAS 1~3分)137例(50.6%)、中度疼痛(VAS 3~7分)79例(29.2%)、重度疼痛(VAS 7~10分)6例(2.2%)。VAS平均(4.8±0.8)分,与治疗前比较有显著性差异(P<0.05)。
3 讨论
国际疼痛研究协会将疼痛定义为“与现实或潜在组织损伤相关的一种使人不愉快的感觉或情绪体验”。作为外周神经和人脑的联系通路,脊髓本身由多种伤害性刺激引起的疼痛正日益引起人们的重视[2]。经动物模型验证,其发生是一个由细胞、生物化学等多个因素相互作用的结果[3-4]。目前针对脊髓疼痛综合征的发病机制有以下几种解释:①脊髓抑制作用的缺失;②轴索和中继性神经元损伤发出的刺激性信号;③突触的可塑性;④脊髓小胶质细胞活化;⑤脊髓细胞信号传导通路的变化[5]。以上机制均可参与脊髓炎性脱髓鞘病所引发的疼痛综合征,因此本病患者往往出现不同程度、不同性质的疼痛症状[6]。研究表明,相对于没有疼痛症状的患者,疼痛患者往往出现严重的情绪异常。这种情绪异常往往会对患者的康复进程、心理健康及人际关系造成负面影响[7]。许多专业人员正致力于这一专题的研究,并在脊髓损伤疼痛综合征的病因分析及治疗手段等方面取得了进展[8]。
与脊髓炎性脱髓鞘病相关的疼痛综合征主要包括以下几类:①Lhermitte征:被动屈颈时诱发的向肩背放射的电击样疼痛,少数可以放射到臀部;多见于颈段脊髓炎性脱髓鞘病患者,是由于脱髓鞘后的轴索对颈部屈曲造成的颈段脊髓的牵拉和压迫的敏感性增高所致;②急性神经根痛:表现为感觉神经根分布区内的切割样疼痛或伴随叠加性锐性刺痛的钝痛,向远端放射,咳嗽、喷嚏或用力时加重;相应脊髓节段神经元损害和脊髓炎症急性期水肿造成的物理性压迫是引起急性神经根性疼痛的主要原因;③痛性膀胱痉挛:神经原性膀胱可见于多数脊髓炎性脱髓鞘病患者,由于反复泌尿系统感染和逼尿肌反射亢进可以引发膀胱区及下腹部的痛性痉挛[9]。
脊髓炎性脱髓鞘病患者通常会遗留不同程度的神经系统后遗症,表现为肢体无力、关节挛缩、异常步态;在疾病的慢性期,以上后遗症也可以引发特异性相对较小的慢性疼痛,其中最常见的是背部疼痛,多见于长期应用轮椅的患者。痉挛性瘫痪可以造成脊柱旁肌肉异常紧张,进而加快脊柱椎间盘变性和小关节病变。部分患者由于长期应用类固醇药物引发的骨质疏松可以导致椎体压缩性骨折,造成后期神经根刺激性疼痛。
鉴于疼痛对脊髓炎性脱髓鞘病患者多种负面影响,应早期确认疼痛症状的病因,及时给予针对性治疗,并最大可能预防后期疼痛[10]。其治疗应根据患者的病情、基础病变和对药物的耐受性及对治疗的依从性,遵循个体化原则[11]。
目前常用的药物主要有:①卡马西平:作为经典的抗惊厥药物,卡马西平可以应用于治疗痛性痉挛和其他阵发性疼痛。文献报道,卡马西平还可以有效缓解Lhermitte征。常用剂量是300~600mg/d,部分患者用量可以增加到1200~1600mg/d。应用卡马西平期间,应注意观察可能出现的白细胞计数下降及药疹等不良反应。奥卡西平因其安全性较高,可作为卡马西平的替代用药。②巴氯酚:巴氯芬是一种γ-氨酪酸(GABA)衍生物。GABA是神经系统冲动传导的主要抑制剂,通过作用于脊髓的GABA受体,巴氯酚可以有效地抑制神经反射的传递,从而发挥解痉作用。5~120mg/d可减轻肌强直程度和急性痉挛发作的频度与严重性,应缓慢增量直至最大耐受量。副作用有短暂镇静、恶心、情绪抑郁、眩晕和意识模糊,男性患者可能出现小便失禁,严重时可出现抽搐和幻觉,需停药。在与地西泮合用时,巴氯酚的日剂量应控制在6~40mg;对于其疗程,多个研究所的结果均倾向于短疗程,一般在11 d~5周之间。巴氯酚在脊髓水平发挥其抗痉挛作用,因其水溶性较差,所以难以在脑脊液中达到很高的药物浓度,加大口服剂量又可能加重不良反应,因此,巴氯酚鞘内给药成为一种新的治疗方法。由微量泵控制的持续鞘内给药可以维持有效的药物浓度并避免潜在的不良反应。③苯二氮类药物:苯二氮类药物通过抑制肌肉和皮肤感受器的神经冲动发挥降低肌紧张度的作用,同时可以增强GABA的抑制性作用。在与巴氯酚等药物进行的对比研究中,苯二氮类药物的不良反应比较明显,主要是镇静作用和肌无力。曾有患者因不良反应而退出临床研究。④肾上腺皮质激素:甲基强地松龙、地塞米松可以通过抑制炎症过程,缓解组织水肿等机制达到缓解疼痛症状的目的,治疗过程中要注意可能出现的骨质疏松、电解质紊乱、应激性溃疡等不良反应。
疼痛是脊髓炎性脱髓鞘病患者的常见症状。正确认识患者疼痛类型及原因,及时给予相应的个体化治疗,有助于改善患者预后、提高生活质量。
[1]Siddall PJ,McClelland JM,Rutkowski SB,et al.A longitudinal study of the prevalence and characteristics of pain in the first 5 years following spinal cord injury[J].Pain,2003,103:249-257.
[2]D'Mello R,Dickenson AH.Spinal cord mechanisms of pain[J].Br JAnaesth,2008,101(1):8-16.
[3]Yezierski RP.Pain following spinal cord injury pain:Central mechanisms[M].//Cervero F,Jensen TS.Handbook of Clinical Neurology.Vol 81,Pain.Amsterdam(the Netherlands):Elsevier Science Pub Co,2006:293-307.
[4]Nakae A,Nakai K,Yano K,et al.The animal model of spinal cord injury as an experimental pain model[J].J Biomed Biotechnol,2011,7:1-11.
[5]Crown ED,Ye Z,Johnson KM,et al.Increases in the activated forms of ERK 1/2,p38 MAPK,and CREB are correlated with the expression of at-level mechanical allodynia following spinal cord injury[J].Exp Neurol,2006,199(2):397-407.
[6]Vall J,Costa CM,Santos Tde J,et al.Neuropathic pain characteristics in patients from Curitiba(Brazil)with spinal cord injury[J].Arp Neurosiquiatr,2011,69(1):64-68.
[7]Kessler R,Mroczek D.Final version of our psychological distress scale[R].The University of Michigan,Open Research Memorandum,2001.
[8]Webb AA,Ngan S,Fowler JD.Spinal cord injury I:A synopsis of the basic science[J].Can Vet J,2010,51(5):485-492.
[9]Henze T.Managing specific symptoms in people with multiple sclerosis[J].Inter MS J,2005,12:60-68.
[10]Cook CE,Hegedus E,Pietrobon R,et al.A pragmatic neurological screen for patients with suspected cord compressive myelopathy[J].Phys Ther,2007,87(9):123-141.
[11]de Miguel1 M,Kraychete DC.Pain in patients with spinal cord injury[J].Rev BrasAnestesiol,2009,59(3):350-357.
