一次性注射器的生物相容性研究
2011-08-07程玲徐玉茵高勇刘海涛张娟丽周静
程玲,徐玉茵,高勇,2,刘海涛,张娟丽 ,周静
1.河南省医疗器械检验所 生物室,河南 郑州 450003;2.浙江大学生物医学工程与仪器科学学院,浙江 杭州310027
一次性注射器已广泛应用于医疗机构,其质量的好坏与人民群众的生命安全息息相关。一次性使用注射器属于体外与体内相接触中间接与血液接触类器械,作用时间为A类(<24h)[1]。依据GB/T16886.1-2001《医疗器械生物学评价第1部分:评价与试验》[2-3],我们选择了体外细胞毒性试验、急性毒性试验、皮内反应和迟发型超敏反应试验等对其生物相容性进行研究。
1 试验材料
1.1 试验样品
选择17批一次性使用注射器,来源于国家抽验。
1.2 试验仪器和所需材料
采用超净工作台(苏州净化设备有限公司,型号:SW-CJ-1C),二氧化碳培养箱(Thermo公司,型号:3111),小鼠成纤维细胞L-929(购自中国科学院上海生命科学研究院细胞库),酶标仪(Tecan公司,型号:Sunrise RC梯度),MEM/EBSS培养基(赛默飞世尔生物化学制品有限公司),胎牛血清(赛默飞世尔生物化学制品有限公司),胰蛋白酶(Thermo),MTT溶液(Sigma公司),完全弗氏佐剂(Sigma公司),植物油(天津嘉里粮油工业有限公司),雄性豚鼠(河南康达实验动物有限公司,合格证号:0007273),日本大耳白(河南康达实验动物有限公司,合格证号:0002677),昆明种小鼠(郑州大学实验动物中心,合格证:0000909)。
2 试验样品的制备[4]
2.1 细胞毒性试验
同一批号取一次性注射器3支,浸提介质为含10%胎牛血清的RPMI 1640培养液,无菌条件下,抽取细胞培养液至最大刻度线处,置于37℃的CO2培养箱中24h。阳性对照用5%二甲基亚砜(DMSO),阴性对照材料选用高密度聚乙烯,取高密度聚乙烯适量,按0.2g/mL加入含10%胎牛血清的RPMI1640培养基,置于37℃培养箱浸提24 h。
2.2 急性全身毒性试验
浸提介质为0.9%的氯化钠注射液,同一批号取注射器10支,分别加0.9%的氯化钠注射液至公称容量并把芯杆最大容量,两端封闭,置121℃恒温箱中保温1h后取出,把浸提液移入无菌的三角烧瓶内,供24h内使用。同法操作制备植物油浸提液和浸提介质对照液。
2.3 皮内反应试验
浸提介质为0.9%的氯化钠注射液,同一批号取注射器3支,分别加0.9%的氯化钠注射液至公称容量,两端封闭,振摇3次,置121℃恒温箱中保温1h后取出,供2h内使用。同法操作制备植物油浸提液。取对照液0.9%氯化钠和植物油各10mL放于无菌三角瓶中,同上方法放置。
2.4 迟发型超敏反应最大剂量试验
浸提方法同皮内反应试验,皮内诱导阶段试剂的配置,注射弗氏完全佐剂与生理盐水以50:50体积比混合的稳定乳化剂,试验样品液以50:50的体积与稳定乳化剂混合后进行皮内注射。
3 试验方法
3.1 细胞毒性试验[5]
选取17批国家抽验的注射器,取生长旺盛的小鼠成纤维细胞L929,胰蛋白酶消化成细胞悬液后,用RPMI1640培养液调整细胞密度至1×104/mL,以100μL/孔接种于96孔培养板,96孔板边缘孔全部加入无菌PBS200μL,然后置5%CO2培养箱中孵育37℃/24h。空白对照组用RPMI1640培养液交换。阴性对照组用高密度聚乙烯浸提液交换,阳性对照组用5%DMSO浸提液。样品试验组分别用体积分数100%、50%(即按1:1用含细胞培养液稀释)的样品浸提液每孔100μL交换,置于培养箱中继续培养。对试验样品组、阴性对照组、阳性对照组及空白对照组的细胞进行显微检查,48h后每孔加入20μL(5 mg/mL)MTT溶液,继续培养5h,小心吸去孔内液体,每孔加入200μL DMSO,振荡10 min ,用酶标仪主波长570nm ,参考波长630nm处检测吸光度OD值,取6孔平均值。按下列公式计算相对增殖率(relative growth rate,RGR ,RGR =实验组OD值/空白对照组OD 值×100 %) 。根据RGR值,按表1 评分定出材料的毒性级别。

表1 细胞相对增殖度分级标准
3.2 急性全身毒性试验[6]
随机选取5批国家抽验的注射器,选用昆明种小鼠,体重17~20g,随机将小鼠分为样品组和对照组,每组10只,其中,各样品组5只小鼠由尾静脉恒速注射材料浸提液,对照组5只注射生理盐水对照液;另外各组5只由腹腔分别注入植物油浸提液和植物油对照液。注射量均为50mL/kg。于注射后4h、24h、48h和72h 观察小白鼠运动是否减少,观察并记录试验组和对照组动物的一般状态、毒性表现和死亡动物数,在72h时称量动物体重量。
3.3 皮内反应试验[7]
随机选取5批国家抽验的注射器,日本大耳白兔15只,用75%酒精消毒皮肤暴露区域,在每只兔脊柱一侧选10个点,每点间隔2cm,前5个点皮内注射氯化钠样品浸提液,后5个点注射氯化钠对照液。在每只兔的脊柱另一侧注射植物油制备的样品浸提液和植物油对照液,操作步骤同上。每点注射量0.2mL,注射后24h、48h、72h观察注射部位的红斑和水肿的组织反应评分,并记录试验结果。72h评分后,分别将每一试验样品和溶剂对照的全部红斑与水肿记分相加,再除以18〔3(动物数)×3(观察期)×2(记分类型)〕,计算出每一试验样品和每一对应溶剂对照的综合平均记分。
3.4 迟发型超敏反应试验[7]
随机选取5批国家抽验的注射器,每组10只豚鼠;另选5只豚鼠做对照。皮内诱导阶段:每只豚鼠在约2 cm×4 cm剪毛区内注射3排(每排2个注射点),第1排注射0.1mL注射弗氏完全佐剂(FCA)与生理盐水,以50:50体积比混合的稳定乳化剂,第2排注射0.1mL样品浸提液,对照组注射生理盐水,第3排注射0.1mL样品浸提液(对照生理盐水)与稳定乳化剂的等比混悬液。局部诱导阶段:注射1周后,试验区用10%的十二烷基硫酸钠进行预处理,按摩导入皮肤,然后用样品浸提液,将20mm×40mm滤纸片浸透后局部贴敷于每只动物的去毛背部试验区的诱导注射点部位。用封闭式包扎带固定敷贴片,并于(48±2)h后除去包扎带和敷贴片。对照组使用生理盐水同法操作。激发阶段:诱导14 d后,每只以样品浸提液或对照液局部贴敷于诱导阶段未试验部位,封闭式包扎带固定,并于24h除去包扎带和敷贴片。除去包扎带后24 h、48h 观察试验组和对照组动物激发部位皮肤情况。按Magnusson和Kligman皮肤致敏的分级标准对每一激发部位和每一观察时间皮肤红斑和水肿反应进行描述并分级。
3.5 统计学处理
4 结果
4.1 细胞毒性试验
倒置显微镜观察发现,空白对照组及阴性对照组细胞培养24h后,贴壁生长好,细胞呈梭形或不规则三角形;而阳性对照组细胞很少贴壁,大部分细胞成圆形,核固缩、死亡细胞明显增多。有4批细胞毒性较大,其余的细胞毒性都在正常范围之内,试验结果,见表2。
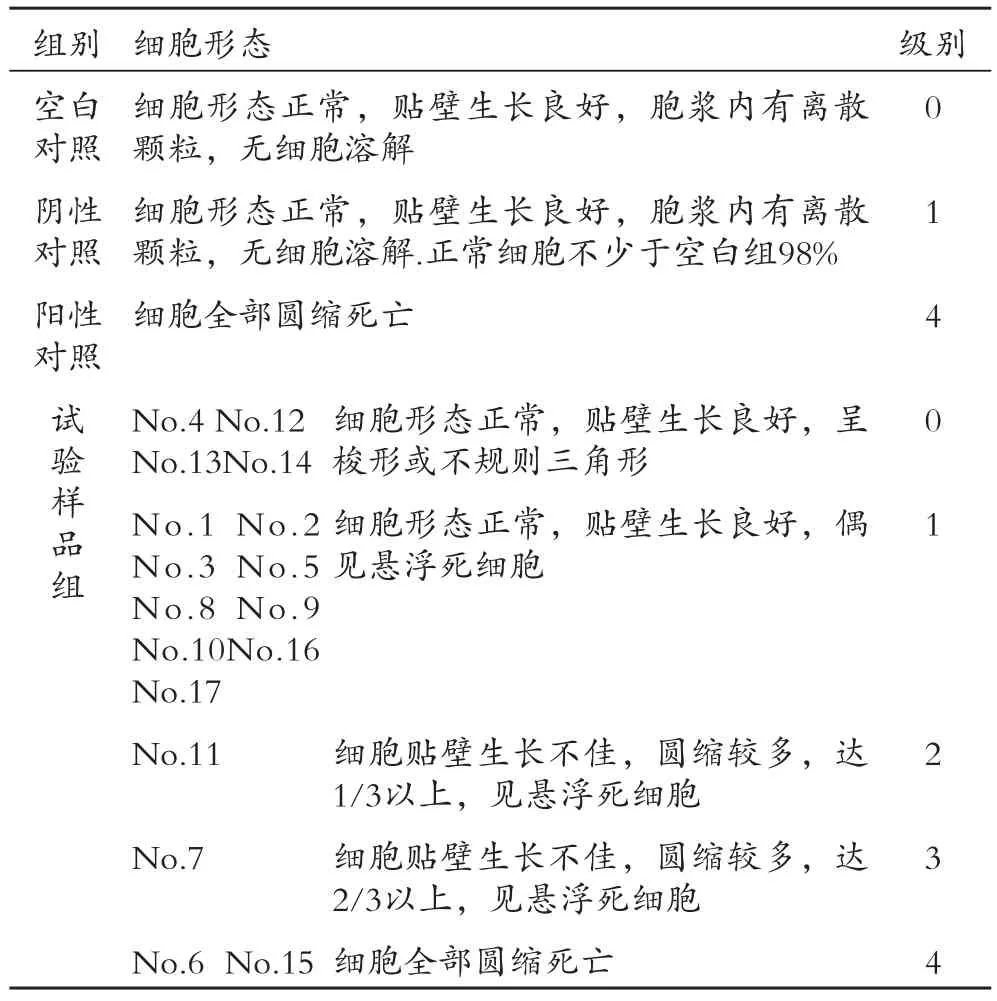
表2 细胞毒性试验结果
4.2 急性全身毒性试验
所有实验小鼠均无死亡,1组4只、2组3只、5组1只动物精神不好,体质量有所减轻,有轻微反应;4组动物整体体质量增长较少;其他动物精神状态良好,活动、进食及大小便均正常,无惊厥、瘫痪、呼吸抑制等毒性反应,体质量均有不同程度的增加,试验结果,见表3。
表3 试验样品对小鼠体质量的影响(±s,g)
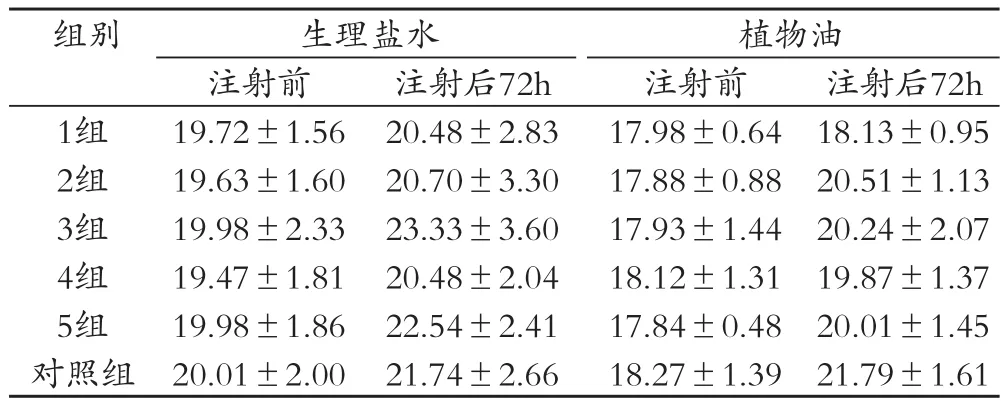
表3 试验样品对小鼠体质量的影响(±s,g)
组别 生理盐水 植物油注射前 注射后72h 注射前 注射后72h 1组 19.72±1.56 20.48±2.83 17.98±0.64 18.13±0.95 2组 19.63±1.60 20.70±3.30 17.88±0.88 20.51±1.13 3组 19.98±2.33 23.33±3.60 17.93±1.44 20.24±2.07 4组 19.47±1.81 20.48±2.04 18.12±1.31 19.87±1.37 5组 19.98±1.86 22.54±2.41 17.84±0.48 20.01±1.45对照组 20.01±2.00 21.74±2.66 18.27±1.39 21.79±1.61
4.3 皮内反应试验
每一试验样品:氯化钠浸提液与氯化钠对照平均记分之差均为0;植物油浸提液与植物油对照平均记分之差也均<1.0(分别为0.3、0.4、0.2、0.3、0.2)。所以在本试验条件下,样品浸提液对皮肤无刺激作用。
4.4 迟发型超敏反应试验
阴性对照组动物记分均为0,试验组动物记分均为0,所以,在本试验条件下,样品浸提液对豚鼠无迟发型致敏作用。
5 讨论
在国家抽验的基础上,本研究采用体外细胞毒性试验和体内试验(急性毒性试验、皮内反应试验和致敏试验)相结合的方法,补充做了一些试验来探究一次性使用注射器的生物相容性。
不少检测机构在检验一次性使用注射器的细胞毒性时,经常会发现送检样品的细胞毒性呈中度或重度,不符合国家标准。据调查分析,注射器细胞毒性不合格的原因可能有以下3方面因素:
(1)目前,一次性使用注射器的原材料主要是聚丙烯(PP),为了降低生产成本,可能会添加质量较差的PP材料。
(2)注射器灭菌的过程中,PP和橡胶活塞经常吸附一定量的环氧乙烷(EO),如果解析时间不够的话,残留的EO就会产生较大的毒性。
(3)在注射器生产过程中,胶塞上使用的硅油不合格,使用工业硅油代替医用硅油,使细胞毒性增加。也有文献[8]研究表明,注射器细胞毒性较大的原因为活塞的洗液残留。建议企业在生产中使用合格的原料,增加EO解析时间,同时改进生产工艺,清除残留洗液。
由于在以往的试验中发现高温对这一类材料有一定影响,所以本次选取注射器在121℃下浸提1h进行试验,虽然致敏试验结果未发现异常,但个别产品的急性毒性试验、皮内反应试验有不同程度的反应,其原因,可能是不同材质高温浸提还是有影响的。建议在注射器的国家标准中增加体外细胞毒性试验和体内相关试验,以较全面地评价产品的质量。
[1]奚廷斐.医疗器械生物学评价[J].中国医疗器械信息,1999,5(3):4-9.
[2]国家药品监督管理局.GB/T16886.1-2001《医疗器械生物学评价第1部分:评价与试验》[S].北京:中国标准出版出,2001.
[3]李彤,等.40株肠球菌应用两种仪器鉴定结果的比较研究[J].中国医疗设备,2009,24(3):55-57.
[4]国家药品监督管理局.GB/T16886.12-2005《医疗器械生物学评价第12部分:样品制备与参照样品》[S].北京:中国标准出版社,2005.
[5]国家药品监督管理局.GB/T14233.2-2005《医用输液、输血、注射器具检验方法第2部分:生物学试验方法》[S].北京:中国标准出版社,2005.
[6]国家药品监督管理局.GB/T16886.11-1997《医疗器械生物学评价第11部分:全身毒性试验》[S].北京:中国标准出版社,1997.
[7]国家药品监督管理局.GB/T16886.10-2005《医疗器械生物学评价第10部分:刺激与迟发型超敏反应试验》[S].北京:中国标准出版社,2005.
[8]何华红,李薇,吴婷.一次性使用医用注射器活塞体外细胞毒性检测[J].中国医疗器械杂志,2010,34(2):123-125.
