全国9家肿瘤专科医院2010年抗肿瘤药利用分析
2011-08-07刘红宁华巩红焦园园张艳华北京大学临床肿瘤学院北京肿瘤医院暨北京市肿瘤防治研究所药剂科恶性肿瘤发病机制及转化研究教育部重点实验室北京市004北京协和医院药剂科北京市00730
刘红,宁华,巩红,焦园园,张艳华#(.北京大学临床肿瘤学院/北京肿瘤医院暨北京市肿瘤防治研究所药剂科/恶性肿瘤发病机制及转化研究教育部重点实验室,北京市 004;.北京协和医院药剂科,北京市00730)
恶性肿瘤已成为严重威胁人类健康的主要疾病。全球2000年新发病例1 010万,死亡病例620万,预计到2020年新发病例将达到2 000万,死亡病例将达到1 200万,成为全球最大的公共卫生问题[1]。肿瘤的治疗是一项综合工程,需要手术、放射、内科治疗等多学科相结合,才能达到提高治愈率和改善患者生活质量的目的。抗肿瘤药因其本身可能引起严重的不良反应,需要合理应用。为了解抗肿瘤药的临床应用情况,笔者对全国9家肿瘤专科医院2010年抗肿瘤药的应用数据进行了统计、分析。
1 资料与方法
1.1 资料来源
资料来源于中国药学会医院药事专业委员会“药学信息利用与评价学组”《医院处方分析》课题项目中全国9家肿瘤专科医院(均为三级甲等医院)2010年抗肿瘤药的应用数据。具体为一年按40 d抽样,每季度抽取10 d,包括2轮周一至周五的抽样数据,并根据各地区床位数及门诊量将抽取数据加权放大到全年。9家肿瘤专科医院包括北京2家,上海2家,广州2家,天津1家,四川1家,浙江1家。
1.2 方法
采用描述性分析研究方法,应用Office Excel2003,对全国9家肿瘤专科医院2010年全年抗肿瘤药应用数据,包括药品通用名、商品名、规格、金额、数量、单次用药剂量及用药频次等进行分类汇总分析。统计2010年抗肿瘤药销售金额和用药频度(DDDs)。限定日剂量(DDD)参考2005年版《中国药典·临床用药须知》[2]、第17版《新编药物学》[3]及药品说明书推荐的成人常用剂量进行确定。DDDs=某药的年消耗量/该药的DDD值。对药品的销售金额和DDDs值进行排序。DDDs越大,说明该药的使用频率越高。
2 结果
2.1 9家医院抗肿瘤药品种数统计
9家医院抗肿瘤药品种数统计见表1。
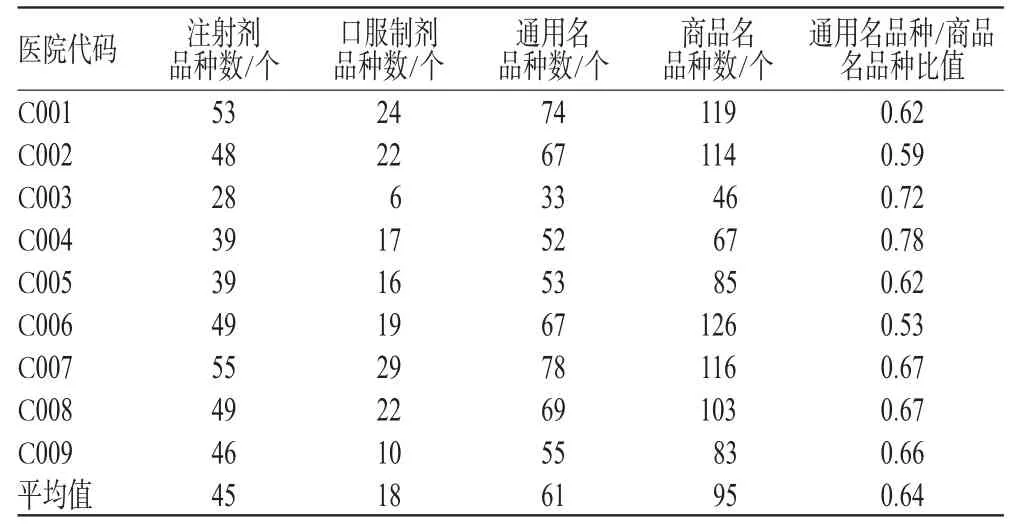
表1 9家医院抗肿瘤药品种统计Tab 1 Com parison of drug categoriesamong 9 cancer hospitals
2.2 9家医院各类抗肿瘤药类别统计
9家医院各类抗肿瘤药类别统计见表2。
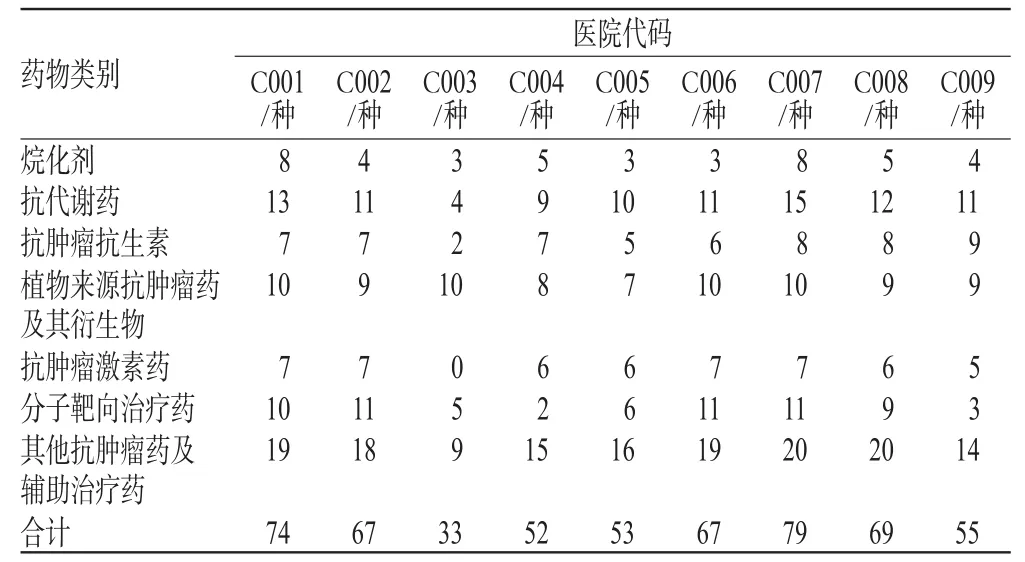
表2 9家医院各类抗肿瘤药类别统计Tab 2 Proportionsof drug types in 9 cancer hospitals
2.3 9家医院注射剂及口服制剂销售金额统计
9家医院注射剂及口服制剂销售金额统计见表3。

表3 9家医院注射剂及口服制剂销售金额统计Tab 3 Com parison of consum ption sum of injections and oralpreparations in 9 cancer hospitals
2.4 9家医院销售金额排序列前20位的药品统计
9家医院销售金额排序列前20位的药品统计见表4。

表4 9家医院销售金额排序列前20位的药品统计Tab 4 Top 20 drugs in the list of consum ption sum in 9 cancer hospitals
2.5 9家医院DDDs排序列前20位的药品统计
9家医院DDDs排序列前20位的药品统计见表5。

表5 9家医院DDDs排序列前20位的药品统计Tab 5 Top 20 drugs in the listof DDDs in 9 cancer hospitals
2.6 用药问题
另外,结合药品说明书,发现用药频次也不合理。用药频次错误统计见表6。
3 讨论
3.1 药物品种数
此次调查共涉及96种抗肿瘤药,其中注射剂68种,口服制剂38种(因注射剂与口服制剂存在相同品种,会有重叠品种,如依托泊苷既有注射剂又有口服制剂,故药品总数小于二者相加之和)。由表1可见,在9家肿瘤专科医院中,注射剂品种数最少28种,最多53种,平均45种;口服制剂品种数最少6种,最多24种,平均18种;通用名品种数最少33种,最多78种,平均61种;商品名品种数最少46种,最多126种,平均95种。有些医院同一药品的生产厂家多达5~6个。通用名品种与商品名品种的比值最高为0.78,说明该院同一通用名药品拥有不同厂家的数量最低,其在保证临床用药的同时,可尽量减少同一药品多种厂家的混乱局面,避免了在调剂、配制以及应用过程中可能出现的错误。
3.2 药物种类
由表2可见,在9家肿瘤专科医院中,应用最多者为其他抗肿瘤药(不包括生物靶向药)及辅助治疗药,其中以铂类药和香菇多糖、重组人白细胞介素-2应用最为广泛。顺铂、卡铂、奥沙利铂、奈达铂在9家医院均有应用。按销售金额排序,铂类药销售情况依次为奥沙利铂、奈达铂、卡铂、顺铂。顺铂作为第1代铂类药,具有抗瘤谱广、易与其他抗肿瘤药配伍等特点,被广泛应用于临床,但其可引起严重的急性恶心呕吐及肾小管损伤、渐进性高音听力损失等,限制了其长期或大剂量应用。第2代铂类药包括卡铂、奈达铂,其生化特征与顺铂相似,但所引起的肾毒性、耳毒性及消化道反应较低。第3代铂类药奥沙利铂的肾毒性最小,但神经毒性较严重。奥沙利铂以其高效、低毒等特点在临床治疗中被广泛应用,因而其销售金额在铂类药中居第1位。香菇多糖和重组人白细胞介素-2在9家医院也均有应用。从药物类别来看,抗代谢药、植物来源抗肿瘤药及其衍生物的用量仅次于前者。抗代谢药中的氟尿嘧啶、吉西他滨、卡培他滨应用最为广泛,在9家医院均有应用。

表6 用药频次错误统计Tab 6 Summery of drug use frequency errors
3.3 药物应用情况
由表4可见,9家医院均应用了紫杉醇和多西他赛,其销售金额分列第1和第2位。紫杉烷类药抗瘤谱广,《美国国立综合癌症网络(NCCN)指南》(2010年版)指出,紫杉醇和多西他赛可用于复发或转移性乳腺癌一线化疗,紫杉醇可用于复发或转移性宫颈癌一线化疗,多西他赛可用于复发或转移性宫颈癌二线化疗,二者还可用于非小细胞肺癌、转移性或局部晚期胃癌、卵巢癌和头颈部肿瘤的治疗。由于紫杉醇普通制剂的助溶剂聚氧乙烯蓖麻油和无水乙醇可加重周围神经毒性,水溶性差,因而研制具有良好水溶性的紫杉醇新制剂一直是研究者关注的热点[4]。此次调查的紫杉醇制剂有3种,包括紫杉醇注射液、紫杉醇脂质体、白蛋白结合型紫杉醇。紫杉醇脂质体具有更好的组织亲和性和更好的缓释与靶向作用,对增加紫杉醇疗效和降低毒性有积极意义[5]。白蛋白结合型紫杉醇是一种新型的紫杉醇制剂,其利用白蛋白结合-释放的剂量,去除了助溶剂聚氧乙烯蓖麻油,能提高紫杉醇的安全剂量。
在销售金额排序列前20位的药物中,有7种属于分子靶向治疗药。近年来,靶向治疗已成为肿瘤治疗新的发展方向。本研究显示,包括北京、上海、广州、天津、四川、浙江等地区,靶向治疗药销售金额均排在前列。酪氨酸激酶抑制剂主要有吉非替尼、厄洛替尼、索拉非尼、舒尼替尼,其中索拉非尼与舒尼替尼为多靶点药;单克隆抗体包括西妥昔单抗、利妥昔单抗、曲妥珠单抗等;新生血管抑制剂有重组人血管内皮抑制素;蛋白酶体抑制剂有硼替佐米。在分子靶向治疗中,有些药物如利妥昔单抗已成为非霍奇金淋巴瘤一线治疗方案药物之一,曲妥珠单抗已成为复发或转移乳腺癌首选化疗方案药物之一,即已成为癌症标准治疗的一部分。虽然靶向治疗还不能完全替代传统治疗,但由于靶向药物的出现,有利于将更多的肿瘤变成慢性疾病,大大提高5年生存率[6],使更多患者受益。
香菇多糖是唯一一个抗肿瘤辅助药,且在9家医院均有应用。香菇多糖是从香菇的子实体中分离得到的具β-1,6支链和β-1,3支链的β-1,3葡聚糖。由于香菇多糖能够刺激和活化T细胞及免疫调节效应器巨噬细胞的诱导和增强作用[7],作为一种良好的免疫增强剂,其在我国已被广泛应用于抗肿瘤治疗,以遏制肿瘤的发展。
由表5可见,他莫昔芬、阿那曲唑、来曲唑的DDDs分列第1~3位;有5种用于乳腺癌的内分泌治疗药位于排名前10位。结合表4,销售金额排名前20位的药品中有9位出现在DDDs排名前20位,说明药品的价格对于药物的选择具有一定作用。如一些单抗类及紫杉类药,由于价格相对较高,限制了其应用。作为抗肿瘤辅助药的应用,医师应同样给予重视,如乌苯美司和香菇多糖的DDDs分列第8和12位,说明它们的应用较为广泛。乌苯美司可增强T细胞的功能,使自然杀伤(NK)细胞的杀伤活力增强,且可使集落刺激因子(CSF)合成增加而刺激骨髓细胞的再生及分化,但要注意用量,不能超过200mg·d-1,否则可致T细胞减少。
3.4 存在的问题
3.4.1 给药频次问题。由于此次调查的是抗肿瘤药,注射剂给药频次一般按其疾病特性以1个化疗周期进行,不宜考察其用药频次,因此只对口服制剂进行了统计。结果发现,在38种口服制剂中,有27种出现用药频次错误(见表6)。如,抗肿瘤激素药依西美坦、阿那曲唑、托瑞米芬的说明书中,明确规定其用法为每日1次(qd),但结果有88份处方中错为每日2次(bid)至每日4次(qid);他莫昔芬的单次用量为10mg或20 mg,bid,而调查发现有260份处方中错为qd、每日3次(tid)至qid的有27例。统计中,含有吉非替尼、厄洛替尼、伊马替尼、索拉非尼、舒尼替尼5种分子靶向治疗药,其中舒尼替尼出现错误的几率最大,有11份处方错误,应为qd而被错为bid,其他几种分子靶向药均出现多于说明书给药频次的处方错误。3.4.2 超剂量用药问题。具体分为以下几种情况:使用剂量超出药品说明书标识剂量但符合国家药典或药学参考书;使用剂量超出药品说明书标识剂量但符合临床实践指南;医师开具的处方剂量与药品说明书标识剂量不符;确实超剂量应用。如,吡柔比星说明书标识用量为7~40mg·m2,《中国药典·临床用药须知》标注剂量为20~50mg·m2,按照后者标准计算,对于体表面积达到2m2者,实际用量则不为超量应用。再如,他莫昔芬单次用量应为10~20mg,而统计结果中记录最大单次用量为140mg;显然是不合格处方,但此处方不一定是依方用药,多数情况是医师为患者开具大处方,加大单次用药剂量所致。有些药物确实为超剂量应用,如香菇多糖说明书及《中国药典·临床用药须知》示单次用量为1~2mg,而实际已用到6mg。
4 结论
总体来看,9家医院中以抗肿瘤激素药、铂类、紫杉烷类药应用最为广泛。近年来,随着肿瘤发病率的逐年增高,全球抗肿瘤药的研发也异常活跃,在研药物种类多样,分子靶向治疗药研发占主导地位,并且已大量应用于临床。在本研究中,发现在抗肿瘤药的应用中,存在给药频次错误及单次用药剂量超过说明书用量问题。药品说明书是指导医师规范用药的依据。药品上市后应不断积累临床资料,如某些药物的特殊剂量用法已广泛应用于临床,并且在相关药学参考书中都已有叙述,则应对原有说明书给予及时补充、修订、完善。建议临床医师在用药时需更加谨慎,处方时应严格按照说明书规定的给药频次,不可随意加减用药次数,否则会增加药物的累积毒性或未达到药品的治疗效果。正确、合理应用抗肿瘤药,减少药品不良反应,不断提高肿瘤患者的疗效、生存质量是我们长期追求的目标。
[1]游伟程.肿瘤的预防——21世纪肿瘤防治研究的焦点[J].北京大学学报(医学版),2005,37(3):229.
[2]国家药典委员会.中华人民共和国药典·临床用药须知[S].2005年版.北京:人民卫生出版社,2005:812.
[3]陈新谦,金有豫,汤 光.新编药物学[M].第17版.北京.人民卫生出版社,2011:721-772.
[4]林本兰,崔 升,沈晓冬.紫杉醇新剂型的研究进展[J].中国现代应用药学杂志,2009,26(3):203.
[5]吴行伟,高洪志,李海燕.注射用紫杉醇脂质体与市售紫杉醇注射液在中国肿瘤患者中的药动学特征比较研究[J].中国药学杂志,2010,45(23):1 851.
[6]孙 燕.分子靶向治疗的不良反应和对策[J].癌症进展杂志,2009,7(4):387.
[7]金 虹.香菇多糖抗肿瘤作用机理及临床应用[J].青海大学学报,2009,27(3):70.
