黄芩苷、黄芩苷磷脂复合物与黄芩苷磷脂复合物鼻用温敏型原位凝胶的鼻黏膜渗透性研究Δ
2011-08-07叶英杰李楠陈祝君向小飞黄亮邹文铨杨明成都中医药大学药学院成都市637四川大学华西药学院成都市6004江西中医学院中药现代制剂教育部重点实验室南昌市330004
叶英杰,李楠,陈祝君,向小飞,黄亮,邹文铨,杨明,3(.成都中医药大学药学院,成都市637;2.四川大学华西药学院,成都市6004;3.江西中医学院中药现代制剂教育部重点实验室,南昌市330004)
黄芩苷属黄酮类化合物,具有多项药理作用,临床应用广泛。由于其具有清除自由基、抗氧化、抗炎、对抗兴奋性氨基酸的神经毒性、保护内皮细胞、抗各种脑水肿及抗缺血再灌注损伤等作用,用于治疗缺血性脑血管疾病已成为临床研究的热点[1]。但因其脂溶性、水溶性差等原因造成体内吸收差、生物利用度低、药效不稳定,从而限制了药效的充分发挥[2]。为了改善这一情况,提高黄芩苷的生物利用度,前人研制了黄芩苷磷脂复合物以改善其理化性质,从而改善体内吸收情况[3]。
鼻腔给药系统是一种新型的给药系统,通过鼻腔给药,药物可绕过血脑屏障而入脑,有望成为静脉注射的替代给药途径。鼻用温敏型原位凝胶(Nasal in-situ gel)能雾化使以溶液状态给药,易于到达鼻黏膜,利用鼻腔特殊的环境温度(32~34℃),使得在鼻腔中及时发生相转变而形成凝胶,黏附于黏膜表面,延长在鼻腔的保留时间,达到缓释长效的目的,且能减少药物流失,增加药物吸收,有利于药物经鼻向脑转运[4~7]。因此,在黄芩苷磷脂复合物的基础上研制了黄芩苷磷脂复合物鼻用温敏型原位凝胶,以扩大临床应用。
Franz扩散池主要应用于体外药物渗透性试验,模拟体内生理情况对药物的膜渗透性进行评价[7]。本文通过体外鼻黏膜渗透性试验比较了黄芩苷磷脂复合物溶液、黄芩苷溶液和3种不同处方的黄芩苷磷脂复合物的鼻用温敏型原位凝胶的鼻黏膜渗透性,确定了黄芩苷磷脂复合物、黄芩苷溶液和黄芩苷磷脂复合物鼻用温敏型凝胶的体外释药曲线,并对黄芩苷磷脂复合物鼻用温敏型凝胶的处方进行了筛选。
1 仪器与材料
1.1 仪器
85-2型数显恒温磁力搅拌器(上海金鹏分析仪器有限公司);FA1104型电子天平(上海精科仪器厂);BP211D型电子天平(北京赛多利斯科学仪器有限公司);TGL-16G型高速离心机(上海安亭科学仪器有限公司);戴安高效液相色谱(HPLC)仪,包括P680四元泵、TCC-100型柱温箱、ASI-100型自动进样器、UVD170U型紫外检测器(戴安中国有限公司);Franz扩散池(笔者自制)。
1.2 试药
黄芩苷对照品(中国药品生物制品检定所,批号:110715-200514);黄芩苷提取物(笔者自制,含量:85%);大豆卵磷脂(成都科龙化工试剂厂,批号:S20020037,含氮量:>99.8%);甘露醇(成都科龙化工试剂厂,批号:000308);PEG6000(广州市化学试剂玻璃仪器批发部,批号:911128);三乙醇胺(成都科龙化工试剂厂,批号:000258);生理盐水(四川科伦药业股份有限公司,批号:060221502);甲醇为色谱纯,水为重蒸馏水,其余试剂均为分析纯。
1.3 动物
猪,♀♂兼用,体重(70±5)kg,由四川省成都市温江区天府镇屠宰场提供。
2 方法与结果
2.1 黄芩苷分析方法的建立[8]
2.1.1 色谱条件与系统适用性试验色谱柱:Kromasil C18(150 mm×4.6 mm,5 μm);流动相:甲醇-水-磷酸(47∶53∶0.2);流速:1.0 mL·min-1;检测波长:280 nm;柱温:40℃;进样量:40 μL。理论板数按黄芩苷峰计算应不低于2000。
2.1.2 检测波长的确定取黄芩苷对照品溶液及供试品溶液,按“2.1.1”项下色谱条件测定,在检测器上进行紫外扫描(200~350 nm)。结果表明,黄芩苷对照品溶液及供试品溶液在280 nm波长处有最大吸收,故选择280 nm作为检测波长。
2.1.3 标准曲线的制备精密称取黄芩苷对照品适量,置于10 mL容量瓶中,用甲醇溶解并定容,得310 μg·mL-1的对照品贮备液。取1 mL置于10 mL量瓶中,用生理盐水稀释至刻度,配制成31 μg·mL-1的对照品溶液,分别进样1、2、4、8、16、32 μL,记录色谱图。以黄芩苷进样量(X)为横坐标,峰面积积分值(Y)为纵坐标,进行线性回归,得回归方程为Y=45.405X+0.0513(r=0.9999)。结果表明,黄芩苷进样量在0.031~0.992 μg范围内与峰面积积分值线性关系良好。
2.1.4 回收率试验按“2.1.3”项下方法操作,制备高、中、低浓度的黄芩苷样品溶液,测定其峰面积,依据外标法计算浓度,测得平均回收率为(100.07±2.6)%,其RSD<2%。
2.1.5 精密度试验按“2.1.3”项下方法操作,选择高、低浓度的黄芩苷溶液,分别于1 d内重复测定5次,得日内RSD均<2%;连续5 d测定,得日间RSD均<2%。
2.2 黄芩苷磷脂复合物的制备
黄芩苷和大豆卵磷脂的投物料比为1∶2(W/W),加入一定体积的四氢呋喃为溶剂,使黄芩苷药物浓度为2.5 mg·mL-1,在55~60℃恒温水浴中以120 r·min-1磁力搅拌1 h,减压回收溶剂,真空干燥,即得黄芩苷磷脂复合物。将制备好的黄芩苷磷脂复合物加入适量的氯仿,充分溶解其中的磷脂及复合物,收集沉淀,干燥,即得黄芩苷磷脂复合物粉末。HPLC法测得复合物中黄芩苷的含量为30%。
2.3 供试品溶液的制备
2.3.1 黄芩苷溶液精密称取黄芩苷0.033 g,于pH 5.8的磷酸盐缓冲溶液中研磨溶解,定容至10 mL,即得。
2.3.2 黄芩苷凝脂复合物溶液精密称取黄芩苷凝脂复合物0.1 g,于pH 5.8的磷酸盐缓冲溶液中研磨溶解,置于10 mL容量瓶中,以pH 7.4磷酸盐缓冲溶液定容至10 mL,3000 r·min-1离心10 min后取上清液,即得。
2.3.3 黄芩苷磷脂复合物鼻用温敏型原位凝胶根据各处方精密称取药物,先将黄芩苷置研钵中,加入适量的三乙醇胺溶液(0.1%)研磨溶解,将溶液转移至西林瓶中,分次用三乙醇胺溶液洗涤,将洗涤液合并至西林瓶中后加入其他辅料。将西林瓶置冰浴4℃磁力搅拌下使其分散均匀,置4℃冰箱中保存24 h,直至聚合物完全溶解得到澄明溶液。
黄芩苷凝胶胶凝温度的测定:将温度计插入装有黄芩苷凝胶的西林瓶中,同时加入搅拌石,开启数显恒温磁力搅拌器,缓慢升温,直到搅拌石不再转动,立即停止,读出温度计上的数字,即为黄芩苷凝胶胶凝温度。选择胶凝温度为30~35℃之间的凝胶进行黏膜渗透试验。黄芩苷凝胶各处方药物含量见表1(加三乙醇胺水溶液至10 g)。

表1 黄芩苷凝胶各处方药物含量Tab 1The drug content of each prescription of baicalin gel
2.4 试验操作与装置[9]
将死亡2 h内的猪鼻部取下,切开鼻腔,暴露出鼻中隔及两侧鼻甲骨,用一个圆头的细玻璃棒及镊子将覆盖在其上的鼻腔薄膜小心剥离,用生理盐水洗净薄膜上残留的血迹,再将薄膜放在一片铝箔上,铺开,立即使用。
本试验采用Franz扩散池法,装置分为两部分,即供给室与接受室,有效扩散面积为3.14 cm2,接受池容积为14 mL。在Franz扩散池接受室内加入电磁搅拌子(长为0.9 cm,宽为0.4 cm)和氯化钠溶液14 mL,并及时排出气泡。将猪鼻黏膜层固定在接受室和供给室之间,置于水浴温度35~37℃、3000 r·min-1的恒温磁力搅拌器上,平衡20 min。用1 mL移液管加入1 mL药液均匀覆盖供给室猪鼻黏膜上,分别于15、30、45、60、90、120、150、180、240、300 min各取样1 mL,每次取样后补足氯化钠溶液1 mL。10000 r·min-1离心5 min后取上清液,作为样品溶液。按“2.1.1”项下色谱条件操作,进样量为40µL。HPLC法测定样品中黄芩苷的浓度,计算单位面积累积渗透量()和稳态透膜速率(Js)。
2.5 统计学方法
根据下列公式计算各个时间点黄芩苷磷脂复合物的μg·cm-2):

式中,V为Franz扩散池接收室的体积(14 mL);A为Franz扩散池有效扩散面积(3.14 cm2);Cn为第n次取样时接受液的浓度;Ci为第i次取样时接受液的浓度;ΣCiVi为取样所损失药量的累积和。
将以上各样品的对渗透时间t进行回归处理,直线斜率即为J(sμg·cm-2·h-1):
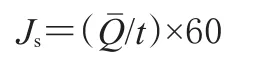
2.6 体外渗透率试验结果
不同时间段的见表2;不同时间段单位面积释药曲线见图1;每种样品Js值(μg·cm-2·h-1)柱形比较见图2。
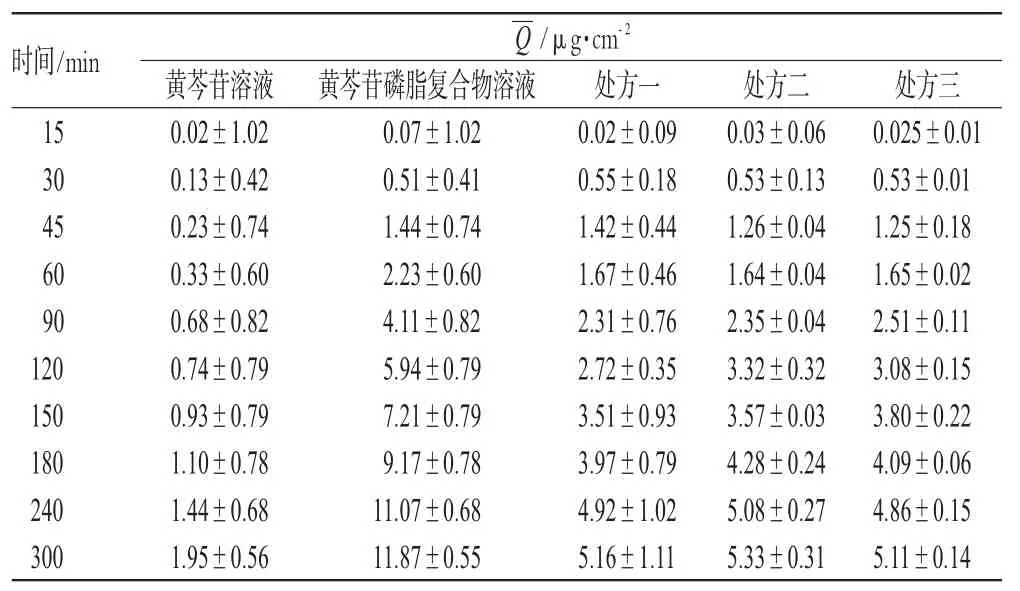
表2 不同时间段的QTab 2Accumulated release amount per unit area in different time
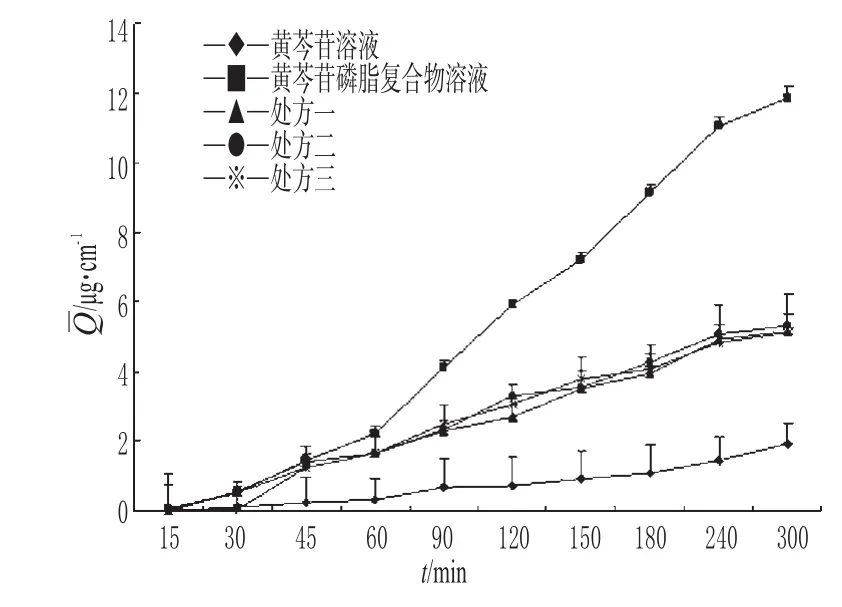
图1 不同时间段单位面积释药曲线Fig 1drug release curves per unit area in different time
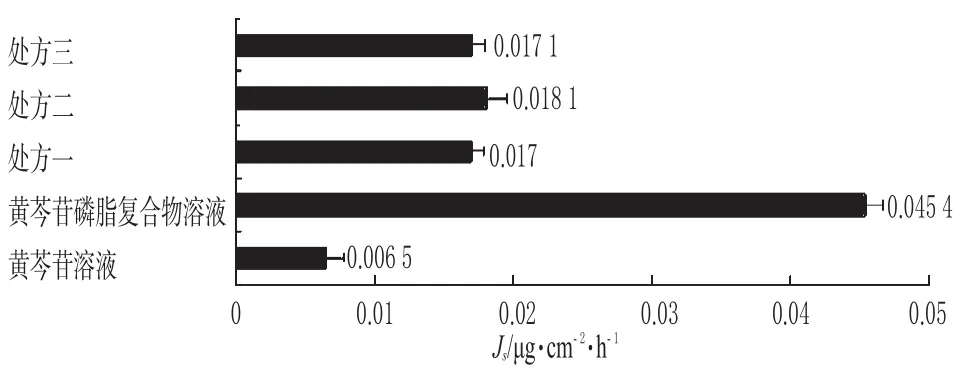
图2 每种样品Js值(μg·cm-2·h-1)柱形比较图Fig 2Column comparison chart of Jsvalue of each sample(μg·cm-2·h-1)
由表2、图1可知,5种被测样品均能透过猪鼻黏膜,且黄芩苷磷脂复合物溶液在每个时间点透过的浓度最高。前15 min每个样品的接受池中均检测不到黄芩苷,证明每个样品在渗透时均有一定的滞留时间。药物的对时间呈良好的线性关系,符合一级动力学方程。最后300 min的为黄芩苷磷脂复合物>处方二>处方一>处方三>黄芩苷溶液。黄芩苷凝胶3个不同的处方在15~90 min时渗透量差异不大,但在90 min后处方二的优势较为明显。由图2可看出,各个样品的Js值大小仍为黄芩苷磷脂复合物>处方二>处方三>处方一>黄芩苷溶液。
3 讨论
在体外透膜或透皮试验过程中,接受液的选择十分重要。为了更确切地描述体内过程,接受液应具有接受透膜或透皮药物的能力,并尽可能地符合类似体内的漏槽条件。常用的接受液有生理盐水、林格氏液和等渗的磷酸盐缓冲液等[10]。本研究前期试验中以主药溶解性能为依据,对生理盐水与pH 5.8、pH 6.5的磷脂缓冲液及加入促渗透剂乙醇、PEG400进行溶解性测定,直接测定黄芩苷在不同接受液中的饱和浓度,最后选择生理盐水为接受液。
有研究发现在采用体外猪鼻黏膜的渗透池扩散试验时,离体的猪鼻黏膜在8 h内可保持生理活性[11,12]。因此,在整个试验过程中可保证所有离体鼻黏膜组织和生理上的完整性避免误差。试验设计各个样品中所含黄芩苷浓度一致,从而可避免药物浓度的差异对渗透过程的干扰。试验中选择嗅区鼻黏膜以尽量模拟体内鼻腔给药形式,因为“鼻-脑”通路主要是通过嗅区黏膜的吸收而直接入脑。
黄芩苷磷脂复合物溶液的和Js都远远高于黄芩苷溶液。黄芩苷制成磷脂复合物后其水溶性和脂溶性都得到极大的改善是造成这一现象的主要原因。因为黄芩苷磷脂复合物在水中溶解量是黄芩苷的4.56倍;在正辛醇中,其溶解量约是黄芩苷的70.17倍。复合物溶液同凝胶剂的比较中,由于凝胶基质会影响药物的释放导致凝胶剂的和Js都低于黄芩苷磷脂复合物溶液。但是,由于溶液剂给药后,患者的吞咽过程会造成药物流失过多且患者顺应性较差;而温敏型凝胶由于鼻腔的温度而发生胶凝形成凝胶黏附于鼻黏膜上,大大减少了药物的损失,同时患者也容易接受,更加适用于鼻腔给药。由黄芩苷凝胶3种处方的试验结果比较可见,处方二的和Js都最高,所以选择处方二为最佳处方。
[1]Lee H,Yang LL,Wang CC,et al.Differential effects of natural polyphenols on neuronal survival in primary cultured central neurons against glutamate and glucose deprivation-induced neuronal death[J].Brain Res,2003,986(103):113.
[2]Wang YY.Advances in research of baicalin absorption and pharmacokinetics[J].Chinese Journal of Current Practical Medicine,2005,4(9):44.
[3]许润春,林彦君,吴品江,等.黄芩苷磷脂复合物理化性质的研究[J].中成药,2008,30(6):934.
[4]Vadnere M,Amidon G,Haslam J,et al.Thennodynamic studies on the gel-sol transition of some pluronic polyols[J].Int J Pharm,1984,23(3):231.
[5]Ricci EJ,Lunardi LO,Nanclares DMA,et al.Sustained release of lidocaine from Poloxamer 407 gels[J].Int J Pharm,2005,288(2):235.
[6]万丽丽,郭澄.中药药动学研究现状和研究方向[J].中国药房,2006,17(8):627.
[7]徐传新,申献玲,王宗喜,等.美洛昔康温敏性水凝胶的处方设计和含量测定[J].药物制剂,2008,27(12):3.
[8]蔡铮,候世祥,宋相容,等.天麻素离子敏感鼻用原位凝胶体外释放研究[J].中国中药杂志,2008,33(7):3.
[9]吴品江,魏萍,林彦君,等.黄芩苷载药体系鼻黏膜渗透性及鼻腔纤毛毒性研究[J].药学学报,2009,44(4):6.
[10]何群,黄海兵,郭建生,等.颈瘤康贴膏剂体外释放、透皮试验研究[J].中成药,2008,30(2):201.
[11]陆彬.药物新剂型与新技术[M].北京:人民卫生出版社,1998:379.
[12]Cecilia Wadell,Erik Bjo¨rk,Ola Camber.Nasal drug delivery-evaluation of an in vitro model using porcine nasal mucosa[J].Eur J Pharm Sci,1999,7(3):197.
