Fenton氧化强化处理经内电解预处理的络合铜废水的研究
2011-08-05刘娉婷兰善红温南兴
刘娉婷 兰善红 温南兴
(东莞理工学院 化学与环境工程学院,广东东莞 523808)
随着印制电路板行业的迅速发展,其生产废水的处理也成为亟待解决的难题。其中以络合铜废水处理难度最大,无法直接采用传统的生物和物化工艺对其进行处理。内电解是一种对印制电路板行业废水有较好处理效果的方法,对络合铜有较高的去除效率,然而内电解出水COD仍较高,达不到排放要求[1-4]。有文献[5]指出,采用Fenton高级氧化法直接处理络合铜废水,可以同时达到较好地破络和显著降COD的效果。但直接采用Fenton试剂进行处理,双氧水和亚铁离子的消耗量大,处理成本高。
本研究采用Fenton氧化法处理内电解法预处理络合铜废水的出水。内电解可为Fenton氧化反应提供亚铁离子,减少Fenton反应的投药量;Fenton氧化法又可弥补内电解的不足,较大程度降低COD,既经济又高效。
1 材料和方法
1.1 主要实验仪器和材料
试验用试剂:硫酸,盐酸,硫酸汞,硫酸银,重铬酸钾,邻菲罗琳,硫酸亚铁铵,盐酸羟铵,乙酸,氢氧化钠,乙酸钠,乙醇,硫酸铝钾,钼酸铵,以上试剂均为分析纯;双氧水 (50%),工业用盐酸 (30%),铁碳烧铸填料 (铁碳比3∶1),铁粉,硝酸 (优级纯)。
仪器及设备:AA6000型原子吸收分光光度计,721/722可见分光光度计,雷磁精密型pH计,CH-02型台式加热器,压差式BOD测定仪,WT603-K1/1000电子天平,内电解+Fenton处理中试装置。
1.2 实验方法
1.2.1 单因素实验方法
影响Fenton氧化反应的因素有双氧水投加量、亚铁投加量、初始pH值、反应时间和温度等。Fenton氧化工艺在工业应用中一般在常温条件下运行,因此本次单因素实验选取双氧水投加量、亚铁投加量、初始pH值和反应时间四个因素进行考察。
1)内电解出水
将络合铜废水调节pH值后充满中试装置中内电解流化床床体,投加适量的铁炭复合填料 (约反应器1/4高度,使用前用废水浸泡24 h,确保活性炭吸附饱和)投加到内电解流化床反应器内,以间歇进水的方式运行反应器获得其30 min出水,测定其COD值以及Fe2+浓度。
2)H2O2/COD质量比
分别取200 mL 1)中的水样置于6个250 mL的锥形瓶中,保持反应条件为:pH=3.0,Fe2+/H2O2质量比为0.2~0.3,H2O2/COD质量比分别设为0.5、1.0、2.0、3.0、4.0、6.0时,搅拌条件下反应90 min,取出反应后水样调节pH至9.0,静置30 min,确保双氧水分解完全,取其上清液测定COD。
3)Fe2+/H2O2质量比
分别取200 mL 1)中水样置于6个250 mL的锥形瓶中,保持双氧水投加量为2)中确定的最佳投加量,初始pH=3.0,保持溶液中Fe2+/H2O2质量比分别为0.2、0.3、0.4、0.5、0.8、1.0,搅拌条件下反应90 min,取出反应后水样调节pH至9.0,静置30 min,取其上清液测定COD。
4)初始pH值
分别取200 mL 1)中水样置于6个250 mL的锥形瓶中,保持双氧水投加量为2)中确定的最佳投加量,亚铁为3)中确定的最佳投加量,搅拌条件下反应90 min,考察反应初始pH分别为2.0~10.0时COD的去除效果。
5)反应时间
取500 mL 1)中水样置于1个500 mL的细口瓶中,保持双氧水投加量为2)中确定的最佳投加量,亚铁为3)中确定的最佳投加量,反应初始pH为4)中确定的最佳值,搅拌条件下反应,分别取反应不同反应时间的样品,调节pH至9.0,静置30 min,确保双氧水分解完全,取其上清液测定COD和铜的浓度。
1.2.2 中试实验方法
采用中试装置对络合铜废水进行处理,中试装置所用材料为透明PVC,具体尺寸如下图所示。
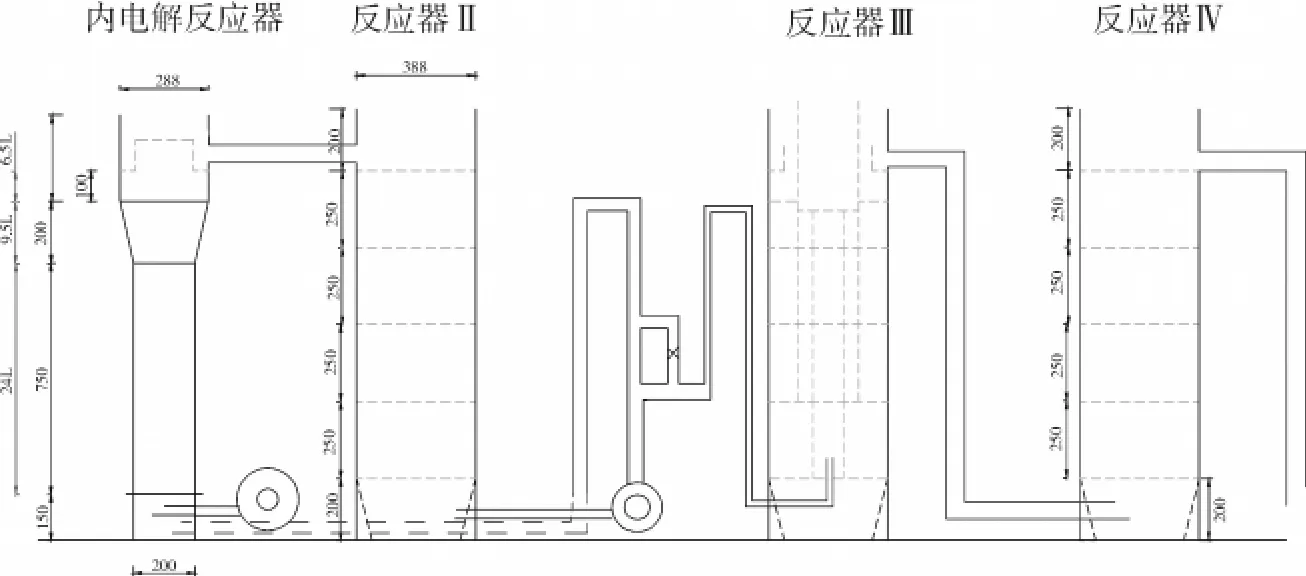
图1 中试装置示意图
中试实验采用两种不同的运行方式,分别为混合运行和串联运行。混合运行是将双氧水投加在反应器Ⅱ里,使得在大流量回流时内电解反应器中也进行Fenton反应;串联运行是将双氧水投加到反应器Ⅲ中,内电解与Fenton氧化先后进行。
2 结果与讨论
2.1 单因素试验结果与讨论
2.1.1 双氧水投加量影响
保持初始pH=3.0,亚铁浓度295.19 mg/L,反应时间90 min,研究H2O2/COD质量比分别为0.5、1.0、2.0、3.0、4.0、6.0时,Fenton氧化法对COD的去除率,以及整个工艺COD总去除率,其结果如图2所示。从图中可以看出COD的去除率随双氧水投加量的增加而逐渐增大,当[H2O2]/[COD]=0.5时,Fenton氧化对COD的去除率为73.59%,[H2O2]/[COD]=6.0时去除率达到94.87%。

图2 双氧水投加量对Fenton氧化的影响
在Fenton反应中双氧水作为底物,是产生OH·的最直接物质,而OH·又是Fenton反应中直接氧化有机物的氧化剂,因此增加双氧水的投加量会促进OH·的产生,从而促进Fenton氧化的进行。由图2可知,[H2O2]/[COD]≤2.0时,COD 随 H2O2量的增加而显著下降,当[H2O2]/[COD]≥3.0时,COD随H2O2的量的增加下降幅度变小。Dutta等[6]的研究表明,H2O2是HO·的捕捉剂,随着H2O2浓度的增加,对羟基自由基的捕捉作用也随之增加,从而消耗一部分羟基自由基,降低双氧水的有效利用。其从反应机理中可知其反应为:HO·+H2O2→HO2·+H2O2,HO·+HO-2→HO2·+OH-,生成的HO2·的氧化能力不如HO·[7],而且投加大量的双氧水会将大量亚铁氧化为Fe3+,从而消耗了部分双氧水。由于内电解已经将铜去除到较低的水平,Fenton进水铜的浓度只有21.4 mg/L,且主要为游离态铜离子,在加碱后基本可以完全去除,当[H2O2]/[COD]≧1.0时,铜的去除率可达到100%。
对于双氧水投加量的确定除了考察处理效果外还要考虑经济性,这就涉及双氧水的效能Q,即单位双氧水投入的有效利用情况,如图3所示,降解单位COD所需的双氧水量Q随[H2O2]/[COD]增加呈线性上升,其关系为 Q=1.0234R+0.2249,其中 Q=[H2O2]/[ΔCOD,R=[H2O2]/[COD]。

图3 双氧水效能(Q=[H2 O2]/[ΔCOD],R=[H2 O2]/[COD],r2=0.9996)
由关系式可以看出,[H2O2]/[COD]每增加1.0,降解单位COD所需的双氧水就会增加1.0234。当双氧水投加量为0时,要降解一个单位的COD就需要0.2249个单位的双氧水,这也是双氧水利用率最高的时候,但显然不可能达到最高的利用率,只可以无限接近。因此在投加一定量双氧水时可以分多次投加,在保证投加量一定的前提下降低废水中双氧水浓度,从而提高双氧水的利用率。根据图2所示,[H2O2]/[COD]=2.0时如果再添加双氧水,COD 的去除率没有明显的增加,[H2O2]/[COD]从1.0升到2.0时COD的去除率增加了7.95%,而从2.0到6.0时,[H2O2]/[COD]每增加1.0时,COD去除率平均增幅才达到2.48%。因此将H2O2的投加量确定为[H2O2]/[COD]=2.0,此时COD的最终去除率达到91.69%。
2.1.2 亚铁量的影响
保持初始pH=3.0,反应时间为90 min,[H2O2]/[COD]=2.0,反应后调节pH=9,絮凝沉淀后取上清液测定COD,其随Fe2+/H2O2的变化情况如图4所示。其中Fe2+/H2O2=0.20是属于不外加亚铁的情况,因为内电解出水中本身就含有110.0 mg/L的亚铁量。

图4 亚铁量对COD的影响
从图中可以看出当Fe2+/H2O2为0.20和0.30时Fenton氧化对COD的去除率为86.23%,之后继续投加亚铁,COD的去除率开始下降,当Fe2+/H2O2>0.50时,COD的去除率又开始上升,这是因为溶液中Fe2+和Fe3+总量的增加,导致混凝沉淀时铁的氢氧化物对有机物的吸附量增加,从而抵消Fenton反应去除率的下降。
为此,测定了Fenton氧化出水加碱絮凝前Fe2+/H2O2为0.30和1.0的COD,结果如表1所示。从表1的数据中可以看出,Fe2+/H2O2=0.3时,Fenton反应所直接引起的COD去除率远大于Fe2+/H2O2=1.0时的COD的去除率,因此可以确定Fe2+/H2O2=0.50之后COD去除率上升的原因是氢氧化铁和氢氧化亚铁絮凝沉淀的吸附作用抵消Fenton氧化效果降低的结果。因此Fe2+/H2O2=0.20是最佳亚铁量。

表1 Fenton反应后絮凝沉淀前COD去除率
2.1.3 初始pH值影响
保持H2O2/COD=2.0,Fe2+/H2O2=0.20~0.30,反应时间90 min,pH值对COD去除率的影响如图5所示。

图5 不同pH值条件下Fenton氧化的处理效果
从图5可知,当pH在2.0~4.0的范围内COD的去除效果较好,当4.0≦pH≦7.0时COD的去除率略有下降,pH>7.0后COD的去除率下降显著,说明在碱性条件下Fenton氧化的效果不佳。这是因为在碱性条件下双氧水的稳定性降低,很容易分解成水和氧气,降低了双氧水的利用率,而且碱性条件下亚铁都生成氢氧化物沉淀,进而被氧化成氢氧化铁,大大降低HO·的生成量,甚至不生成,使氧化过程靠新生成的氧气和双氧水自身的氧化性进行。因此Fenton氧化不应在碱性条件下进行,最好初始pH为3.0。
2.1.4 反应时间的确定
保持[H2O2]/[COD]=2.0,Fe2+/H2O2=0.20~0.30,初始pH=3.0,处理时间与COD和铜的去除率关系如图6所示。
从图6中可以看出,随着Fenton反应的进行,COD和总铜的去除率在不断上升,说明在反应刚开始时,Fenton氧化具有较高的反应速率,当反应进行到60 min后,COD的去除率曲线趋于平缓,此时COD的去除率基本达到最大值。而对于铜的去除率则在30 min就达到了最大值,此时的铜离子浓度为0.5 mg/L。由于,Fenton氧化工艺主要用于去除COD,因此选择60 min为Fenton氧化的最佳反应时间。
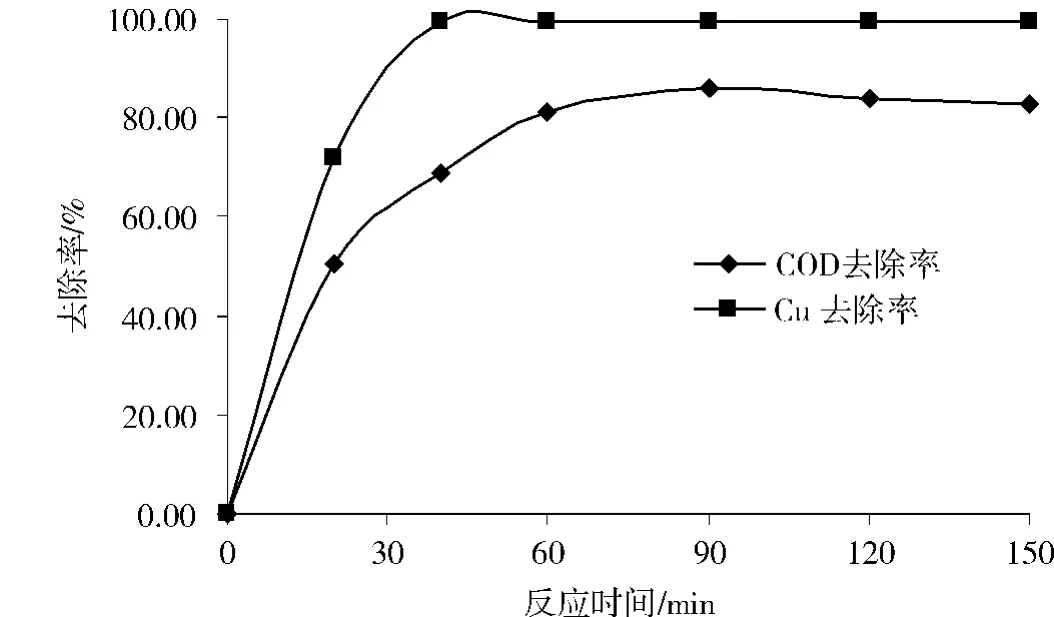
图6 Fenton氧化时间对处理效果影响
2.2 中试实验
通过单因素实验,确定了Fenton氧化强化处理经内电解处理的络合铜废水出水的最佳反应条件,中试试验在此条件下进行,通过考察内电解与Fenton氧化混合运行和串联运行时的处理效果,结果如表2所示。

表2 不同运行方式时COD去除率%
从表2中可以看出,混合运行时的COD去除率为80.56%,串联运行时内电解出水的COD去除率为27.12%,Fenton氧化絮凝出水的COD去除率为87.04%,在内电解出水的基础上Fenton氧化将COD的去除率提升了近60%。将两种处理工艺对COD的去除效果做对比,可以看出串联运行时的处理效果明显比混合运行时的处理效果好,这是因为内电解和Fenton氧化都对大分子有机物有较强的去除能力,但Fenton氧化的氧化能力比内电解强,将内电解和Fenton反应放在同一个反应器中会导致Fenton试剂在开始时就氧化初始的进水,而内电解又无法降解Fenton氧化后剩下的COD,同时在反应器中有铁碳填料,会影响到Fenton氧化中Fe2+和Fe3+的平衡,最终导致双氧水的利用率不高,而且Fenton反应所形成的大量沉淀物会留在内电解填料中,阻碍铁碳微电池形成,进一步降低处理效果,同时增加填料结块的可能。当将这两个反应工序分开时内电解先将大分子的有机物分解成较小的分子,并且打开了一些难断裂的化学键,当内电解反应出水进入Fenton反应器后,Fenton试剂又可以进一步降解内电解反应后形成的小分子物质和一些内电解无法降解的有机物,从而最大限度地利用了双氧水。而且分开运行又解决了Fenton反应形成的沉淀物堆积在铁碳填料中的问题。同时还可以看出Fenton强化氧化后,COD的去除率显著上升,这也说明Fenton反应对内电解出水具有较好的强化效果。
3 结论
1)单因素实验确定Fenton氧化的双氧水投加量为[H2O2]/[COD]=2.0,最佳亚铁投加量为Fe2+/H2O2=0.20~0.30,初始pH为3.0,反应时间为60 min。在此最佳条件下Fenton氧化对COD的去除率可以达到81.35%。
2)通过中试实验确定串联运行时的处理效果比混合运行时的效果好,混合运行时COD去除率为80.56%,串联运行时COD的去处率在内电解的基础上提升近60%,最终去除率为87.04%,铜的总去除率达到99.86%。
[1]何明,梁振驹,李红进.铁屑内电解法处理PCB络合废水[J].水处理技术,2008,34(6):84-86.
[2]李辉.铁碳微电解-Fenton氧化联合处理染料废水研究[D].哈尔滨:哈尔滨工业大学,2006.
[3]孙旭辉,贾宇宇,马军,等.微电解-Fenton联合工艺处理硝基苯废水效能研究[J].水处理技术,200935(1):74-78.
[4]张琦.酸化-Fenton氧化-混凝法处理印制电路板有机废水研究[D].哈尔滨:东北农业大学资源与环境学院,2009.
[5]彭军,胡勇为.Fenton试剂在印制电路板工业废水处理中的应用[J].工业用水与废水,2006,37(3):31-34.
[6]Duttu K,Mukhopadhyay S,Bhattacharjee S,et al.Chemical oxidation of methylene blue using a Fenton -like reaction[J].Journal of Hazardous Material,2001,84(1):57 -71.
[7]祁佩时,赵俊杰,刘云芝,等.Fenton试剂深度处理稠油石化废水的反应动力学[J].化工学报,2011,62(2):491-494.
