HPLC-DAD法对扶正平消胶囊中龙胆苦苷的含量研究
2011-08-05姜云霞金柔男朱张超上海东方肝胆外科医院药材科上海200438
姜云霞,战 旗,金柔男,朱张超,王 彬(上海东方肝胆外科医院药材科,上海 200438)
扶正平消胶囊是由黄芪、当归、全蝎、蜈蚣等二十八味中药组成的复方制剂。对于这二十八味中药大复方制剂,我院现有的质量标准中仅有黄芪、浙贝母及狼毒这三味药材的薄层鉴别,无法满足《中国药典》2010版一部对于中药制剂的标准要求。因此为了提高医院制剂的质量标准,我们选择复方中比重最大的药材之一龙胆作为研究对象,进行含量测定方面的研究。
龙胆药材其化学成分含裂环烯醚萜苷类苦味成分(龙胆苦苷,当药苦苷,当药苷,苦龙胆酯苷,痕量苦当药酯苷),生物碱(龙胆碱)[1~3]。《中国药典》2010版中将龙胆苦苷作为控制龙胆药材的指标,其中龙胆苦苷含量可高达3.0%。其含量测定方法有多种,包括高效液相色谱法[4],薄层色谱扫描法[5],
液相色谱-串联质谱法[6],毛细管电泳法[7]等。其中高效液相色谱法在中药制剂分析中具有较多优点,包括速度快,分辨率高,并且用一根色谱柱可分离不同的化合物并且可反复使用等等。因此,我们首先考虑使用高效液相色谱法对扶正平消中龙胆苦苷进行含量测定的研究。
1 仪器和试药
1.1 仪器 Agilent 1100 Series(安捷伦)高效液相色谱仪(G1379A脱气阀,G1311A泵,G1367A进样器,G1316A柱温箱,G1314A紫外检测器),AE240电子天平(德国梅特勒),SK2200H型超声波清洗器(上海科导超声仪器有限公司)。
1.2 试药 扶正平消胶囊由第二军医大学附属东方肝胆外科医院制剂室生产(批号:080901,081101,090101,090301,090801,091201),龙胆苦苷对照品购自中国药品生物制品检定所(110770-200712),无水乙醇、磷酸、甲醇等均为分析纯,流动相甲醇为色谱纯,水为娃哈哈纯净水。
2 方法和结果
2.1 对照品溶液的制备 精密称取龙胆苦苷对照品6.1 mg,加19%甲醇溶解定容置25 ml量瓶中,配成浓度为244 μg/ml龙胆苦苷对照品母液。精密吸取上述对照品母液10 ml,用19%甲醇稀释定容置25 ml量瓶中,得对照品母液浓度为 97.60 μg/ml,再分别精密吸取上述对照品母液 0.5、1、2、4、6、8 ml,用19%甲醇分别稀释定容置10 ml量瓶中,得对照品标准系列溶液,浓度依次为 4.88、9.76、19.52、39.04、58.56、78.08 μg/ml。
2.2 供试品溶液的制备 取扶正平消胶囊10粒的内容物,混匀,精密称定,加40%甲醇溶解定容置50 ml量瓶中,静置12 h,超声1 h,放冷,稀释至刻度,混匀,用微孔滤膜(0.22 μm)滤过,取续滤液即得。
2.3 色谱条件 色谱柱 Agilent Zorbax XDB-C8(4.6 mm ×150 mm,5 μm),流动相为甲醇-水(19∶81),检测波长 275 nm,流速 1 ml/min,柱温为 25℃,进样量 20 μl。
2.4 阴性供试品的制备及考察 取处方量药材(全蝎、蜈蚣由厂家提取)加水回流提取2次,每次2 h,水量分别为10、8倍量,过滤,得滤液;滤液浓缩至相对密度1.1,加乙醇至乙醇终浓度为60%,放置24 h,过滤得滤液。合并全蝎、蜈蚣滤液,回收乙醇,浓缩,干燥,粉碎,过120目筛,即得阴性样品。按照供试品溶液的制备方法项下制备阴性样品溶液,20 μl进样测定。样品图中目标峰后还有一小峰,通过计算得出其分离度R=1.76,符合色谱图分离要求。色谱图见图1。
2.5 线性关系的考察 分别将不同浓度的对照品溶液依次连续进样,重复5次,以对照品溶液的浓度(X,μg/ml)对对照品的峰面积(Y)进行线性回归。得到龙胆苦苷的回归方程为Y=23.82X-7.170(r=0.999 9),在 4.88 ~ 97.60 μg/ml之间的线性关系良好。以信噪比10∶1确定最低定量限为0.244 μg/ml。
2.6 精密度试验
2.6.1 日内精密度 取上述对照品溶液中的4.88、39.04、97.60 μg/ml 3 个浓度各 20 μl进样,早、中、晚各一次,记录各色谱峰的峰面积,计算得RSD 值依次为 1.06%、1.47%、1.68%,日内精密度均小于2%,符合检测要求。
2.6.2 日间精密度 取上述对照品溶液中的4.88、39.04、97.6 μg/ml 3 个浓度各 20 μl进样,连续测定5 d,记录各色谱峰的峰面积,计算得RSD值依次为1.35%、1.55%、2.75%,日间精密度均小于3%,符合检测要求。

图1 HPLC色谱图
2.7 回收率试验 取090301批号扶正平消胶囊10粒,精密称定2.528 40 g,加40%甲醇49 ml及39.04 μg/ml龙胆苦苷标准液 1 ml,静置 12 h,超声1 h,静置,过滤即得。取20 μl进样,测定4次。结果显示样品加样回收率为99.39%,在95% ~105%之间,符合检测要求。
2.8 稳定性试验 取对照品溶液 4.88、39.04、97.6 μg/ml 3 个浓度,分别于 0、12、24、48、72、96 h进样 20 μl,测得峰面积,计算得 RSD值依次为1.47%、4.26%、3.87%。在符合要求的情况下,取相对回收率试验时配制的样品,于 0、12、24、48、72、96 h进样20 μl,结果得 RSD值为3.83%。结果显示,龙胆苦苷对照品及龙胆苦苷在扶正平消胶囊中含量在96 h内稳定。
3 讨论
3.1 检测波长的选择 文献检索发现潘利明等[4]将270 nm作为龙胆苦苷的最大吸收波长,而高言明等[7]使用275 nm作为最大吸收波长。本实验中,我们通过对对照品龙胆苦苷进行DAD测定,发现275 nm为最大吸收波长,光谱图见图2。
3.2 色谱柱的选择 我们选择了几种不同的色谱柱进行考察,发现应用XDB-C8(4.6 mm×150 mm,5 μm)有更好的效果,峰形有分离的趋势,且保留时间良好。因此在此基础上进行进一步优化。
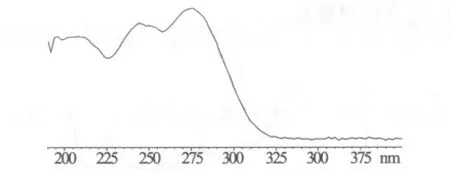
图2 龙胆苦苷光谱图
3.3 溶剂的选择 我们选择了100%、50%、19%甲醇以及100%乙醇与纯水为溶剂溶解样品进行考察,分别进样,其中50%甲醇溶解较好。后又进样发现,50%甲醇溶解时,有峰倾斜的现象,不利于定量分析,所以又尝试其他浓度甲醇溶解,最后发现40%甲醇溶解时,峰面积最高。具体结果见图3。

图3 光谱图(40%甲醇为溶剂)
3.4 流动相的选择 通过实验研究,我们考察的范围为甲醇-水(25∶75,23∶77,21∶79,19∶81),我们发现,随着甲醇比例的减少,分离度越来越高。当甲醇-水比例为19∶81时,龙胆苦苷峰能与前一干扰峰完全分离,并且出峰时间在15 min内,符合分离度的要求。具体结果见表1。

表1 龙胆苦苷峰流动相甲醇-水比例与分离度的关系
4 样品测定
取不同批号的扶正平消胶囊按照供试品溶液配制方法制备供试品溶液,各取20 μl进样,每个样品重复2次。结果见表2。
2010版药典一部规定,龙胆药材中龙胆苦苷的含量应不低于3.0%,同时根据龙胆药材占处方中比例计,龙胆苦苷理论含量应不低于0.16 mg/粒;而测定结果显示只有090101、090301两批号符合此要求。同时批号080901、081101含量低于0.16 mg/粒,我们怀疑是由于此制剂放置时间超过1年半,有可能龙胆苦苷分解导致含量降低。批号091201中龙胆苦苷含量低于0.16 mg/粒,我们怀疑有可能是更换了生产厂家,供应的药材与前一厂家不同,造成含量偏低。而批号090101、090301测定的含量大于0.16 mg/粒,虽然其放置时间超过一年保质期。

表2 样品中龙胆苦苷含量测定结果
5 结论
本法专属性强,灵敏度高,选择性好,可用于测定扶正平消胶囊中龙胆苦苷的含量。
[1]Anonymous.Reports on phytotherapy findings from L.Y.Chen and co-researchers provide new insights[J].Drug Week,2010,26(2):1658.
[2]Anonymous.University of Liege details research in natural products[J].Science Letter,2009,3(2):1830 .
[3]Anonymous.Study results from Northwest University,College of Life Science provide new insights into analgesics[J].Pain &Central Nervous System Week,2008,11(8):314.
[4]潘利明.金胆胶囊中龙胆苦苷的定性定量研究[J].广东药学院学报,2008,24(3):226.
[5]钟 强,谢 娇,潘 洪.双波长薄层扫描法测定泻胆丸中龙胆苦苷的含量[J].时珍国医国药,2004,15(7):393.
[6]冯 怡,邓远辉,曾 星,等.液相色谱-串联质谱法测定人血浆中的龙胆苦苷浓度[J].药物分析杂志,2007,27(02):157.
[7]高言明,宋 勤,陈惠玲,等.高效毛细管电泳测定龙胆中龙胆苦苷的含量[J].药物分析杂志,2007,27(02):1572.
[8]中国药典2010版.一部[S].2010:89.
[9]刘 涛,韩立伟,黄学石,等.紫外分光光度法测定龙胆软胶囊中总裂环环烯醚萜苷的含量[J].中国医科大学学报,2006,35(4):388.
[10]白小红,杨 雪,陈 璇,等.不同产地龙胆中龙胆苦苷的含量测定[J].沈阳药科大学学报,2004,21(2):114.
[11]陈国锋,高东雁,张文鑫,等.龙胆苦苷的体外稳定性[J].复旦学报(医学版),2008,41(7):220.
[12]李莲芳,梁晓原,王 扣.龙胆中龙胆总苷的含量测定[J].云南中医学院学报,2006,29(5):9.
