内聚营养源SRB污泥固定化处理含锌及硫酸根废水
2011-08-04李二平闵小波舒余德杨少辉柴立元
李二平,闵小波,舒余德,杨少辉,柴立元
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
大量排放的含锌废水对人体健康和工农业活动有严重危害性,具有持久性、毒性大、污染严重等特点,一旦进入环境后不能被生物降解,并最终在生物体内积累,破坏生物体正常生理代谢活动,危害人体健康[1-2]。目前,对于含锌废水的治理,国内外应用的技术有化学沉淀法、离子交换法、吸附法和萃取法等[3],虽然这些处理方法效果好,但由于操作费用及原材料成本相对过高,难以推广应用[4-6],而且容易造成二次污染[7]。生物法与传统物理化学法相比具有投资小、运行费用低、无二次污染等优点,使得利用微生物处理重金属废水成了各国学者研究的热点[4]。微生物法处理含硫酸盐的重金属废水是在厌氧条件下,利用硫酸盐还原菌(SRB) 将SO42-还原为H2S,废水中的重金属离子再与 SO42-还原产生的 H2S形成金属硫化物沉淀去除[8-9]。目前SRB法主要存在两大不足:一是现有的技术中,无论是游离的细菌还是载体化的SRB,都会与废水中金属离子直接接触,难以避免客观存在的重金属离子的毒害作用[10];二是加入的SRB生长必需的有机碳源很难被其全部利用,导致出水COD偏高[11-12]。作者提出一种处理重金属废水的新方法——内聚营养源 SRB 污泥固定化新技术[13],将SRB生长所需的有机营养源经固定化处理,与 SRB污泥共同包埋于同一颗小球内部,构造SRB污泥生长良好的内、外环境,既可以避免金属离子对SRB污泥的毒害,又可解决有机物污染的问题, 同时,更有利于SRB污泥对营养物质的利用,实现重金属废水低廉高效处理,达到废水“零排放”要求。前期实验已完成SRB污泥的驯化、固定化小球的制备与再生及 SRB固定化处理重金属废水的工艺参数研究[14-16],但均采用间歇式实验,未进行连续化反应。本文作者在自制上流式厌氧反应器中利用内聚营养源 SRB污泥固定化颗粒小球进行含锌废水的连续处理,进一步证明了该固定化技术处理的可行性,为该技术处理重金属废水的设计和运行提供参考和依据。
1 试验材料与方法
1.1 试验装置
上流式厌氧反应器为有机玻璃制成的圆柱形,有效体积为850 mL,内径为45 mm,高径比为12:1。反应器置于生化培养箱内,温度控制在(35±1) ℃。试验装置如图1所示。

图1 试验装置示意图Fig.1 Schematic diagram of experimental setup
1.2 模拟废水
模拟废水:KH2PO40.5 g/L;NH4Cl 1.0 g/L;MgSO4·7H2O 0.06 g/L;CaSO41.0 g/L;FeSO4·7H2O 0.01 g/L;Na2SO45.05 g/L;CaCl20.06 g/L;Zn(Ⅱ) 0.100 g/L;pH=5.9。
1.3 内聚营养源 SRB污泥固定化小球及含锌废水试验方法
SRB污泥的驯化,固定化小球的制备、储藏、激活、营养源的内聚与再生方法与前期研究所采用的方法相同[14-15]。将一定量激活并内聚营养源的固定化SRB小球洗净置于图1试验装置中,充氮气排除反应器中空气并密封,调整反应器进水SO42-的质量浓度、pH、废水与固定化小球质量比,定时取样分析出水中锌离子与硫酸根含量。试验结束后取出小球洗净,重新内聚营养源,如此反复进行试验。
1.4 分析方法[16]
锌离子浓度测定采用原子吸收分光光度法;硫酸根浓度测定采用铬酸钡分光光度法;硫总离子测定采用碘量法;固定化小球组分采用 EDX能谱分析;沉淀物相采用X线衍射(XRD)分析。
2 结果与讨论
2.1 进水 SO42-质量浓度对出水 Zn2+和 SO42-去除效果及出水总硫离子质量浓度的影响
硫酸根是SRB 能量的来源,对SRB 的生长起关键性作用。在反应器水力滞留时间为20 h,进水SO42-质量浓度为0.775~6.006 g/L,固定化小球与废水的质量比为1:5,pH为5.9,Zn2+质量浓度为0.100 g/L的条件下,考察反应器进水 SO42-质量浓度对出水 Zn2+和 SO42-去除效果以及总硫离子质量浓度的影响,结果见图 2~4。
由图2可见:进水SO42-质量浓度为0.775~4.151 g/L时,出水Zn2+质量浓度随着进水SO42质量浓度的增加而降低;当进水SO42-质量浓度为4.151~6.006 g/L时,出水Zn2+质量浓度基本不变,保持在1.4 mg/L左右;在整个试验 SO42-质量浓度范围内,出水 Zn2+质量浓度均低于2 mg/L,Zn2+去除率均可达到98%以上。由图3可知:当进水SO42-质量浓度由0.775 g/L逐步提高到3.259 g/L时,SO42-去除率由60.3%缓慢下降到57.8%,进一步提高进水 SO42-质量浓度,当 SO42-质量浓度升高到6.006 g/L时,SO42-去除率降为33.3%;当进水SO42-质量浓度为0.775~4.151 g/L时,SO42-的去除率随着进水 SO42-质量浓度的升高而增加;当进水SO42-质量浓度为4.151~6.006 g/L时,SO42-的去除率变化不大,保持在2.00 g/L左右。图4表明:出水总硫离子浓度随着进水SO42-质量浓度的增加而增加;当SO42-质量浓度小于3.259 g/L时,出水总硫离子质量浓度随着进水 SO42-质量浓度增加而大幅增加;当SO42-质量浓度大于3.259 g/L时,出水总硫离子质量浓度随着SO42-质量浓度增加幅度变小。
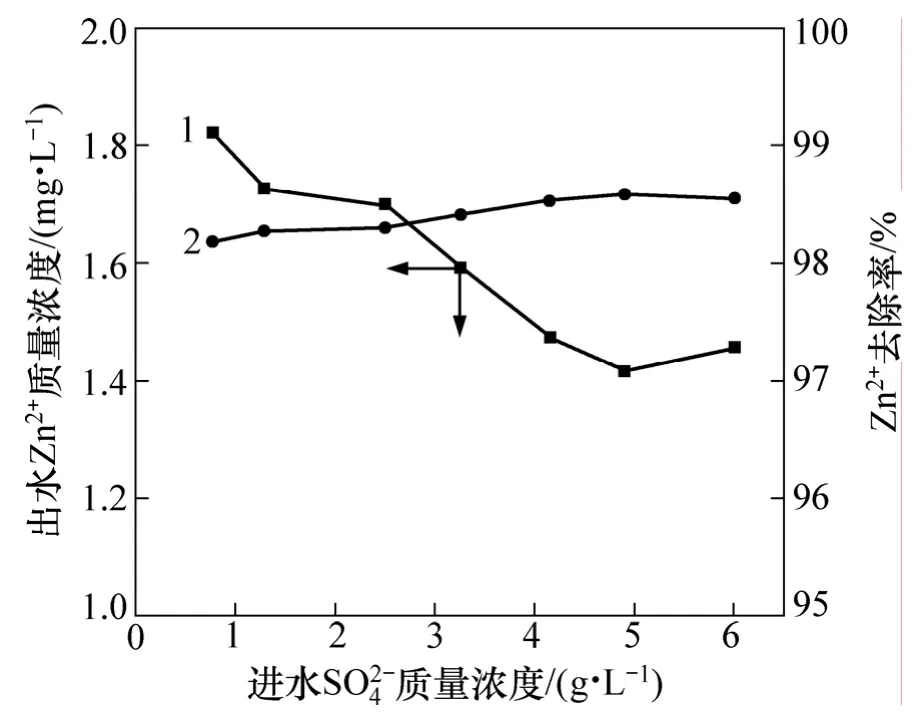
图2 进水SO42-质量浓度对出水Zn2+去除效果的影响Fig.2 Effects of SO42- concentration in influent on Zn2+ removal

图3 进水SO42-浓度对出水SO42-去除效果的影响Fig.3 Effect of SO42- concentration in influent on SO42- removal
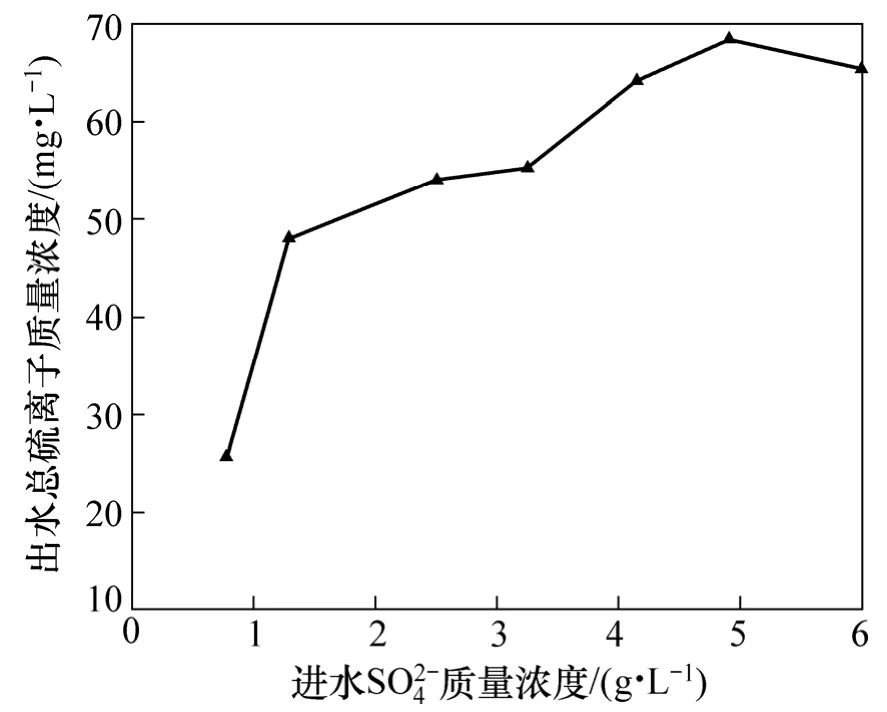
图4 进水SO42-浓度对出水总硫离子浓度的影响Fig.4 Effects of SO42- concentration in influent on total sulfur ion in effluent
2.2 进水pH、固定化小球与废水质量比对Zn2+去除效果的影响
pH 是影响SRB 活力的主要因素[17-18],相对于产酸菌来说,SRB 所能耐受的pH 范围较窄,尽管其比MPB 适应环境的能力要强,但是在过低或过高的pH条件下,SRB必定难以生长和进行硫酸盐还原。保持反应器中高浓度微生物数量是固定化微生物技术的一大优点,而维持较高的容积负荷及较低的污泥负荷是绝大多数废水处理工艺所力求达到的[19]。改变固定化小球与废水的质量比,反应器中的生物量与容积负荷也随之改变。在水力滞留时间为20 h,进水SO42-质量浓度为4.151 g/L,Zn2+质量浓度为0.100 g/L的条件下,考察反应器进水pH、固定化小球与废水质量比对出水Zn2+去除效果的影响,结果见图5~6。
从图5可以看出:当进水pH在3~7之间变化时,固定化小球对Zn2+的去除率始终保持在98%以上,且出水Zn2+质量浓度保持在1.4~1.7 mg/L之间;进水pH为8~12时,Zn2+的去除率均在95%以上,且出水Zn2+质量浓度保持在2.2~4.9 mg/L;当进水pH小于3或大于12时,Zn2+的去除率急剧下降。该现象说明,SRB经包埋固定后,包埋剂特殊的结构使SRB包裹在一个微环境中,受外界影响较小,对pH的适应性增强。
由图6可见:当固定化小球与废水质量比为1:20,1:15,1:10,1:5,1:2和1:1时,出水Zn2+质量浓度分别为10.6,7.0,2.3,1.4,0.7和0.3 mg/L,相应去除率为89.4%,93.0%,97.7%,98.6%,99.3%和99.7%。可见固定化小球与废水的质量比越大,锌离子去除率越高,考虑经济成本因素,实际运行过程中选择球液质量比1:2为最佳工艺参数。
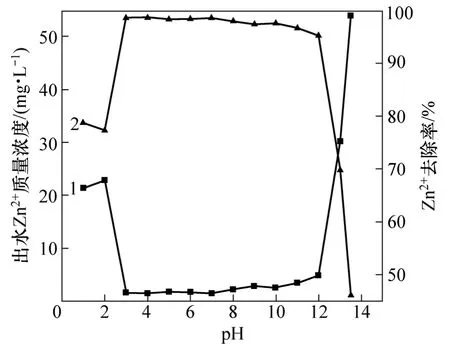
图5 进水pH对出水Zn2+去除效果的影响Fig.5 Effects of pH in influent on Zn2+ removal
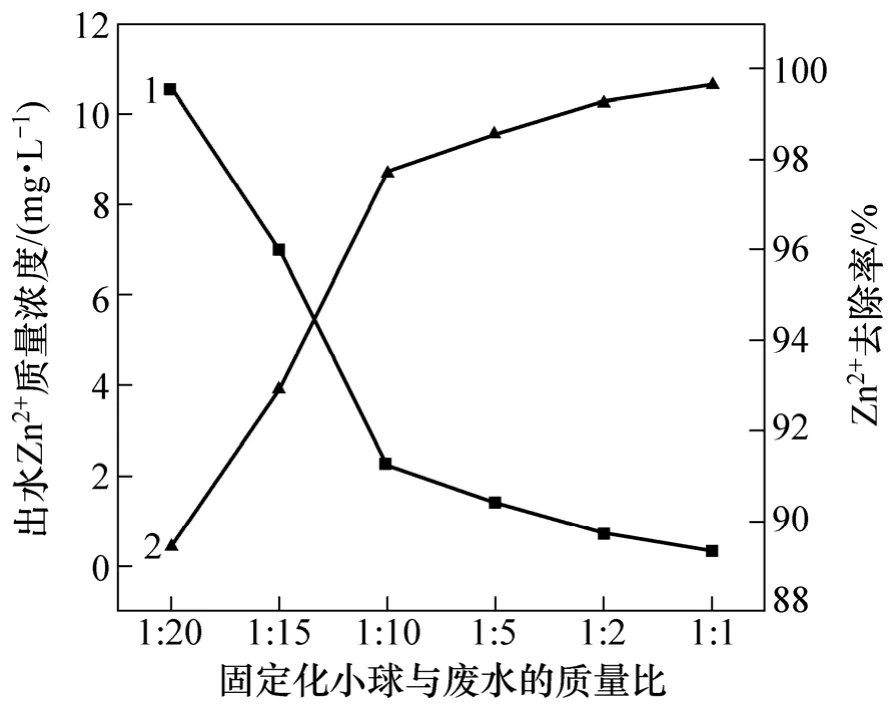
图6 固定化小球与废水质量比对出水Zn2+去除效果的影响Fig.6 Effects of mass ratio of beads to liquid on Zn2+ removal
由米式方程得[20-21]:

式中:v为酶催化反应速率,mol/(L·h);vmax为酶反应最大反应速率,mol/(L·h);Km为米式常数,mol/L;为底物浓度,mol/L。
2.3 SO42-还原动力学及硫离子分布
根据方程(1)将图3数据转化为酶催化反应速率与SO42-浓度的关系,见图7。
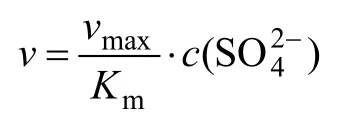
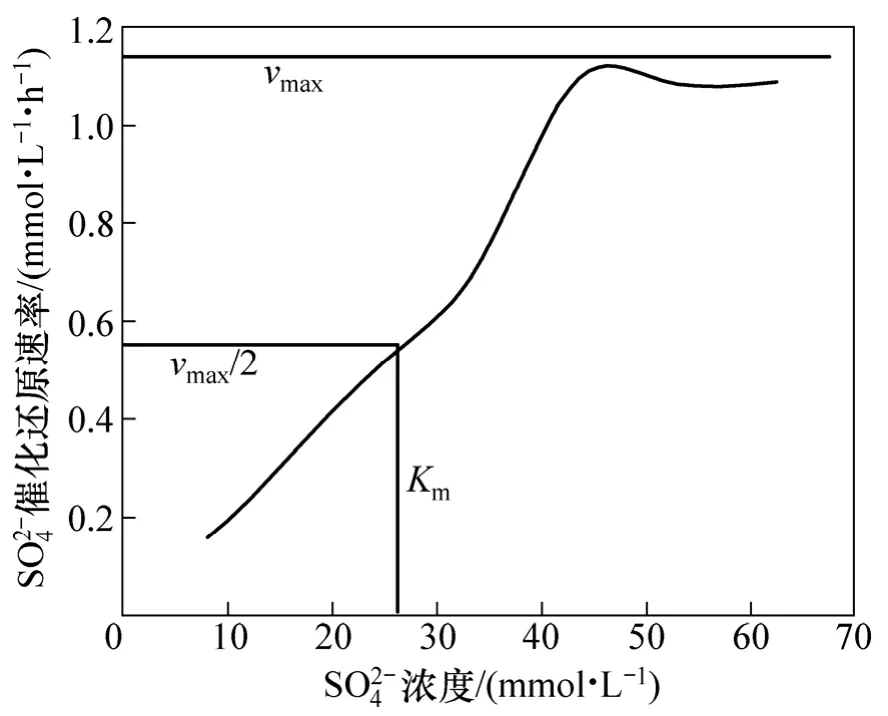
图7 SO42-催化反应速率与SO42-浓度的关系Fig.7 Relationship between rates of SO42- catalytic reaction and SO42- concentration
此时SO42-还原为酶反应动力学一级反应,由于是一级反应,因此,当进水SO42-质量浓度为0~3.259 g/L时,出水Zn2+质量浓度及SO42-质量浓度随着进水SO42-质量浓度增加而下降;反应速率与进水 SO42-浓度成正比,还原得到的大量S2-(主要以HS-存在),未能与 Zn2+反应从而出现大量 HS-过剩,故出水 SO42-质量浓度增加,出水中过剩的总硫离子也随进水SO42-质量浓度增加而大幅度增加。

此时,SO42-还原为酶反应动力学零级反应,反应速率与硫酸根浓度无关。这也就解释了 SO42-质量浓度>3.259 g/L时,随着进水SO42-浓度增加,SO42-去除率迅速下降,出水Zn2+浓度及出水总硫离子浓度随着SO42-质量浓度增加而变化不大。
SRB污泥固定化小球还原 SO42-得到的硫离子主要有3种形态:一是S2-与废水中的Zn2+产生ZnS沉淀;二是溶解在出水中;三是吸附于固定化小球的内外表面。根据图 2~4可得出进水 SO42-质量浓度与总硫离子浓度、硫化锌中硫离子浓度和出水中总硫离子浓度的关系,见图8。
从图8可以看出:还原总硫离子浓度大于ZnS沉淀中与出水中硫离子质量浓度之总和,而这部分差值主要是固定化小球内外表面吸附硫所引起的。图9所示为处理含锌废水后的固定化小球的能谱分析结果。从图9可以看出:在小球内外表面都含有一定量的硫,而且外表面的含量明显高于内部含量,从而可以证明部分硫离子被球吸附。
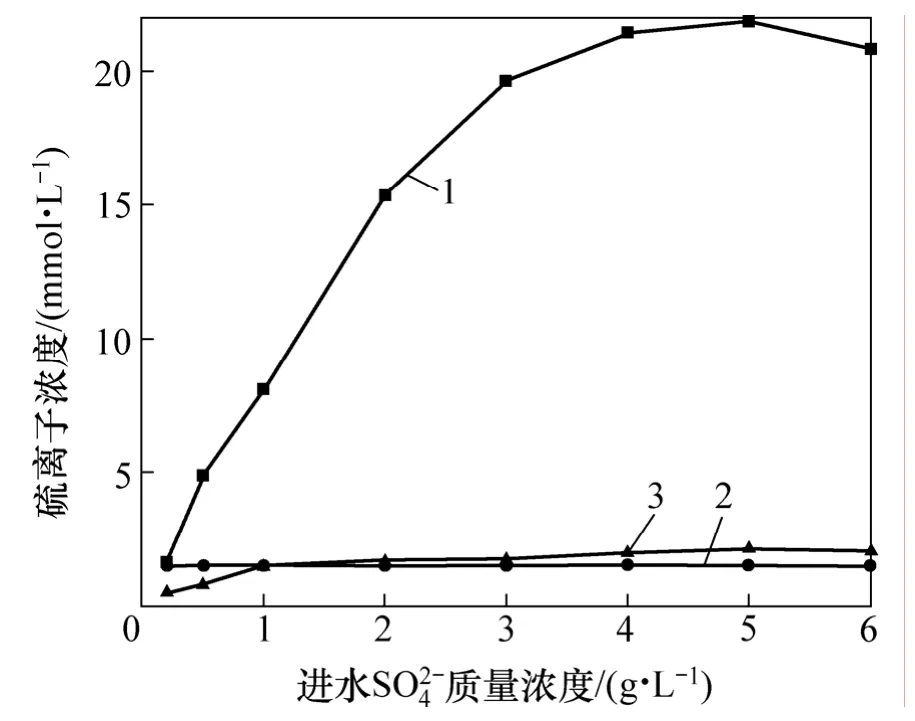
图8 进水SO42-质量浓度与各种形态硫离子浓度的关系Fig.8 Relationships between various forms of sulfur and influent SO42- concentration

图9 处理废水后固定化小球能谱分析结果Fig.9 EDX results of immobilized beads after reaction
2.4 SRB污泥固定化除锌机理
将去除锌离子的试验废水进行离心,去掉上层清液,得到混合沉淀物,烘干并研磨成粉末状态,进行X线衍射分析[22],结果见图10。
结合图9与10可以得出:混合沉淀物中含有ZnS,证明废水中所含锌离子是以 ZnS 沉淀的形式被去除的。因此,可以证明利用SRB污泥固定化去除废水中锌离子的一个主要优势就是利用 SRB 生长代谢过程中产生的硫离子与锌离子结合生成难溶于水的 ZnS沉淀,从而达到高效除锌的目的。
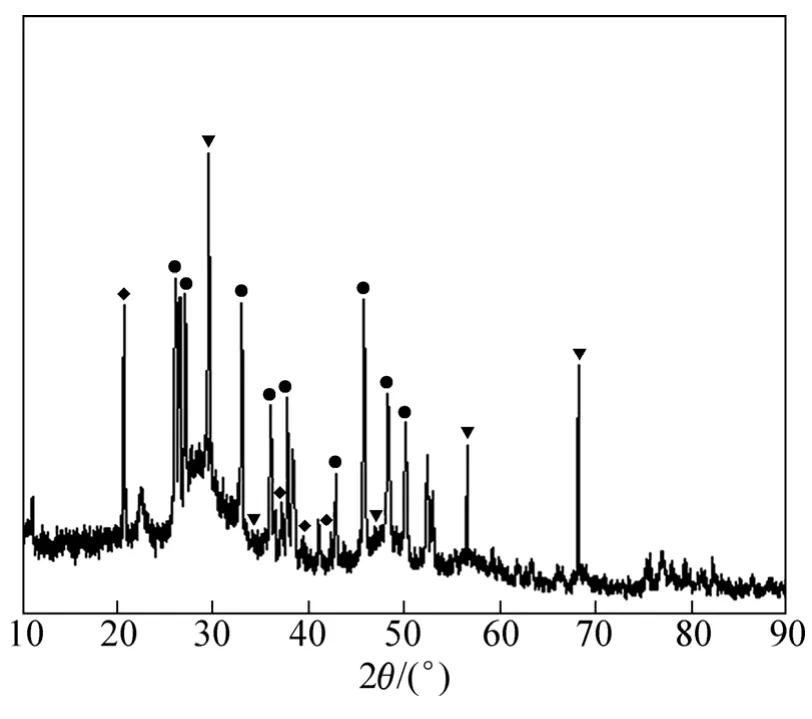
图10 处理后沉淀物的X线衍射谱Fig.10 XRD pattern of sediments precipitated from wastewater by imobilized SRB sludge bead
3 结论
(1) 在进水SO42-质量浓度为4.151 g/L、Zn2+质量浓度为0.100 g/L、pH为5.9、固定化小球与废水质量比为1:2、水力滞留时间为20 h的条件下,Zn2+去除率达98%以上,出水Zn2+质量浓度低于2 mg/L,达《污水综合排放标准》(GB 8978—1996);SO42-质量浓度小于3.259 g/L时,脱除率可达57.8%。
(2) SRB污泥经固定化后,pH在3~12范围内均可进行生物还原,且锌去除率均达到95%以上,对pH的适应性增强。
(3) 在沉淀物分析中检测到 ZnS,且处理废水后的固定化小球内外表面几乎不存在Zn,说明锌离子主要是以ZnS 的形式从水溶液中被去除。
(4) 利用稳态法得到的 SO42-催化还原速率与SO42-浓度的函数关系曲线遵守米氏方程式规律,根据得到的动力学方程式能合理解释有关实验结果。
[1] 方艳, 闵小波, 唐宁. 含锌废水处理技术的研究进展[J]. 工业安全与环保, 2006, 32(7): 5-8.FANG Yan, MIN Xiao-bo, TANG Ning. Research development on the treatment for wastewater containing zinc[J]. Industrial Safety and Environmental Protection, 2006, 32(7): 5-8.
[2] 邓敬石, 张宗华, 陈家栋. 浅淡含重金属离子的铅锌矿尾矿废水危害及治理[J]. 云南冶金, 2002, 31(2): 20-22, 53.DENG Jing-shi, ZHANG Zong-hua, CHEN Jia-dong. A preliminary discussion on the harmful effect and treatment of Lead-Zinc tailing wastewater containing heavy metal ions[J].Yunnan Metallurgy, 2002, 31(2): 20-22, 53.
[3] 王彦斌, 王卓, 苏琼. 乳状液型液膜法处理含锌废水的动力学[J]. 计算机与应用化学, 2003, 20(3): 345-347.WANG Yan-bin, WANG Zhuo, SU Qiong. Kinetics of zinc extraction from wastewater by surfactant liquid membrane[J].Computers and Applied Chemistry, 2003, 20(3): 345-347.
[4] 孟祥和, 胡国飞. 重金属废水处理[M]. 北京: 化学工业出版社, 2000: 139-143.MENG Xiang-he, HU Guo-fei. Treatment of heavy metal wastewater[M]. Beijing: Chemical Industry Press, 2000:139-143.
[5] 张建梅, 韩志萍, 王亚军. 重金属废水的治理和回收综述[J].湖州师范学院学报, 2002, 24(3): 48-52.ZHANG Jian-mei, HANG Zhi-ping, WANG Ya-jun. A summary of harnessing and retrieval of waste water containing heavy metals[J]. Journal of Huzhou Teachers College, 2002, 24(3):48-52.
[6] 李宾. 化学法处理含重金属废水的应用介绍[J]. 材料保护,2000, 33(10): 18-19.LI Bin. Application of chemical treatment for heavy metals wastewater[J]. Materiais Protection, 2000, 33(10): 18-19.
[7] 夏君, 瞿建国, 李福德. 硫酸盐还原菌(SRB)处理含锌废水的基础研究[J]. 上海化工, 2006, 31(8): 1-3.XIA Jun, QU Jian-guo, LI Fu-de. The basic research of using microorganisms to remove Zinc from wastewater[J]. Shanghai Chemical Industry, 2006, 31(8): 1-3.
[8] Ueki K, Ueki A. Removal of sulfate and heavy metal from acid mine water by anaerobic treatment with cattle waste: Effects of heavy metals on sulfate reduction[J]. Environ Sci Health A, 1991,A26(8): 1471-1489.
[9] Dvorak D H, Hedin R S. Treatment of metal-contaminated water using bacterial sulfate reduction: Results from pilot-scale reactor[J]. Biotechnology and Bioengineering, 1992, 40(5):609-616.
[10] Diels L, Svan R, Hooyberghs L, et al. Heavy metal biosorption and bioprecipitation by Alcaligenes eutrophusER121[J].International Biodeterioration and Biodegradation, 1996, 37(3/4):241-252.
[11] Hayashita T, Noguchi H, Oka H. Selective sorption of heavy metal thiocyanate complexes on crown ether resin[J]. Journal of Applied Polymer Science, 1990, 39(3): 561-569.
[12] Maree J. A biological treatment of mining effluents[J]. Environ Tech Letters, 1987, 8(4): 53-66.
[13] Min X B, Chai L Y, Zhang C F, et al. Control of metal toxicity,effluent COD and regeneration of gel beads by immobilized sulfate-reducing bacteria[J]. Chemosphere, 2008, 72(7):1086-1091.
[14] 王娜, 闵小波, 王云燕. 内聚营养源 SRB固定化交联剂的选择及对含锌废水的处理[J]. 中南大学学报: 自然科学版, 2008,39(2): 276-277.WANG Na, MIN Xiao-bo, WANG Yun-yan. Determination of crosslinking agent in immobilized beads of SRB sludge with inner cohesive carbon source and treatment of wastewater containing zinc[J]. Journal of Central South University: Science and Technology, 2008, 39(2): 276-277.
[15] Postgate J R. Cultivation and growth in the sulphate-reducing bacteria[M]. Cambridge: Cambridge University Press, 1984.
[16] 魏复盛. 水和废水监测分析方法[M]. 北京: 中国环境学出版社, 2002: 436-440.WEI Fu-sheng. Water and wastewater monitoring analysis method[M]. Beijing: China Environmental Press, 2002:436-440.
[17] 张小里, 陈志昕, 刘海洪. 环境因素对硫酸盐还原菌生长的影响[J]. 中国腐蚀与防护学报, 2000, 20(4): 224-229.ZHANG Xiao-li, CHEN Zhi-xin, LIU Hai-hong. Effect of environment factors on the growth of Sulfate-reducing Bacteria[J]. Journal of Chinese Society For Corrosion and Protection, 2000, 20(4): 224-229.
[18] Kusel K, Roth U, Trinkwalter T. Effect of pH on the anaerobic microbial cycling of sulfur in mining-impactedfreshwater lake sediments[J]. Environmental and Experimental Botany, 2001,46(3): 213-223.
[19] 吴晓磊. 好氧及厌氧固定化微生物处理能力的比较研究[J].环境科学, 1994, 15(4): 50-52.WU Xiao-lei. Comparative study on the capacities of aerobic and anaerobic immobilized microbes to treat organics[J]Enviromental Science, 1994, 15(4): 50-52.
[20] 李盛贤, 刘松梅, 赵丹丹. 生物化学[M]. 哈尔滨: 哈尔滨工业大学出版社, 2005: 189-194.LI Sheng-xian, LIU Song-mei, ZHAO Dan-dan.Biochemistry[M]. Harbin: Harbin Institute of Technology Press,2005: 189-194.
[21] 沈仁权, 顾其敏, 李詠棠, 等. 基础生物化学[M]. 上海: 上海科学技术出版社, 1980: 172-176.SHEN Ren-quan, GU Qi-min, LI Yong-tang, et al. Basic biochemistry[M]. Shanghai: Shanghai Science and Technology Press, 1980: 172-176.
[22] 中国科学院贵阳地球化学研究所. 矿物X 射线粉晶鉴定手册[M]. 北京: 科学出版社, 1978: 53-57.Guiyang Institute of Geochemistry. Chinese Academy of Sciences. Mineral identification manual X-ray[M]. Beijing:Science Press, 1978: 53-57.
