联合检测TRACP5b和CA-153诊断早期乳腺癌骨转移及评价双膦酸盐治疗疗效的临床研究
2011-08-01薛小萍
薛小萍
(江苏省苏北人民医院临床医学检测中心,江苏扬州,225001)
早期乳腺癌骨转移患者可能无任何症状,一般只有到骨转移后期才出现一系列症状或并发症。血清抗酒石酸酸性磷酸酶5b(TRACP5b)主要来源于破骨细胞,是一个反映破骨细胞功能的指标[1]。糖类抗原-153(CA-153)为乳腺癌标志物。本文比较了健康女性、乳腺癌伴随或不伴随骨转移患者的T RACP5b及CA-153的血清水平,观察骨转移患者双膦酸盐治疗前后以上2种指标的改变,探讨TRACP5b和CA-153在早期乳腺癌骨转移及评价双膦酸盐治疗疗效中的临床价值。
1 资料与方法
45例患者均来自本院2010年5月~2011年6月乳腺癌根治术后的门诊及住院病例,均经组织学病理证实,手术当时无临床及影像学骨转移征象。年龄 19~74岁,平均50.3岁,其中,骨转移组28例,无骨转移组17例。23例健康女性血清为正常对照组。
样本采集:清晨取受试者外周血2 mL,室温放置30~40 min,待血液完全凝固后3 000 r/min条件下离心15 min,吸取血清至Eppel管中,置于-80℃冰箱中保存备测。
酶联免疫吸附法(ELISA)检测人血清TRACP5b,试剂由英国IDS公司生产,按说明书采用BIO-RAD Model 680酶标仪405 nm波长测定。电化学发光免疫法检测CA-153,仪器为BECKMAN COULTER Unicel DXI800,试剂为相应配套试剂,所有操作均严格按照说明书进行。
临界参考值:健康女性血清TRACP5b<4.15 U/L,CA-153正常参考值<31.1 U/mL,以超过限定值为阳性。
2 结 果
2.1 3组血清TRACP5b和CA-153检测结果比较
无骨转移组T RACP5b和CA-153浓度与健康对照组比较无统计学意义(P>0.05);骨转移组TRACP5b浓度明显高于健康对照组(P<0.05)和无骨转移组(P<0.05);骨转移组CA-153浓度明显高于健康对照组(P<0.05),但与无骨转移组比较无统计学意义(P>0.05)。见表1。
2.2 血清TRACP5b的活性随骨转移速度而改变,血清CA-153的浓度随骨转移速度改变不明显。见表2。
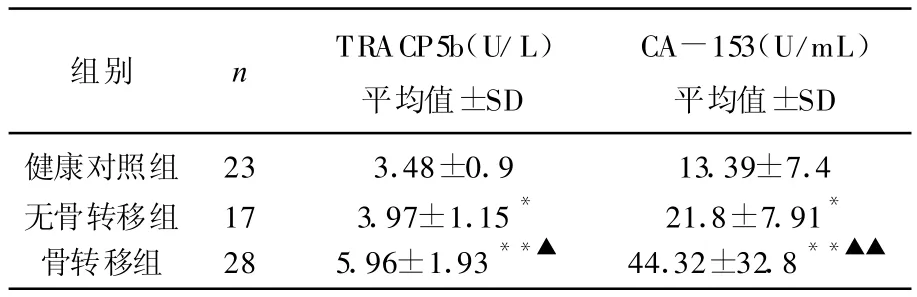
表1 血清TRAC P5b和CA-153在各组中的检测结果比较

表2 TRACP5b和CA-153活性随骨转移速度而改变
2.3 3组血清中TRACP5b和CA-153敏感性
及特异性比较(表3)
TRACP5b与CA-153相比,敏感度分别为78.57%、39.28%,有统计学意义(P<0.05),特异性分别为87.5%、77.5%,无统计学意义(P>0.05)。
2.4 骨转移患者双膦酸盐治疗前后血清
TRACP5b和CA-153水平变化(表3)
20名应用双膦酸盐治疗骨转移的患者,其治疗后血清TRACP5b和CA-153水平均较治疗前下降,但前者有统计学意义(P<0.05),后者无统计学意义(P>0.05)。

表3 骨转移患者双膦酸盐治疗前后血清TRACP5b和CA-153水平变化
3 讨 论
骨是乳腺癌最常见的远处转移部位之一,据文献报道80%的乳腺癌患者尸检发现均已发生骨转移。吴炅[2]等通过对20年内116例乳腺癌骨转移患者资料进行回顾性分析后指出:63.4%患者在手术后2年内发生骨转移,28.4%在手术后2-5年发生,7.8%发生于5年后。目前常通过临床症状、实验室检验(如CA-153和CEA等)以及影像学检查(如X线、ECT、CT和 MRI等)等方法诊断骨转移[3],但敏感性和特异性均不高。因此临床上一旦发现骨转移,预后较差,中位生存期一般为20~30个月,是严重危害患者生存质量和生命的原因[4]。
近几年,骨代谢的临床生化检查有了极大进步,相继发现了一些与骨转换密切相关的骨代谢标志物。这些标志物是在骨重塑的不同阶段由成骨细胞和破骨细胞产生、释放的蛋白质或骨基质降解产物[5],在肿瘤骨转移中,骨的重塑过程大大加快,骨代谢率增高,因此骨代谢标志物可以作为辅助诊断肿瘤骨转移的参考指标。血液循环中的TRACP有TRACP5b和TRACP5a两种形式,前者来自破骨细胞[6],后者来自巨噬细胞。由破骨细胞刚分泌到血液中的TRACP5b是有活性的酶,但在血液循环中被清除之前便已失去活性,并被降解成碎片。因此TRACP5b含量不受昼夜、饮食及肝肾功能受损的影响,体内水平波动小,重复性高[7-8],可以准确地反映破骨细胞的活性,反映骨吸收率。CA-153是一种高分子糖蛋白,为乳腺癌相关抗原,其在进展期和转移性乳腺癌患者阳性率较高,故CA-153被认为是一种相关性较高的乳腺癌标志物[9]。本研究结果显示TRACP5b在骨转移组水平显著高于无骨转移组和健康对照组,而CA-153在骨转移组及无骨转移组间无统计学差别,提示TRACP5b在预测乳腺癌骨转移方面的独特潜力;同时通过对非骨转移和骨转移的乳腺癌患者进行随访,本研究还发现TRACP5b在小面积癌症骨转移患者中就有升高,进一步证实了乳腺癌患者随访血清TRACP5b对早期发现乳腺癌骨转移具有较好的价值[10]和高度的敏感性。
双膦酸盐制剂是强有力的破骨细胞性骨溶解的抑制剂,选择性地吸附于骨组织,修复溶骨性病灶,减少或延缓肿瘤并发症的发生,从而减轻肿瘤引起的骨破坏,改善骨痛,而且是唯一可以降低骨折风险的药物[11]。本实验发现20例患者接受双磷酸盐制剂治疗后,影像学复查未发现骨转移病灶明显改变,但部分患者痛苦改善,20例患者TRACP5b和 CA-153水平均下降,且仅TRACP5b下降有统计学意义。故提示在双膦酸盐治疗过程中,可以通过T RACP5b的监测来确定其疗效和疗程。
目前临床上常用CA-153和CEA作为监测乳腺癌远处转移的血清指标,但以往研究提示:血清肿瘤标志物不同程度地易受多种内外因素的影响,比如性别、年龄、饮食、肾肝功能、昼夜等,以致各种标志物的值不断波动。TRACP5b是一个反映破骨细胞功能的标志物,所以针对乳腺癌80%均为以破骨细胞活动为主的溶骨性转移的特点,决定了TRACP5b在乳腺癌骨转移方面独特的检测潜力,加上其高度的敏感性、与骨转移药物治疗反应有很好的相关性等特点,相比较CA-153和CEA,如联合使用TRACP5b和CA-153综合评价预测乳腺癌骨转移,可以提高早期诊断及疗效监测的可靠性。
[1] Capeller B,Caffier H,Sutterlin M W,et al.Evaluation of tartrate-resistant acid phosphatase(TRAP)5b as serum marker of bone metastases in human breast cancer[J].Anticancer Res,2003,23(2A):1011.
[2] 吴 炅,邵志敏,沈坤炜,等.乳腺癌骨转移相关的临床病理因素的研究[J].中国癌症杂志,2003,13(4):316.
[3] Rougraff B T.Evaluation of the patient with carcinoma of unknown origin metastatic to bone[J].Clin Orthop,2003,415(suppl):105.
[4] Roodman G D.Mechanisms of bone metastasis[J].N Engl J Med,2004,350:1655.
[5] RAMANKULOV A,LEIN M,KRISTIANSEN G,et al.Plasma osteopontin in comparison with bone markers as indicator of bone metastasis and survival outcome in patients with prostate cancer[J].Prostate,2007,67(3):330.
[6] Janckila A J,Neustadt D H,Nakasato Y R,et al.Serum tartrate-resistant acid phosphatase isoforms in rheumatoid arthritis[J].Clin Chim Acta,2002,320:49.
[7] Halleen J M,Alatalo S L,Janckila A J,et al.Tartrate-resistant acid phosphatase 5b is a specific and sensitive marker of bone resorption[J].Clin chem,2001,47:597.
[8] Nowak Z,Konieczna M,Wankowicz Z,et al.Tartrate-resistant acid phosphatase-TRAP5b as a novel marker of bone resorption in patients with irreversible renal failure treated with dialysis[J].Pol Merkuriusz Lek,2004,17(98):138.
[9] 宋恕平,杨锡贵,陈 陈.临床肿瘤转移学[M].济南:山东科技出版社,2001:195.
[10] CHAO T S,YU J K,KU C H,et al.Tartrate-resistant acid phosphatase 5b is a useful serum marker for extensive bone metastasis in breast cancer patients[J].Clin Cancer Res,2005,11(2ptl):544.
[11] Watts N B.Bisphosphonate treatment of osteoporosis[J].Clin Geriatr Med,2003,19(2):395.
