消癌平片微生物限度检查法验证
2011-07-30陆娟陈建玲
陆娟,陈建玲
(湖北省襄阳市食品药品检验所,441021)
消癌平片是一种抗癌、消炎、平喘药,主要成分是乌骨藤,临床多用于食道癌、胃癌、肺癌等多种恶性肿瘤。本品具有一定的抑菌作用,用常规方法对其进行微生物限度检查时,结果不能真实反映样品的污染情况。按《中华人民共和国药典》2010年版规定,在进行微生物限度检查时,应对所用方法进行验证,以确认所采用的方法适合该产品,准确有效地检出样品中污染的微生物[1]。按照《中国药品检验标准操作规范》[2]及参考有关文献[3-6],笔者采用培养基稀释法进行验证,报道如下。
1 仪器与试药
1.1 仪器 立式灭菌器(山东新华医疗器械股份有限公司),HTY-761型匀浆仪(杭州泰林生物技术设备有限公司),202-2型电热恒温干燥箱(上海浦东跃欣科学仪器厂),SPX-150生化培养箱(慧科电子有限公司),生物安全柜(苏净安泰)。
1.2 菌种 大肠埃希菌[CMCC(B)44102],金黄色葡萄球菌[CMCC(B)26003],枯草芽孢杆菌[CMCC(B)63501],白念珠菌[CMCC(F)98001],黑曲霉[CMCC(F)98003]。
1.3 培养基及稀释剂 营养琼脂培养基、玫瑰红钠琼脂培养基、营养肉汤培养基、胆盐乳糖培养基(BL)、胆盐乳糖发酵培养基、乳糖发酵培养基、改良马丁培养基、改良马丁琼脂培养基、4-甲基伞形酮葡糖苷酸培养基,以上均由北京三药科技开发公司提供。含0.05%聚山梨酯80的0.9%无菌氯化钠溶液,0.9%灭菌氯化钠溶液,pH7.0无菌氯化钠-蛋白胨缓冲液,新配。
1.4 供试品 消癌平片(湖北创力药业有限公司,批号:20101101,20101201,20110101)。
2 方法与结果
2.1 菌液的制备
2.1.1 大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌菌液 取营养琼脂斜面新鲜培养物,接种于营养肉汤培养基中,30~35℃培养18~24 h;用0.9%无菌氯化钠溶液稀释制成每毫升含菌数为50~100 cfu的菌悬液。
2.1.2 白念珠菌菌液 取新鲜培养物接种于改良马丁培养基23~28℃培养24~48 h,用0.9%无菌氯化钠溶液稀释制成每毫升含菌数为50~100 cfu的菌悬液。
2.1.3 黑曲菌液 取新鲜培养物,接种至改良马丁琼脂斜面培养基中,23~28℃培养5~7d,用含0.05%聚山梨酯80的无菌0.9%氯化钠溶液8mL将孢子洗脱,吸出孢子悬液至无菌试管中,用含0.05%聚山梨酯80的无菌0.9%氯化钠溶液稀释制成每毫升含孢子50~100 cfu的孢子悬液。
2.2 供试液制备 取供试品10 g,加pH7.0无菌氯化钠-蛋白胨缓冲液至 100mL,用匀浆仪以2 000 r·min-1的转速旋转30 s,制备成1∶10的供试液。
2.3 回收率测定
2.3.1 实验组 常规法:取供试液和实验菌液各1mL,分别注入平皿,立即倾入相应培养基,摇匀待凝固后按规定条件培养,每日观察计算菌落数,每种实验菌平行制备2个平皿,结果见表1。
培养基稀释法:取供试液0.2mL和实验菌液1mL分别注入平皿,立即倾入相应培养基,摇匀待凝固后按规定条件培养,每日观察计算菌落数,每种实验菌平行制备10个平皿,结果见表2。
2.3.2 菌液组 取上述实验菌液按常规法测定每一种菌株所加的实验菌数。
2.3.3 供试品对照组 常规法:取供试液1mL注入平皿,立即倾入相应培养基,摇匀待凝固后按规定条件培养,每日观察计算菌落数,每种实验菌平行制备2个平皿,结果见表1。培养基稀释法:取供试液0.2mL注入平皿,立即倾入相应培养基,摇匀待凝固后按规定条件培养,每日观察计算菌落数,每种实验菌平行制备10个平皿,结果见表2。
2.3.4 稀释剂对照组 用相应稀释剂代替供试液加入实验菌,使菌液最终浓度为50~100 cfu·mL-1按实验组方法进行菌落计数。
2.3.5 结果判断 回收率(%)=(实验组平均菌落数-供试品对照组平均菌落数)/菌液组平均菌落数×100%。
2.4 控制菌检验验证
2.4.1 实验组 取1∶10供试液10mL接种至100mL胆盐乳糖培养基中,同时加入50~100 cfu·mL-1大肠埃希菌菌液1mL,35℃培养24 h,取培养物0.2mL,接种至含MUG培养基5mL的试管中,35℃培养,5,24 h在366 nm紫外光灯下观察,管内培养物呈现蓝白荧光,为MUG阳性;然后进行靛基质实验,液面呈玫瑰红色,为靛基质阳性。
2.4.2 阴性菌对照组 方法同实验组,实验菌为金黄色葡萄球菌菌液。结果管内培养物不呈现荧光,为MUG阴性;然后进行靛基质实验,液面呈试剂本色,为靛基质阴性。

表1 常规法回收率测定结果
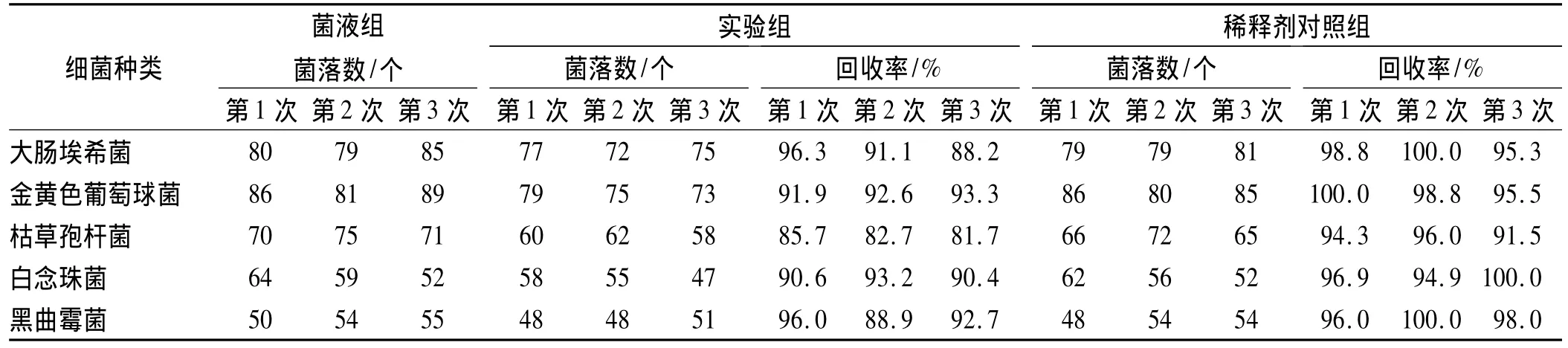
表2 培养基稀释法回收率测定结果
2.4.3 供试品对照组 方法同实验组,但不加实验菌,结果同阴性菌对照组。
2.4.4 结果判断 实验组检出实验菌,阴性菌对照组未检出实验菌,结果符合要求,控制菌按常规法检查即可。
3 讨论
消癌平片的微生物限度检查验证实验中,稀释剂对照组各菌落计数回收率均>70%;常规法菌落计数大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌回收率<70%;培养基稀释法各菌落计数回收率均>70%,按供试品制备方法和培养基稀释法对消癌平片进行细菌检查,真菌和酵母菌检查、控制菌检查采用常规法是固定可行的。
实验制备计数用的菌液稀释到合适的浓度后,菌落数在48 h后有较大变化,宜控制好实验时间,实验的同时进行活菌计数,才能保证实验结果的准确性。
目前国家越来越重视微生物限度检查,《中华人民共和国药典》收载的品种也越来越多。《中华人民共和国药典》从2005年版开始对微生物限度检查要求进行方法学的验证实验。由于某些供试品具有抗菌或抑菌活性,其本身会影响检验结果的准确性。通过方法学验证,避免了采用常规方法难以检出菌落,而得出“阴性”或计数偏低的“合格”结论的情况。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:附录C 79-88.
[2]中国药品生物制品检定所,中国药品检验总所.中国药品检验标准操作规范[M].北京:中国医药科技出版社,2010:351-407.
[3]颜栋林,李萍,兰茜.冠心丹参片微生物限度检查法方法验证[J].医药导报,2010,29(8):1080-1081.
[4]张丽梅,李俊,邢建华.抗生丸微生物限度检查法的验证[J].医药导报,2009,28(6):792-793.
[5]李俊,张丽梅.6种中成药微生物限度检查方法验证[J].医药导报,2010,29(9):1222-1223.
[6]马绪荣,苏德模.药品微生物学检验手册[M].北京:科学出版社,2000:65.
