巨大芽孢杆菌Bacillus megaterium NCIB 8508蔗糖磷酸化酶生物催化合成α-熊果苷的研究
2011-07-25李群良张欣英杨克迪姚评佳魏远安
李群良,张欣英,杨克迪,姚评佳,魏远安
(1.广西大学化学化工学院,广西 南宁530004; 2.广西大学广西亚热带生物资源保护利用重点实验室,广西 南宁530004)
熊果苷(Arbutin),又名熊果甙、熊果素、熊果叶甙、熊果酚甙或杨梅甙,是一种源于杜鹃花科熊果属的多年生常绿小灌木植物熊果叶子细胞里的成分,具有良好的皮肤美白效果,广泛应用于化妆品行业[1]。
熊果苷的制备方法有天然产物提取法、植物组织培养法、化学合成法以及酶转化法[2]。生物酶法主要以糖基转移酶或糖苷酶作为催化剂,通过催化糖基转移或逆水解反应合成熊果苷,其中转糖基反应中酶底物为双糖或多糖。糖基转移酶能特异地催化糖基从糖基供体如UDPG衍生物转移到目标产物,催化效率较高[3]。迄今为止已发现Leuconostocmesenteroides、Bacillussubtilis、Bacillusmacerans、Saccharomycescerevisiae、Rhizopussp.以及Xanthomonascampestris等微生物细胞能转化合成熊果苷[4]。Wu等[5]研究了高密度细胞培养大肠杆菌表面锚定转糖基酶作为全细胞生物催化剂合成α-熊果苷。Kitao等[6]首次报道了用Leuconostocmesenteroides蔗糖磷酸化酶转化合成α-熊果苷。通过蔗糖磷酸化酶催化合成的熊果苷只有α-熊果苷,相比β-熊果苷,其美白效果高10倍以上,且不抑制人体细胞[7]。利用蔗糖磷酸化酶催化合成α-熊果苷具有专一性强、产品纯度高及生产条件温和等优点,因此意义重大。
在前期研究中,作者首次验证并鉴定了巨大芽孢杆菌BacillusmegateriumNCIB 8508中存在蔗糖磷酸化酶[8],在此对该蔗糖磷酸化酶催化蔗糖与对苯二酚合成α-熊果苷进行了初步研究,其反应式如下:

1 实验
1.1 菌株、试剂与培养基
巨大芽孢杆菌BacillusmegateriumNCIM 2087(即巨大芽孢杆菌BacillusmegateriumNCIB 8508)购于印度浦那国家化学实验室(National Chemical Laboratory,Pune 411008,India)。
α-熊果苷标准品购自Sigma 公司,其它试剂为生化试剂。
种子培养基:葡萄糖2 g,蛋白胨1.5 g,NaCl 0.5 g,牛肉膏0.05 g,蒸馏水100 mL,pH值7.0。
1.2 蔗糖磷酸化酶粗酶液的制备
无菌操作下,取一环菌株于种子培养液中发酵培养8 h,吸取发酵液分装到新种子培养液中培养48 h,8000 r·min-1冷冻离心20 min后收集菌体,用缓冲溶液洗涤菌体2次,超声破碎细胞,离心,取上清液即为胞内粗酶液。
1.3 α-熊果苷的生物合成
取上述胞内粗酶液5 mL(其中湿菌体浓度为50 mg·mL-1),加入反应物蔗糖和对苯二酚,30℃、180 r·min-1摇床反应24 h。取1 mL反应液,离心取上清液进行高效液相色谱检测。对苯二酚的转化率(x1)和选择性(x2)依下式计算:
式中:M1为加入到反应液中的对苯二酚摩尔量;M2为反应消耗掉的对苯二酚摩尔量;M3为对应生成α-熊果苷的对苯二酚摩尔量。
1.4 高效液相色谱检测条件
色谱条件:色谱柱为DiamonsilTMC18柱,5 μm,250 mm×4.6 mm; 柱温25℃; 流动相为H2O ∶CH3OH = 95∶5;流速1 mL·min-1;检测器为紫外检测器;检测波长280 nm;进样量10 μL。
2 结果与讨论
2.1 缓冲溶液pH值对反应的影响
在反应底物对苯二酚浓度为5 mmol·L-1、对苯二酚与蔗糖摩尔比为1∶4的条件下,考察缓冲溶液pH值对反应的影响,结果见图1。

图1 缓冲溶液pH值对反应的影响
从图1可知,当缓冲溶液pH值为6.5时,α-熊果苷含量最大,对苯二酚的选择性达到最高、转化率也较高,这说明在pH值为6.5的缓冲溶液反应体系中,转糖基作用最佳,且残余对苯二酚量最少。这与Nomura等[9]报道的一致,当蔗糖磷酸化酶催化反应中受体为氢醌一族时,转糖基作用的最适pH值偏中性。
2.2 缓冲溶液浓度对反应的影响
考察磷酸盐缓冲溶液(pH值为6.5)浓度对反应的影响,结果见图2。

图2 缓冲溶液浓度对反应的影响
从图2可知,缓冲溶液浓度对α-熊果苷含量影响不是很明显,缓冲溶液浓度达到30 mmol·L-1时,α-熊果苷含量最大,此时对苯二酚的选择性也达到最高,但其转化率相对最低。
2.3 对苯二酚浓度对反应的影响
50 mg·mL-1湿菌体所含蔗糖磷酸化酶量为定值,底物的起始浓度较低时,蔗糖磷酸化酶催化反应速度与对苯二酚浓度成正比,即生成的α-熊果苷量随对苯二酚浓度的增加而增大;但当对苯二酚浓度超过一定值时,催化反应生成的α-熊果苷量不再随着对苯二酚浓度的增加而增大。考察对苯二酚浓度对反应的影响,结果见图3。

图3 对苯二酚浓度对反应的影响
从图3可知,对苯二酚的选择性和转化率均随着其浓度的增加先升高后降低,当对苯二酚浓度为5 mmol·L-1时,α-熊果苷含量最大,对苯二酚的选择性与转化率也达到最高。
2.4 反应物摩尔比对反应的影响
本实验通过增加蔗糖的量来提高对苯二酚的转化率,从而提高α-熊果苷的产量。考察反应物摩尔比(对苯二酚与蔗糖摩尔比,下同)对反应的影响,结果见图4。
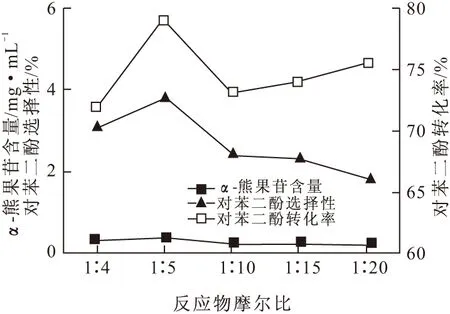
图4 反应物摩尔比对反应的影响
从图4可知,对苯二酚与蔗糖的摩尔比为1∶5时,α-熊果苷含量最大,对苯二酚的选择性与转化率也达到最高;继续增加蔗糖的量,对苯二酚的选择性与转化率反而有所下降。
2.5 反应时间对反应的影响
考察反应时间对反应的影响,结果见图5。

图5 反应时间对反应的影响
从图5可知,反应时间为24 h时,对苯二酚的选择性及α-熊果苷含量达到最高;继续延长反应时间,对苯二酚的选择性及α-熊果苷含量逐渐下降,而对苯二酚转化率则逐渐上升,这可能与粗酶液中含有其它催化酶有关。
3 结论
采用巨大芽孢杆菌BacillusmegateriumNCIB 8508蔗糖磷酸化酶催化合成α-熊果苷,确定最佳反应条件如下:湿菌体50 mg·mL-1破碎细胞粗酶液催化合成α-熊果苷,pH值为6.5的磷酸盐缓冲溶液浓度为30 mmol·L-1,反应温度为30℃,摇床转速为180 r·min-1,对苯二酚浓度为5 mmol·L-1,对苯二酚与蔗糖摩尔比为1∶5,反应时间为24 h。在此条件下,α-熊果苷含量达0.35 mg·mL-1,对苯二酚选择性为4.0%,对苯二酚转化率为74%。
由于实验用酶为蔗糖磷酸化酶粗酶液,酶含量少,其催化合成α-熊果苷相对有限,致使反应物选择性较低。为了进一步提高α-熊果苷产量,今后研究中可利用分子生物学方法构建高表达蔗糖磷酸化酶基因的工程菌,以获得酶活力高、稳定性好的蔗糖磷酸化酶用于α-熊果苷的生产。
[1] 郭静,徐平,金立元.熊果苷的研究进展[J].宁夏医学杂志,2008,30(3):281-283.
[2] 郭起,陈朗秋,蔡进,等.熊果苷的合成新方法[J].化学试剂,2010,32(1):17-20.
[3] 周防震,郭勇.生物转化生产熊果苷的研究进展[J].安徽农业科学,2009,37(26):12393-12394,12396.
[4] 梁晓夏,庞宗文,梁静娟,等.生物催化合成熊果苷的微生物的筛选研究[J].现代食品科技,2007,23(7):22-25,31.
[5] Wu P H,Nair G R,Chu I M,et al.High cell density cultivation ofEscherichiacoliwith surface anchored transglucosidase for use as whole-cell biocatalyst for alpha-arbutin synthesis[J].Journal of Industrial Microbiology and Biotechnology,2008,35(2):95-101.
[6] Kitao Satoshi,Sekine Hiroshi.α-D-Glucosyl transfer to phenolic compounds by sucrose phosphorylase fromLeuconostocmesenteroidesand production ofα-arbutin[J].Bioscience Biotechnology and Biochemistry,1994,58(1):38-42.
[7] 侯顾伟,马江锋,隋姗姗,等.蔗糖磷酸化酶制备及应用的研究进展[J] .中国酿造,2010,(6):17-20.
[8] 李群良,张欣英,姚评佳,等.巨大芽孢杆菌BacillusmegateriumNCIB 8508蔗糖磷酸化酶的分离鉴定[J].化学与生物工程,2010,27(12):61-64.
[9] Nomura K,Sugimoto K,Nishiura H,et al.Glucosylation of acetic acid by sucrose phosphorylase[J].Bioscience Biotechnology and Biochemistry,2008,72(1):82-87.
