大黄酚固体分散体的制备及体外溶出研究
2011-07-25王彦雪郭肖菲
韩 刚, 刘 莉, 康 欣, 王彦雪, 赵 媛, 肖 倩, 郭肖菲
(华北煤炭医学院药学系,河北省煤矿卫生与安全重点实验室,河北唐山063000)
大黄酚(chrysophanol)是中药大黄的主要活性成分之一,具有抗菌、止咳、止血、抗脂质过氧化、抗衰老等多种药理作用[1-2]。但大黄酚不溶于水,微溶于乙醇等有机溶剂,体内吸收差,生物利用度低[3]。改进难溶性药物溶出度的方法较多,其中利用固体分散技术较为常用[4-5]。本实验以聚乙二醇6000为载体,制备了大黄酚固体分散体,考察了大黄酚固体分散体在体外的溶出性质。
1 仪器与材料
D/max-rc型X-射线分析仪器(日本Rigaku公司);DSC-60差示扫描量热仪(日本Shimadzu公司);1100高效液相色谱仪(美国 Agilent公司);BT-125D电子天平(Sartorius公司);气浴恒温振荡器(江苏金坛市荣华仪器公司);RCZ-8A药物溶出仪(天津大学精密仪器厂)。
大黄酚对照品(中国药品生物制品检定所,供定量测定用,批号:110796-200716);大黄酚原料药(南京泽朗有限公司,纯度>97%);聚乙二醇6000(PEG)、聚乙烯吡咯烷酮(PVP)(北京化学试剂厂);甲醇为色谱纯(Fisher公司);其余试剂均为分析纯。
2 方法与结果
2.1 供试品的制备
2.1.1 大黄酚-PEG固体分散体的制备 将大黄酚溶解于适量四氢呋喃中,再加入适量95%乙醇制成大黄酚溶液,将PEG6000加热熔融,将大黄酚溶液倒入熔融的PEG6000中搅拌均匀,室温冷却。按上述方法制备大黄酚与PEG6000质量比为1∶2、1∶4、1∶6的固体分散体备用。
2.1.2 大黄酚-PVP固体分散体的制备 将大黄酚与载体PVP分别按质量比1∶2、1∶4、1∶6的比例,加入适量的无水乙醇使其完全溶解,溶液转入旋转蒸发仪中,60℃将溶剂蒸干,得大黄酚-PVP固体分散体,备用。
2.1.3 物理混合物的制备 将大黄酚与载体PVP、PEG分别按质量比1∶2、1∶4、1∶6的比例研细,过60目筛即得不同载体,不同比例的大黄酚与载体的物理混合物。
2.2 大黄酚测定
2.2.1 色谱条件 色谱柱:Agilent extend-C18柱(150 mm×4.6 mm,5 μm);流动相:甲醇-水-冰醋酸(77 ∶22 ∶1);体积流量 1.0 mL/min;柱温:室温;检测波长:428 nm[5];进样量:20 μL。
2.2.2 标准曲线的绘制 准确称取干燥后的大黄酚对照品约3 mg于25 mL量瓶中,甲醇定容即为大黄酚对照品溶液。取对照品溶液适量,分别稀释成 0.1、1.0、2.5、4.0、8.0、10.0、15.0、20μg/mL,20μL 进样,测定大黄酚的峰面积 A,以大黄酚质量浓度C对峰面积A进行回归,得回归方程:A=35.76C-6.58,r=0.9994,线性范围 1 ~20 μg/mL。
2.2.3 精密度实验 分别准确称取干燥后的大黄酚-PVP固体分散体、大黄酚-PEG固体分散体各约4 mg,分别置于25 mL量瓶中,甲醇溶解,即为供试品溶液。取供试品溶液于同日内连续进样6次测定 (时间间隔为2 h),测得大黄酚-PVP固体分散体的RSD为1.44%,大黄酚-PEG固体分散体RSD为1.78%,表明所建立的大黄酚测定方法重复性良好。
2.2.4 回收率实验 分别准确称取大黄酚-PVP固体分散体、大黄酚-PEG固体分散体约4 mg,各9份,分别置于25 mL量瓶中,分别精密加入大黄酚对照品溶液适量,制成低、中、高3种质量浓度的供试品溶液,20 μL进样,测定大黄酚的峰面积,计算大黄酚-PVP固体分散体低、中、高3种质量浓度的回收率分别为 97.52%、98.60%、98.75%;大黄酚-PEG固体分散体低、中、高3种浓度的回收率分别为99.11%、101.4%、99.73%,表明建立的大黄酚测定方法回收率良好。
2.3 样品溶解度测定 在具塞三角烧瓶中分别加入10 mL人工肠液,分别加入过量的大黄酚、大黄酚固体分散体、大黄酚与不同载体的物理混合物,置于气浴振荡器中,37℃振荡72 h,0.45μm微孔滤膜过滤,进样测定大黄酚的峰面积,根据标准曲线计算溶解度。见表1。

表1 样品的溶解度(37℃)
2.4 样品溶出度测定 照2010年版《中国药典》二部附录XC第一法测定溶出度[7],以900 mL含0.2%十二烷基硫酸钠人工肠液为溶出介质,温度(37±0.5)℃,转速100 r/min。取各处方固体分散体适量,取大黄酚、大黄酚与载体的物理混合物适量(相当于含大黄酚 3.5 mg),分别于 3、6、10、15、20、30、40、60 min 取样 2 mL,立即用 0.45μm 微孔滤膜过滤,同时补充等温度等体积溶出介质。20μL进样测定,将测定换算成累积溶出百分率。
2.5 载体的选择 以聚乙二醇6000为载体制备的大黄酚固体分散体其溶出速率较大黄酚原料药均提高,其中以PEG 6000为载体制得的固体分散体效果最好,40 min内累积溶出百分率达70%,明显高于PVP固体分散体,故选用聚乙二醇6000为载体。见图1。
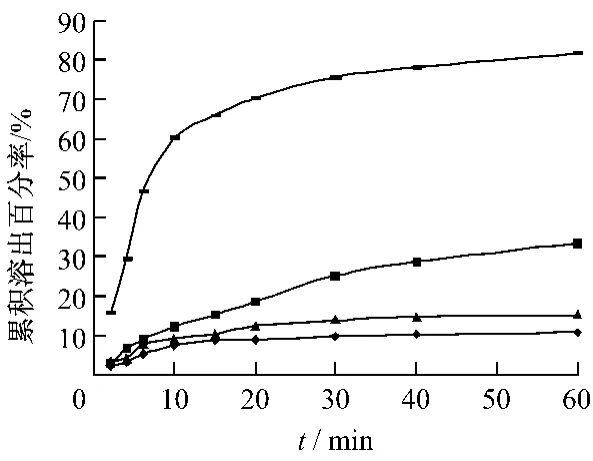
图1 不同载体制备固体分散体溶出度曲线
2.6 载体比例的选择 分别取1∶2、1∶4、1∶6大黄酚-PEG固体分散体,测定大黄酚固体分散体的体外溶出度,如图2所示,大黄酚与载体质量比为1∶4时,40 min内大黄酚累积溶出百分率达70%。从溶出度曲线可知,大黄酚与PEG载体以1∶4比例形成的固体分散体最好,故选用大黄酚-PEG固体分散体(1∶4)的样品进行X射线衍射和差热分析。

图2 不同比例大黄酚-PEG固体分散体的溶出曲线
2.7 样品差示扫描量热(DSC)分析[8]取 PEG6000、大黄酚、大黄酚-PEG固体分散体(1∶4)、大黄酚与PEG物理混合物(1∶4)分别进行差示扫描量热(DSC)分析。测定条件:空铝坩埚为参比,气氛为N2,升温范围20℃ ~250℃,升温速率10℃/min。结果见图3。

图3 大黄酚(a),大黄酚-PEG固体分散体(b),大黄酚与PEG物理混合物(c),PEG(d)的DSC图
2.8 样品的X射线衍射分析 取大黄酚PEG固体分散体进行X射线衍射分析,测试条件为CuKa石墨单色器衍射,管流:20 mA,高压:30 kV,掠角 θ为5 ~35°。见图4、5。

图4 大黄酚

图5 大黄酚固体分散体
3 讨论
差示扫描量热(DSC)分析结果显示,大黄酚在196℃有一吸热峰,为大黄酚的熔点峰,与文献报道一致[9]。PEG6000在75℃有一吸热峰[10]。在大黄酚与PEG 6000的物理混合物中大黄酚的吸热峰仍存在,说明载体与大黄酚的机械混合虽然可以使药物的结晶有所减少但是药物依然以原来的晶型存在,在大黄酚与PEG 6000形成的固体分散体中大黄酚196℃处的吸热峰完全消失,说明大黄酚与载体发生相互作用,使药物结晶结构发生改变,大黄酚在固体分散体中以无定形形式存在,从而增加了大黄酚的分散程度,提高了大黄酚的体外溶出度。由图4可见,大黄酚的晶体衍射峰清晰可辨。而固体分散体的衍射图仅为一宽带,说明在固体分散体中,大黄酚的晶体已完全消失,而以无定形状态分散于非晶体的PEG中,从而达到高度分散状态(见图5)。
体外溶出实验显示,大黄酚固体分散体的溶出度大于物理混合物,大于大黄酚,并且大黄酚与PEG 6000的比例为1∶4时大黄酚固体分散体溶出度最大。
以聚乙二醇6000为载体将大黄酚制成固体分散体可增加大黄酚的溶解度,改善大黄酚的溶出度。
[1]Lu C C,Yang J S,Huanq A C,et al.Chrysophanol induces necrosis through the production of ROS and alteration of ATP levels in human liver cancer cells[J].Mol Nutr Food Res,2010,18(12):264-269.
[2]张丹参,张 力,薛贵平,等.大黄酚的抗衰老作用[J].中国医院药学杂志,2005,25(1):15-17.
[3]Zhao X,Zheng Z,Feng S,et al.A TD-DFT study on the photophysicochemical properties of chrysophanol from rheum[J].Int J Mol Sci,2009,10(7):3186-3193.
[4]Joe J H,Lee W M,Park Y J,et al.Effect of the solid-dispersion method on the solubility and crystalline property of tacrolimus[J].Int J Pharm,2010,21(5):5216-5220.
[5]Silav T D,Arantes V T,Resende J A,et al.Preparation and characterization of solid dispersion of simvastatin[J].Drug Dev Ind Pharm,2010,14(6):312-317.
[6]韩 刚,安 静,孙海燕.通脉降脂胶囊质量标准的建立[J].中成药,2005,27(7):778-780.
[7]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[8]何 丹,杨 林,贺浪冲.白芷香豆素固体分散体的制备及溶出特性研究[J].中成药,2006,28(1):20-23.
[9]张黎明,王玲玲,赵 希.大黄酚和大黄素甲醚的热分析与X-射线衍射图谱特征[J].药物分析杂志,2009,29(2):257-260.
[10]严瑞暄.水溶性高分子[M].北京:化学工业出版社,2001:633-642.
