微生物絮凝剂XM09与PAC复配处理生活污水
2011-07-19刘云洁
王 兰,唐 静,刘云洁
(南开大学环境科学与工程学院,天津 300071)
絮凝剂,特别是人工合成的化学絮凝剂,已广泛应用于物质的固液分离过程,如给水处理、废水处理、食品加工与发酵过程等 .目前,用于废水处理相分离的絮凝剂分无机、有机和生物 3类.聚合氯化铝(polyaluminum chloride.PAC)等无机絮凝剂一般用量大且易产生二次污染;聚丙烯酰胺等人工合成有机絮凝剂的单体往往是“三致”物质且具有不可生物降解性;而微生物絮凝剂是由微生物产生的代谢产物,有良好的絮凝沉淀性能,安全、无毒、可生物降解,具有广阔的应用前景.近年来,对微生物絮凝剂有大量的研究,并已取得了一些初步成果,为其在城市生活污水中的应用奠定了理论基础.但微生物絮凝剂产量低、成本高等问题严重制约着其广泛应用.因此,有研究者重点研究了微生物絮凝剂与其他絮凝剂的配合使用,一方面能够显著提升微生物絮凝剂的絮凝能力,扩展絮凝对象的范围,提高絮凝条件的适应性,改善絮体沉降状态;另一方面通过减少微生物絮凝剂的投加量降低其使用成本,同时降低传统絮凝剂中有害物质所造成的二次污染风险[1-2].
国内关于微生物絮凝剂与化学絮凝剂复配使用处理废水的报道比较少,而与处理生活污水常用的化学絮凝剂进行复配处理后对水中残留铝影响的研究则更少.笔者以微生物絮凝剂XM09为主体,复配使用少量的 PAC,进行生活污水的絮凝预处理过程,并获得最佳的复配比例.同时还考察了不同 XM09投加量对水中残留铝的影响,以评价复配絮凝剂的使用安全性.
1 材料与方法
1.1 材料
1.1.1 菌种来源及培养基
试验菌种来源于天津市某污水处理厂活性污泥,经筛选、纯化,得到高效稳定的絮凝剂产生菌 M09,经鉴定为酱油曲霉(Aspergillus sojae).
培养基:NaNO33,g,KCl,0.5,g,K2HPO4,1,g,FeSO4,0.01,g,MgSO4·7H2O,0.5,g,蔗糖 20,g,水1,000,mL,pH值为,6.121,℃高压蒸汽灭菌20,min.
1.1.2 生活污水
天津市纪庄子污水处理厂的一沉池水,废水中悬浮颗粒物较多,呈淡黄色,较浑浊,OD550为 0.2~0.3,pH 为 7.0.
1.2 方法
1.2.1 微生物絮凝剂的制备
用无菌水洗下 M09菌斜面上的孢子,制成 107个/mL的孢子悬液,按 1%的接种量接入灭过菌的第1.1.1节中的培养基中,在 28,℃、150,r/min条件下振荡培养 60,h.所得发酵液即为本实验所采用的微生物絮凝剂XM09.
1.2.2 XM09成分分析
取1,L发酵液进行过滤去菌体,得到上清液,然后加入其3倍体积的无水乙醇在4,℃条件下沉淀12,h,5,000,r/min离心 40,min获得沉淀,用蒸馏水重新溶解,重复上述操作,最后收集沉淀,再用无水乙醇反复洗涤沉淀物,在 40,℃下低温干燥,最终得到微生物絮凝剂固体产品.
利用糖和蛋白质显色反应[3]来判断上述所提纯产品的主要成分.采用红外光谱扫描,判定成分里所含有的官能团.通过成膜实验[4]判定絮凝剂分子的分子构型.
1.2.3 XM09(或PAC)处理生活污水
取生活污水 60,mL,置 100,mL烧杯中,加入不同量的 XM09(或 PAC),然后在 JJ-4型四联电动搅拌器上进行搅拌混匀,快速搅拌(400,r/min)1,min,慢速搅拌(50,r/min)5,min,静置 5,min后取上清液在550,nm 波长下测定吸光度值.以蒸馏水代替 XM09(或PAC)做空白对照,用样品分别做3次平行试验.
絮凝活性用絮凝率F来表征,其计算方法为
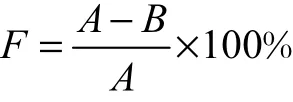
式中:A为对照上清液的吸光度;B为样品上清液的吸光度.
1.2.4 XM09与PAC复配处理生活污水
根据试验所得 XM09和 PAC各自的最佳添加量,进行正交试验,以确定最佳的复配比例,并获得最优的絮凝效果.
运用铬天青S分光光度法[5],测定处理后水中总铝的含量.通过分别考察不同絮凝条件、XM09的投加量对水中残留铝的影响,以评价复配絮凝剂的使用安全性.
2 结果与讨论
2.1 微生物絮凝剂XM09的成分分析
经第 1.2节的方法进行微生物絮凝剂的制备和提纯,可从1,L发酵液中分离纯化得到0.35,g絮凝剂,XM09质量浓度为0.35,g/L.
对提纯产物进行糖和蛋白质的显色反应,结果表明微生物絮凝剂 XM09的主要成分为多糖,不含有蛋白质.
为了进一步验证显色反应的结果,进行了红外光谱扫描,结果见图1.从图1中可以看出:特征吸收峰为 3,388,cm-1、1,670,cm-1、1,331,cm-1、1,078,cm-1、877,cm-1和 553,cm-1,这表明分子中具有多糖的特征基团.其中3,388,cm-1为一宽吸收峰,是多糖—OH伸展振动的结果;1,670,cm-1处的吸收峰是由多糖的羧基C=O伸缩振动所致;1,331,cm-1处的小吸收峰是醇中—OH伸缩振动及 C—H面内弯曲振动的结果;1,078,cm-1又为一较宽吸收峰,为多糖环中醚C—O的特征吸收峰,同时也证明了—CH3O的存在[6];877,cm-1处的吸收峰证明了C—H的面外摇摆振动,同时也证明了β-糖苷键的存在;553,cm-1证明了C=O扭曲振动的存在[6].Gong等[7]也提到 1,000~1,200,cm-1处的吸收峰是所有已知糖类的特征峰.因此从以上所有的峰显示,该物质主要成分应该是多糖,且富含羟基和羧基.文献[8-9]表明,羟基和羧基官能团在微生物絮凝剂的絮凝过程中起着关键的作用.
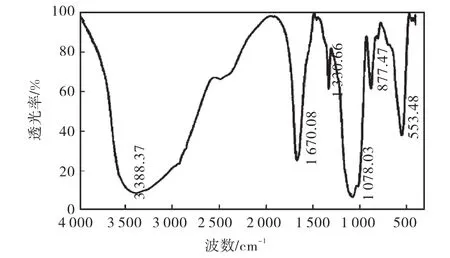
图1 微生物絮凝剂XM09的红外光谱Fig.1 Infrared spectrum of microbial flocculant XM09
成膜实验表明,微生物絮凝剂风干后会形成一层韧性很强的薄膜,这从一定程度上说明 XM09分子构型是线性的.一般认为,与非线性分子相比,线性分子在溶液中的伸展有效长度更长,在溶液中同胶体颗粒能够更充分接触,以便捕集胶粒,更好地起到架桥的作用,因此絮凝性更高[10].
2.2 XM09对生活污水的处理效果
2.2.1 单独使用XM09处理生活污水
XM09对生活污水的絮凝效果见图2.从图2可知,XM09的投加量在2~30,mg/L范围内时,絮凝率是随着投加量的增加而不断提高的,而当投加量超过30,mg/L时,絮凝率则增加缓慢,逐渐趋于稳定,此时的絮凝率为 87.74%.这是因为当微生物絮凝剂的投加量过少时,不能形成有效的絮体,或絮体颗粒粒径过小,无法克服浮力作用而下降,从而无法起到卷扫作用,故往往上清液较为浑浊,絮凝率较低;当絮凝剂过多时,絮凝剂与胶体颗粒达到结合的饱和状态,故絮凝率趋于稳定.
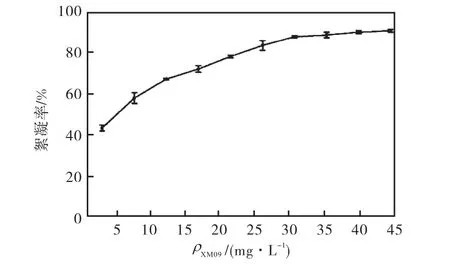
图2 XM09对生活污水的絮凝效果Fig.2 Effect of XM09 on domestic wastewater
2.2.2 单独使用PAC处理生活污水
PAC对生活污水的絮凝效果见图3.从图3可以看出,在较小的 PAC投加量范围内,絮凝率随着PAC加量的增加逐渐上升,当投加量为 133,mg/L时,絮凝率可达到 89.96%;继续增加投加量,絮凝率趋于稳定,而在整个过程中体系 pH没有明显变化,所以可以排除絮凝率的变化是由于pH变化造成的.
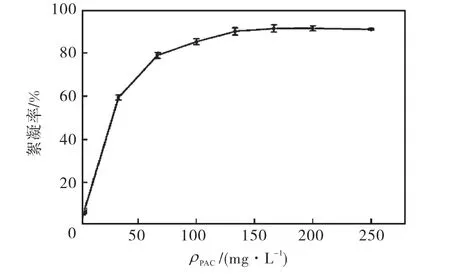
图3 PAC对生活污水的絮凝效果Fig.3 Effect of PAC on domestic wastewater
2.2.3 XM09与PAC复配处理生活污水
根据2种化学絮凝剂的单因素试验结果,进行2因素4水平的正交试验,实验结果见表1.
从表1中可以看出,复配正交试验中,PAC的投加量对生活污水处理效果的影响最大,这2个因素的主次关系为:PAC>XM09.在 PAC的投加量为50,mg/L、XM09的投加量为 15,mg/L时,其絮凝率可达到最大值91.57%.
2.2.4 不同复配处理体系上清液中的残留铝
通过铝的标准曲线的制作,发现铝含量在 0~10,µg/25,mL范围内与 OD640值呈良好的线性关系,回归方程为 y=0.044,64,x-0.018 9,R2=0.973 62.
在5种不同的絮凝条件(处理1:生活污水原样;处理 2∶30,mg/L XM09;处理3∶133,mg/L PAC;处理4∶15,mg/L XM09+50,mg/L PAC;处理 5∶30,mg/L XM09+133,mg/L PAC)下对上清液中的总铝浓度进行了测定,具体结果见图 4.从图4可以看出,处理1含有较高量的铝,其质量浓度为0.234,9,mg/L.处理1与处理2比较发现,单独加入30,mg/L XM09时,处理2中的残留铝大幅度降低;处理3与处理5比较发现,在加入相同量的PAC条件下,处理 5中投加 XM09后,絮凝率变化不大,但残留铝有很大程度的降低.在4种不同絮凝条件下处理的上清液中,处理3的水样中残留有最高的铝含量,而在处理4下残留铝的量是最少的.上述情况的原因可能在于:PAC本身含有铝,会在絮凝过程中引入新的铝离子到水体中,而XM09则不但不会引入新的铝离子,反而由于其絮凝作用能够大幅度减少水中铝离子存在,一方面XM09中含有羟基和羧基等极性基团,能够与铝离子形成共价键或配位键而结合在一起,另一方面絮凝剂分子的羟基很容易与颗粒物形成氢键,其线性分子结构具有吸附架桥的功能,能够将颗粒物通过网捕的方式聚集成大颗粒物,从而残留的铝也随之被沉降下来.在XM09与PAC复配的絮凝过程中,上清液中铝浓度由PAC单独絮凝的0.289,3,mg/L降至复配絮凝后的0.073,39,mg/L,降幅达到74.6%.而在处理4中的残留铝浓度更低至0.003,5,mg/L.从上述结果可以推测,XM09对于生活污水中存在的铝有一定的去除作用.黄兢[1]就指出微生物絮凝剂对水体中的残留铝有很好的去除作用.
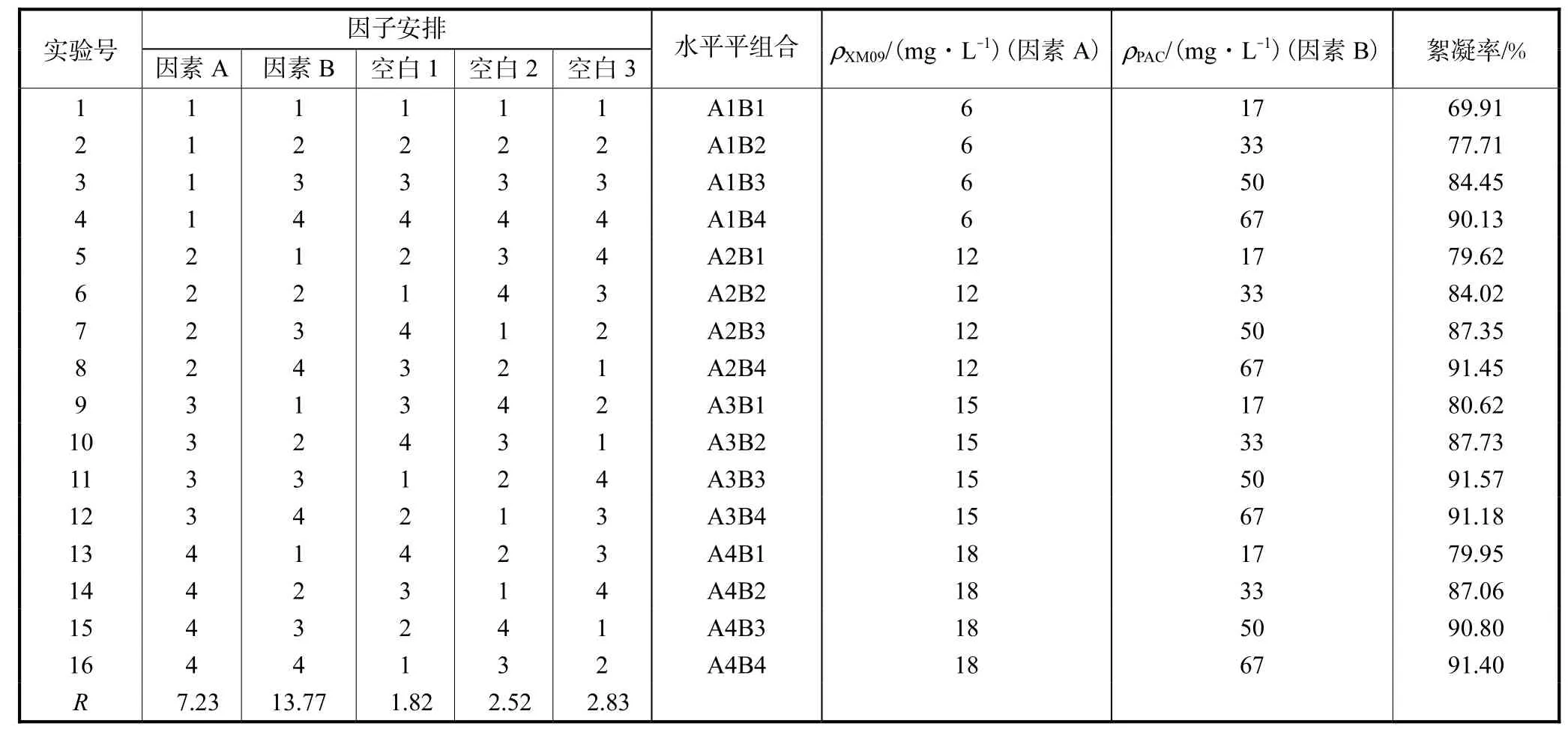
表1 XM09与PAC复配的正交试验结果Tab.1 Orthogonal experimental results of combining XM09 and PAC
为了验证上面所得的推论(XM09具有去除水中残留铝的作用),进一步探讨了在固定 PAC的量为50,mg/L的条件下,投加不同量的XM09对上清液中残留铝的影响,结果见图5.从图5中可以看出,单独使用PAC的水样中残留铝含量最高,而投加了 XM09后,产生了2种现象.当XM09的投加量在 6~23,mg/L范围内时,絮凝率有小幅度的提升,残留铝却是大幅度的降低,铝浓度由单独投加PAC时的0.184,5,mg/L降低至 0.000,8,mg/L;但当 XM09的投加量超过 30,mg/L时,虽然絮凝率的变化不大,铝浓度却有很大程度的回升,特别是投加量为30,mg/L时,其残留铝浓度竟高达0.172,8,mg/L.这个现象说明,当加入 XM09少量时,可能在絮凝作用下,上清液中的铝随水中颗粒物的絮凝沉降而得到去除.而XM09加入过量时,XM09的大量存在可能会影响絮凝剂与生活污水中铝离子或颗粒物的结合方式,同时也会影响PAC在水中的存在形式,从而使得水中的铝浓度也发生了变化.至于在絮凝剂处理生活污水中是否存在一些复杂的作用机理,还需进一步深入探讨.
图4 不同絮凝条件下的残留铝浓度Fig.4 Concentrations of residual aluminum under different flocculating conditions
总之,XM09的絮凝作用在减少废水中的残留铝方面扮演着重要的角色.由于 PAC与生活污水是此次絮凝体系中唯一的铝源,而在单独投加 PAC和XM09与PAC复配的 2种絮凝过程中,PAC的投加浓度与生活污水浓度都保持恒定,不同之处是添加了XM09.由此可知,在少量加入 XM09的情况下,XM09与PAC的联合使用对于水中的残留铝有非常好的去除效果.图4和图5表明,在XM09,12,mg/L、PAC,50,mg/L的复配组合下,残留铝是最少的,为0.8,µg/L,且此条件下的絮凝率也在90%左右,因此选择此条件为最佳的絮凝复配条件.
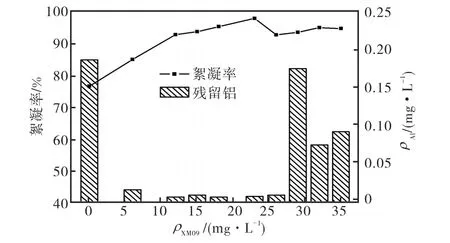
图5 XM09的投加量对残留铝的影响Fig.5 Effect of XM09 dosage on residual aluminum
3 结 论
(1) 由微生物絮凝剂产生菌 M09产生的微生物絮凝剂 XM09,其成分主要为富含羟基和羧基的多糖,分子构型为线性.
(2) 单独利用微生物絮凝剂XM09或PAC对生活污水进行处理,均能取得很好的絮凝效果.但微生物絮凝剂具有无毒无害、无二次污染等特点,使其优于传统絮凝剂,更具有实际应用价值.
(3) 采用正交试验设计进行了微生物絮凝剂XM09与 PAC的复配比例的优化,得出最佳的复配比例为 XM09,15,mg/L、PAC,50,mg/L.结果还发现 2种絮凝剂复配后既可以大大减少传统絮凝剂的投加量,又可以提高絮凝沉降速度和絮凝效果.
(4) 考虑到复配絮凝剂的使用安全性,还对各处理上清液中的残留铝浓度进行了测定,结果发现XM09的加入对于残留铝有一定的去除作用.当 PAC的投加量为50,mg/L时,加入 12,mg/L的 XM09,上清液中的铝浓度可低至0.8,µg/L,比单独使用PAC时降低了99.57%,且此时的絮凝率可达90%左右.
[1] 黄 兢. 微生物絮凝剂 MBFGA1与聚合氯化铝复配技术研究[D]. 长沙:湖南大学环境科学与工程学院,2009.Huang Jing. Studies on the Technology of Composite Flocculant between MBFGA1 and Polyaluminum Chloride[D]. Changsha:School of Environmental Science and Engineering,Hunan University,2009(in Chinese).
[2] Yang Zhaohui,Huang Jing,Zeng Guangming,et al.Optimization of flocculation conditions for Kaolin suspension using the composite flocculant of MBFGA1 and PAC by response surface methodology[J]. Bioresource Technology,2009,100(18):4233-4239.
[3] 湛雪辉. 微生物絮凝剂 MBFXH的制备及其性能研究[D]. 长沙:中南大学资源加工与生物工程学院,2004.Zhan Xuehui. The Research of the Preparation and Characterization of Micromicrobial flocculant MBFXH [D].Changsha:School of Resource Processing and Biological Engineering,Zhongnan University,2004(in Chinese).
[4] 阮 敏,杨朝晖,曾光明,等. 多粘类芽孢杆菌 GA1所产絮凝剂的絮凝性能研究及机理探讨[J]. 环境科学,2007,28(10):2336-2341.Ruan Min,Yang Zhaohui,Zeng Guangming,et al.Flocculating capability and mechanism of microbial flocculant produced by Paenibacillus polymyxa GA1[J]. Environmental Science,2007,28(10):2336-2341(in Chinese).
[5] 中华人民共和国卫生部. GB/T 5750. 6—2006 生活饮用水标准检验方法金属指标[S]. 北京:中国标准出版社,2006.Ministry of Health,People’s Republic of China. GB/T 5750. 6—2006 Standard Examination Methods for Drinking Water:Metal Parameters[S]. Beijing:Standards Press of China,2006(in Chinese).
[6] Li Zhong,Chen Ruowei,Lei Hengyi,et al. Characterization and flocculating properties of a novel microbial flocculant produced by Bacillus circulans[J]. World J Microbiol Biotechnol,2009,25(5):745-752.
[7] Gong Wenxin,Wang Shuguang,Sun Xuefei,et al.Microbial flocculant production by culture of Serratia ficaria and its application in wastewater treatment[J]. Bioresource Technology,2008,99(11):4688-4674.
[8] Lian Bin,Chen Ye,Zhao Jin,et al. Microbial flocculation by Bacillus mucilaginosus:Applications and mechanisms[J]. Bioresource Technology,2008,99(11):4825-4831.
[9] Zhang Zhiqiang,Xia Siqing,Zhao Jianfu,et al. Characterization and flocculation mechanism of high efficiency microbial flocculant TJ-F1 from Proteus mirabilis[J]. Colloids and Surfaces B:Biointerfaces,2010,75(1):247-251.
[10] 邓述波,余 刚,蒋展鹏,等. 微生物絮凝剂 MBFA9的絮凝机理研究[J]. 水处理技术,2001,27 (1):22-25.Deng Shubo,Yu Gang,Jiang Zhanpeng,et al. Study of flocculating mechanism of microbial flocculant MBFA9[J]. Technology of Water Treatment,2001,27(1):22-25(in Chinese).
