鲜肉中挥发性盐基氮含量测定的不确定度评定
2011-06-26郭亚萍张永春
郭亚萍, 张永春, 陈 宇
挥发性盐基氮是一种有毒物质,是指动物性食品由于酶和细菌的作用,在腐败过程中,使蛋白质分解而产生氨以及胺类等碱性含氮物质.一般氨基酸、蛋白质类等含氮高的食品,如鱼、虾、贝类及肉类,在需氧性败坏时,可引起食品化学组成的变化,并产生多种腐败性产物.因此,直接测定这些腐败产物就可作为判断食品质量的依据,常以测定挥发性盐基氮含量的多少作为评定的化学指标.挥发性盐基氮是肉制品新鲜度的主要卫生评价指标[1].本文利用半微量凯氏定氮法对鲜肉中挥发性盐基氮的含量进行了测量不确定度评定,找出该方法中影响测量结果不确定度的主要因素.
1 材料和方法
1.1 仪器和主要试剂[2]
半微量定氮器,微量滴定管(最小分度0.01 mL).
氧化镁混悬液(10 g/L):称取1.0 g氧化镁,加100 mL水,振摇成混悬;硼酸吸收液(20 g/L);盐酸[c(HCl)=0.10 mol/L]的标准溶液.
盐酸标准使用溶液[c(HCL)=0.010 mol/L]:临用前,吸取盐酸标准溶液10 mL置于100 mL容量瓶中,加水稀释至刻度,此溶液浓度为0.010 mol/L.
混合指示剂:使用前各取1 mL 甲基红 乙醇溶液(2 g/L)和次甲基蓝溶液(l g/L)混匀.
1.2 试验方法[2]
1.2.1试样处理
将试样除去脂肪、骨及腱后,绞碎搅匀,称取约10.0 g,置于锥形瓶中,加100 mL水,不时振摇,浸渍30 min后过滤,滤液置冰箱内备用(时间不得超过30 min).
1.2.2蒸馏滴定
将盛有10 mL吸收液及5~6滴混合指示液的锥形瓶置于冷凝管下端,并使其下端插入吸收液的液面下,准确吸取5.0 mL上述试样滤液于蒸馏器反应室内,加5 mL氧化镁混悬液(10 g/L),迅速盖塞,并加水以防漏气,通入蒸汽,进行蒸馏,蒸馏5 min即停止,吸收液用盐酸标准滴定溶液(0.010 mol/L)或硫酸标准滴定溶液滴定,终点至蓝紫色.同时做试剂空白试验.
1.2.3结果计算
试样中挥发性盐基氮的含量按公式(1)进行计算

式中 X——试样中挥发性盐基氮的质量分数,mg/100 g.
V1——测定用样液消耗盐酸标准溶液的体积,mL.
V2——试剂空白消耗盐酸标准溶液的体积,mL.
cs——盐酸标准使用溶液的浓度,mol/L.
14——与 1.00 mL盐酸标准滴定溶液[c(HCl)=1.000 mol/L]或硫酸标准滴定溶液[c(1/2H2SO4)=1.000 mol/L]相当的氮的质量,mg.
m——试样质量,g.
2 不确定度来源分析
根据测量过程和计算公式(1)分析不确定度来源,如图1[3-6].

图1 不确定度来源分析图Fig.1 Sources analysis of uncertainty
3 建立数学模型
X值的数学模型[7]为

式中 fmJfmTfmSfmrep——天平校准、温度和湿度分别对m引入的不确定度分量
fV1JfV1TfV1ZfV1rep——测样时滴定管校准、温度、重复性和终点对V1引入的不确定度分量
fV2JfV2TfV2ZfV2rep——试剂空白时校准、温度和重复性和终点对V2引入的不确定度分量
fc0和fcx——标准溶液和稀释体积过程对c引入的不确定度分量
fyJfyTfyrepfrJfrTfrrep——盐酸标准溶液稀释过程中移液管和容量瓶校准、温度和重复性对c引入的不确定度分量.
4 不确定度分量的量化
4.1 m引入的标准不确定度u(m)[8]
4.1.1m校准(fmJ)引入的标准不确定度u(m)
天平计量证书标明其称量的最大允差为0.6 mg,假定为矩形分布,换算成标准不确定度为:

所以称取10.0 g样品引入的相对标准不确定度为:
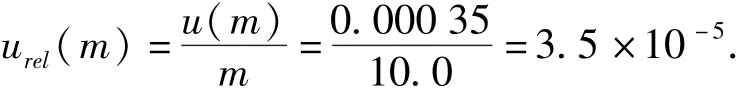
4.1.2 称量中fmTfmS的影响
因为实验室环境相对独立,称量操作迅速及时,所以环境温度、湿度在短时间内变化甚微,所以对称量结果影响可以忽略不计.
4.1.3称量重复性fmrep引入的不确定度并入到结果重复性rep中考虑
称量样品时,由重复称量引入的不确定度已包含在测量结果重复性当中,不须再重复评定.
4.2 滴定样品溶液实际消耗盐酸溶液体积引入的标准不确定度u(V1-V2)[8]
4.2.1V1引入的不确定度u(V1)
4.2.1.1校准即(fV1J)对体积的影响u1(V1)
检定证书标明A级2 mL座式滴定管其容量允差为0.01 mL,假定为矩形分布,换算成标准不确定度为:
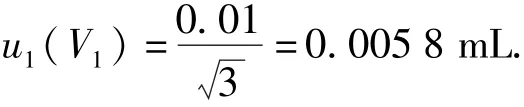
4.2.1.2温度即(fV1T)对体积影响u2(V1)
实验温度控制在(20±3)℃,水的体积膨胀系数为2.1×10-4℃-1,因此产生的体积变化为±(V1×3×2.1×10-4)= ±6.3×10-4V1(mL),假定温度变化为矩形分布,则
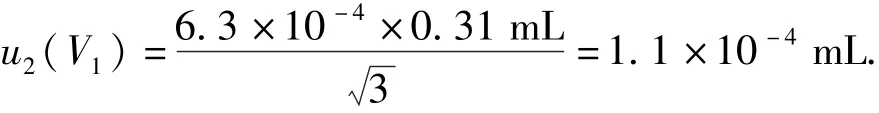
4.2.1.3V1的重复性frep和终点判定fV1Z的影响并入到测量结果X的重复性rep中考虑
将上述V1不确定度分量合成
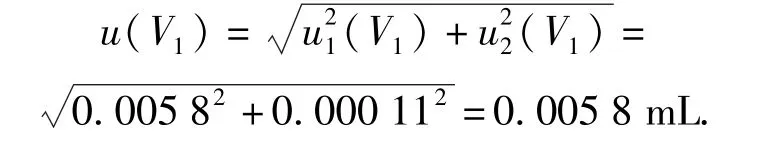
4.2.2V2引入的不确定度u(V2)
4.2.2.1校准即(fV2J)对体积的影响u1(V2)分析同V1,即:

4.2.2.2温度即(fV2T)对体积影响u2(V2)
分析同V1,V2消耗0.04 mL:
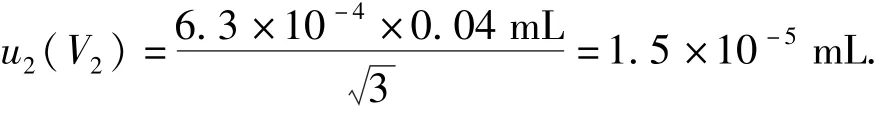
4.2.2.3V2的重复性影响frep和终点fV2Z的影响并入到测量结果X的重复性rep中考虑
将上述V2不确定度分量合成:

将V1和V2的不确定度分量再进行合成得:

4.3 盐酸标准使用溶液cs的标准不确定度u(cs)[8]
4.3.1盐酸标准溶液c0即(fc0)引入的不确定度u(fc0)
由GBW(E)080463盐酸标准物质证书中可知,标准值为0.103 6 mol/L,该标准值的扩展不确定度为0.000 1 mol/L,扩展因子k=2,故盐酸标准物质的相对标准不确定度:

4.3.2稀释过程中(fcx)引入的不确定度u(fcx)
4.3.2.1移液管校准即(fyJ)引入的不确定度u(fYJ)
检定证书标明B级10 mL单标线移液管其容量允差0.04 mL,假定其为矩形分布,其校准的不确定度为:
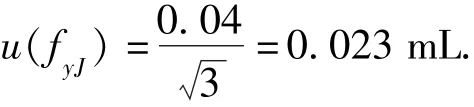
4.3.2.2温度即(fyT)对体积影响u(fyT)
分析同V1,即:

4.3.2.3移液管充满至刻度的重复性变化对体积的影响u(fyrep)
多次吸取溶液,做排液称量实验,标准差为0.01 mL,则u(fyrep)=0.01 mL.
将上述移液管不确定度分量合成:

4.3.2.4容量瓶校准即(frJ)引入的不确定度u(frJ)
检定证书标明A级100 mL单标线容量瓶其最大滴定允许误差0.10 mL,假定其为三角分布,分析同V1,即:校准的不确定度为:
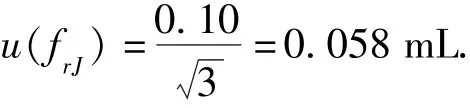
4.3.2.5温度即(frT)对体积影响u(frT)
分析同V1,即:

4.3.2.6容量瓶充满至刻度的重复性变化对体积影响u(frrep)
100 mL容量瓶充满至刻度10次,做称量实验,标准差为0.02 mL,则
u(frrep)=0.02 mL,
将上述容量瓶不确定度分量合成:

合成上述分量,即得盐酸标准使用液浓度cs的相对标准不确定度urel(cs):
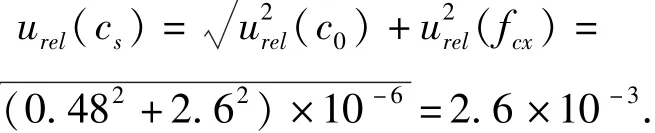
4.4 测量结果X重复性rep引入的不确定度u(rep)[8]
将待测的样液连续滴定进行平行测量,算得的X的值如表1.

表1 鲜肉中挥发性盐基氮重复性测定结果Tab.1 Determination result of repeatability for TVB-N in fresh meat mg/100 g
测量重复性引入的标准不确定度由2次测量结果的平均值的标准差表示.
相对标准不确定度为:
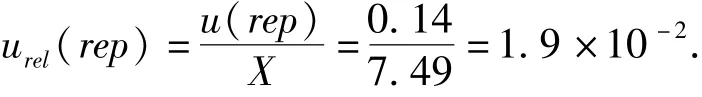
4.5 整理测定挥发性盐基氮含量的数学模型[8]
由上分析,公式(2)整理结果为:

5 合成标准不确定度的计算
测定过程中的数值与不确定分量见表2.

表2 测定过程中的数值与不确定度分量Tab.2 Values of measurement process and uncertainty components
将不确定度分量进行合成[9].
由上分析,公式(3)知:

样品中挥发性盐基氮质量分数的测定结果为7.49 mg/100 g,则:
uc(X)=Xurel(X)=7.49×0.036=0.27 mg/100 g.
6 包含因子及扩展不确定度的计算
95%置信水平下取包含因子k=2,将合成标准不确定度乘以包含因子计算得到测量结果的扩展不确定度为:

7 测量结果及其不确定度表述
鲜肉中挥发性盐基氮质量分数为:
(7.49±0.54)mg/100 g,k=2.
8 结 论
通过利用半微量凯氏定氮法,对鲜肉中挥发性盐基氮的含量进行了测量不确定度的评定,找出了影响测量结果准确性的主要因素.检测样品鲜肉中挥发性盐基氮含量为7.49 mg/100 g,U=0.54 mg/100 g,k=2,样品溶液实际消耗盐酸溶液的体积和结果重复性是影响该方法测量不确定度的主要因素.建议从不确定度来源分析实施测量改进,在人员方面,进一步提高检测人员操作技能,尽量减少由于检测人员操作重复性引入的不确定度;在仪器设备方面,建议使用1 mL座式滴定管进行测量,可以进一步降低由滴定管容量允差引入的不确定度;在环境方面,减小测量环境的温度波动幅度,可以减少由环境温度变化对样品溶液实际消耗盐酸溶液的体积引入的不确定度;此外,在样品处理前将其充分混匀可以减少由于取样不均匀对结果重复性产生的影响.从上述几方面努力实施改进,可以使测量结果的不确定度水平降低,从而提升实验室的检测能力.
