一步相转移-沉淀法制备轻质碳酸钙的沉淀工艺条件研究
2011-06-05杨保俊王百年袁新松董晓祥
杨保俊, 陈 曦, 王百年, 袁新松, 董晓祥
(1.合肥工业大学 化学工程学院,安徽 合肥 230009;2.合肥师范学院 化学化工系,安徽 合肥 230601)
0 引言
磷石膏的主要成分[1]是CaSO4·2H2O,是化学工业中排放量最大的固体废弃物之一[2]。目前全国磷石膏累计堆存量超过1.2×108t[3-4],不仅占用大量的土地资源,造成环境污染,而且浪费了宝贵的硫、钙等资源,因此,磷石膏废渣的综合利用已迫在眉睫。关于磷石膏的综合利用,目前报道的由磷石膏制备轻质碳酸钙和/或硫酸铵的方法主要为复分解法[5-9],包括复分解反应制硫酸铵、粗品碳酸钙的再资源化2个主要步骤。但该方法通过强酸浸取,较好地解决了不溶性杂质的去除问题,但同时也带来所生成的CO2的净化和再利用的问题;流程中包括强酸浸取和2次碳化反应,工艺流程长、成本高,且存在二次污染。
本文针对上述复分解法工艺中存在的主要不足,采用如图1所示的一步相转移沉淀法制备轻质碳酸钙和硫酸铵,并研究了该反应的工艺条件,确定了较适宜的工艺条件。采用相转移沉淀法提取磷石膏中的钙离子,不仅可以提高钙离子的利用率,而且为磷石膏的综合利用和深度开发开辟了新的途径。

图1 一步相转移-沉淀法制备轻质碳酸钙和硫酸铵工艺流程
1 实验部分
1.1 主要原料和试剂
原料为磷肥生产过程中的磷石膏,经分析其主要化学组成见表1所列。

表1 磷石膏主要化学组成
本实验中所用试剂均从上海化学试剂公司购得,使用前未经任何纯化处理。
1.2 主要仪器
D/MAX-γA型 X-射线衍射仪,日本理光生产;H-800型透射电子显微镜,Hitachi公司;PHS-29A型数显酸度计,上海虹益仪器仪表有限公司。
1.3 实验步骤
(1)相转移反应。称取一定量的相转移剂溶于100mL蒸馏水并转移到三口烧瓶中,加入适量经水洗预处理后的磷石膏,反应一定时间后,过滤得到钙离子溶液。
(2)沉淀反应。向Ca2+溶液中加入适量固体碳酸氢铵和氨水,调节pH值至确定值,水浴恒温条件下搅拌反应确定时间、陈化3h后,过滤、洗涤至滤液用BaCl2检验无白色沉淀为止。滤饼置于60℃烘箱中干燥3h,得到粉末样品,待测。
1.4 分析和检测方法
溶液成分和样品纯度分析,按国家标准进行。溶液中Ca2+质量分数采用高锰酸钾法分析,产品中CaCO3纯度采用EDTA法分析。
根据沉淀反应前后滤液中的钙离子的质量(m1,m2),计算出轻质碳酸钙的产率η为:
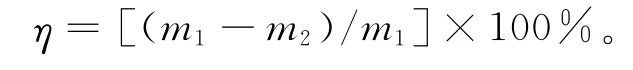
2 结果与讨论
2.1 单因素条件实验
2.1.1 沉淀反应温度对碳酸钙产率的影响
反应时间60min、钙离子与碳酸氢根离子的摩尔比为1∶1、沉淀反应体系pH=7的条件下,沉淀反应温度对碳酸钙产率的影响如图2所示。
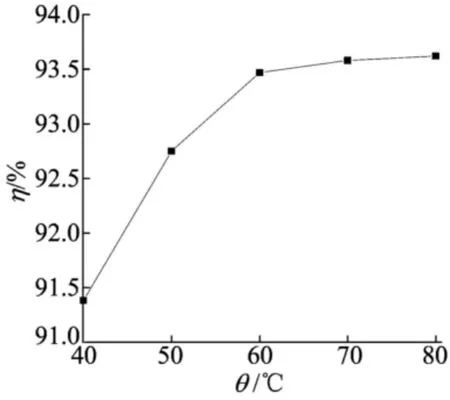
图2 沉淀反应温度对碳酸钙产率的影响
由图2可看出,当沉淀反应温度小于60℃时,随着沉淀反应温度的增加,碳酸钙的产率增加;当温度大于60℃时,碳酸钙的产率随温度的变化相对不大。从节能等角度综合考虑,实验中选择较适宜的沉淀反应温度为60℃。
2.1.2 反应时间对碳酸钙产率的影响
沉淀反应温度60℃、钙离子与碳酸氢根离子的摩尔比1∶1、沉淀反应体系pH值为7的条件下,反应时间对碳酸钙产率的影响如图3所示。
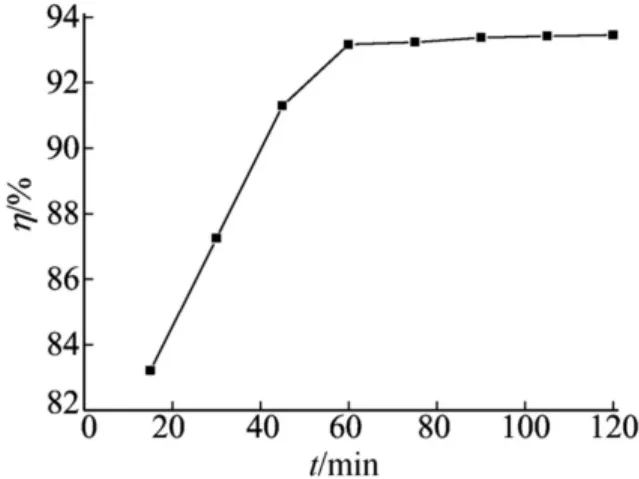
图3 反应时间对碳酸钙产率的影响
由图3可知,当反应时间小于60min,碳酸钙的产率随时间变化较大;当反应时间大于60min,随着反应时间的延长,碳酸钙产率的增加趋于缓慢,实验中选择较适宜反应时间为60min。
2.1.3 摩尔比对碳酸钙产率的影响
沉淀反应温度60℃、反应时间60min、沉淀反应体系pH值为7的条件下,钙离子与碳酸氢根离子摩尔比对碳酸钙产率的影响如图4所示。从图4可知,当钙离子与碳酸氢根物质摩尔比小于1∶1.00时,碳酸钙的产率随其比值的增加快速增加;当摩尔比介于1∶1.00到1∶1.10之间时,碳酸钙产率的增加趋于缓慢;当比值大于1∶1.10时变化不明显。因此,实验中选择较适宜的钙离子与碳酸氢根离子的摩尔比为1∶1.10。
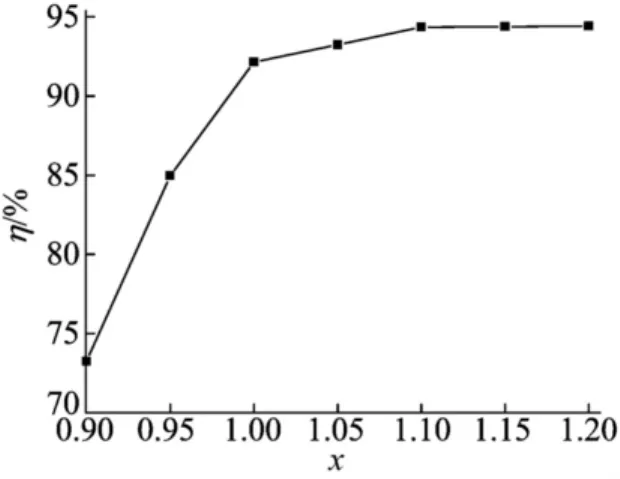
图4 钙离子与碳酸氢根摩尔比对碳酸钙产率的影响
2.1.4 沉淀反应体系pH值对碳酸钙产率影响
沉淀反应温度60℃、反应时间60min、钙离子与碳酸氢根离子的摩尔比为1∶1.10的条件下,沉淀反应体系pH值对碳酸钙产率的影响如图5所示。由图5可以看出,随着体系pH值的增加,碳酸钙产率增大;当pH值大于10时,碳酸钙的产率变化不大,且随着pH值的进一步增加,所需氨水量也迅速增大,导致体系的体积分数下降、设备的单程产率下降。综合考虑,实验中选择较适宜的pH值为10。
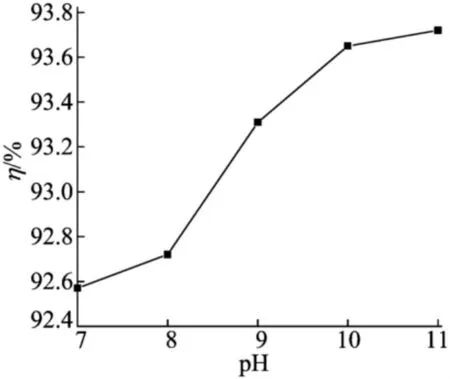
图5 沉淀反应体系pH值对碳酸钙产率的影响
由以上单因素条件实验所确定的较适宜的沉淀反应工艺条件为:沉淀反应温度60℃、反应时间60min、钙离子与碳酸氢根离子的摩尔比1∶1.10、沉淀反应体系pH=10。
2.2 正交实验
由上述单因素条件实验可看出,沉淀反应温度、反应时间、钙离子与碳酸氢根离子的摩尔比等因素的变化对碳酸钙产率均有明显的影响,沉淀反应体系pH值的影响相对较小。因此,在沉淀反应体系pH值为10的前提下,以碳酸钙的产率为考察指标,采用三因素三水平正交实验法,因素水平见表2所列,进一步优化沉淀反应条件,实验结果见表3所列。

表2 正交实验的因素和水平

表3 正交实验与极差分析结果
由表3中的极差R可以看出,各因素对轻质碳酸钙样品产率影响的显著性依次为:钙离子与碳酸氢根离子的摩尔比>反应时间>沉淀反应温度。
因素A以A3的影响最大,因素B以B3的影响最大,因素C以C3的影响最大。因此,得到的较优水平组合为A3B3C3,所确定较佳沉淀反应工艺条件为:沉淀反应温度70℃,反应时间75min,n(Ca2+)∶n(HCO3-)=1∶1.15。
2.3 较适宜工艺条件下的重复实验
在所确定的较佳工艺条件下的3次重复实验结果见表4所列,由表4可看出,碳酸钙的平均产率达到95.25%,平均纯度达到98.17%。
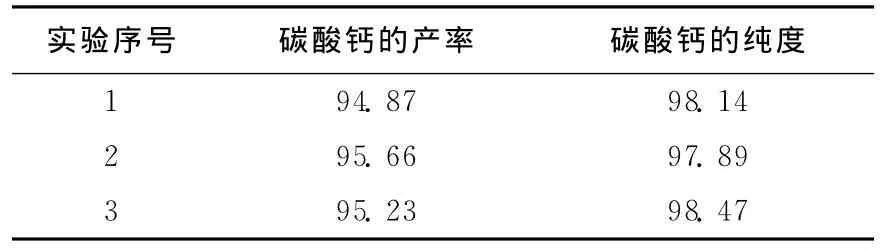
表4 较佳工艺条件下的重复实验结果 %
所制备碳酸钙样品的XRD图如图6所示。
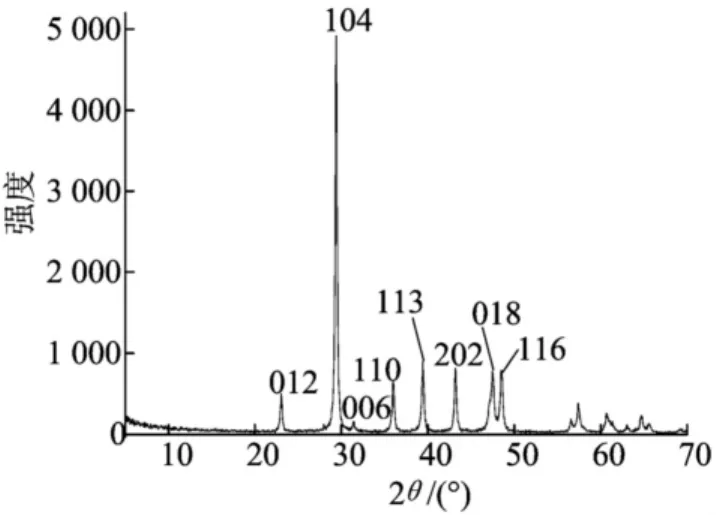
图6 所制备的轻质碳酸钙样品的XRD图
图6中所有衍射峰均可指标化为方解石型碳酸钙,计算所得的晶胞参数为a=0.498 8nm,c=1.707nm,与文献值a=0.498 9nm,c=1.706nm (JCPDF05-0586)吻合得很好。图6中没有观察到明显的杂质衍射峰,表明所制备的样品为纯相的方解石型碳酸钙。由谢乐公式计算平均粒径为29.44nm。
轻质碳酸钙样品的TEM图如图7所示。

图7 所制备的轻质碳酸钙样品的TEM图
由图7可以看出,所制备样品表现为大小粗细较为均匀,长度为0.8~1.2μm的“无柄哑铃”状,每个“无柄哑铃”是由很多粒径为20~40nm碳酸钙颗粒团聚形成。
3 结论
通过单因素条件实验和正交实验,考察并优化了一步相转移-沉淀法由磷石膏制备轻质碳酸钙的沉淀反应工艺条件,所确定的较佳工艺条件:沉淀反应温度70℃、钙离子和碳酸氢根离子的摩尔比1∶1.15、反应时间75min、沉淀反应体系pH=10。该条件下的重复试验结果表明:所制备的样品为纯相方解石型碳酸钙,平均产率为95.25%,平均纯度为98.17%,样品呈现由很多粒径为20~40nm碳酸钙颗粒团聚而成的“无柄哑铃”。
[1]Smadi M M,Haddad R H,Akour A M.Potential use of phosphogypsum in concrete[J].Cement and Concrete Research,1999(29):1419-1425.
[2]曾 光,胡 宏.磷石膏综合利用副产物碳酸钙渣的深加工研究[J].贵州化工,2009,34(2):1-3.
[3]秦俊芳.磷石膏综合利用现状探讨[J].中国资源综合利用,2010,28(3):23-24.
[4]陈和全.湿法磷酸生产中副产物磷石膏的综合利用[J].磷肥与复肥,2009,24(4):68-69.
[5]张兴法.磷石膏综合利用副产物碳酸钙渣的再资源化[J].化工矿物与加工,2004,33(12):21-23.
[6]解 田,刘 佳,李白玉,等.磷石膏复分解制硫酸铵的工艺研究[J].硫磷设计与粉体工程,2009(4):4-8.
[7]周亮亮,夏举佩,张召述,等.利用磷石膏制备高活性碳酸钙[J].昆明理工大学学报:理工版,2007,32(15):96-99.
[8]刘 健,解 田,朱云勤,等.磷石膏钙渣制备高品质轻质碳酸钙工艺研究[J].无机盐工业,2010,42(6):47-48.
[9]张 群,方 亮,陈传宝.PSSS基质及温度对碳酸钙结晶的影响[J].合肥工业大学学报:自然科学版,2008,31(10):1638-1640.
