小儿蜗神经发育不良△
2011-06-05莫玲燕燕飞刘辉陈静陈雪清黄丽辉韩德民
莫玲燕 燕飞 刘辉 陈静 陈雪清 黄丽辉 韩德民
·临床研究·
小儿蜗神经发育不良△
莫玲燕1燕飞2刘辉1陈静1陈雪清1黄丽辉1韩德民1
目的 报道一组蜗神经发育不良(cochlear nerve deficiency,CND)小儿的临床特征,以提高对本病的认识。方法 回顾性分析2007年1月到2008年4月就诊的、内耳MRI及听力学资料完整的20例(37耳)CND小儿(其中男13例,女7例,年龄10个月到4岁)的影像学、听力学表现及人工耳蜗植入效果。结果 85%(17/20)的患儿为双侧发病,15%(3/20)为单侧发病;16.22%(6/37)合并前庭神经发育异常,8.11%(3/37)合并面神经发育异常。根据是否伴有内耳畸形分为三组:32.43%(12/37)伴耳蜗畸形或同时伴有前庭畸形(第一组);13.51%(5/37)仅伴前庭畸形(第二组);54.05%(20/37)独立发病,不伴内耳畸形(第三组)。听力学测试结果:86.49%(32/37)ABR最大输出(100 d B n HL)无反应,13.51%(5/37)在非常高的刺激强度仅有分化不良的波Ⅴ;9耳有行为听阈结果者均为极重度感音神经性聋;第一组12耳DPOAE和CM均未引出,第二组60%(3/5)DPOAE和CM均未引出,40%(2/5)DPOAE和/或CM引出;第三组45%(9/20耳)DPOAE和CM均未引出,55%(11/20耳)DPOAE和/或CM引出。人工耳蜗植入效果:2例术前、术后资料完整者中1例术后开机一年婴幼儿有意义听觉整合量表(infant and toddler meaningful auditory integration scale,IT-MAIS)评估得分与蜗性聋儿相当,另1例无效。结论
蜗神经发育不全; 听神经病; 内耳畸形
蜗神经发育不良(cochlear nerve deficiency,CND)指第八对颅神经的耳蜗支在内耳MRI上缺失或狭窄[1]。CND可以是蜗神经先天部分或完全未发育造成,也可以是后天由于种种原因导致的退行性变。研究表明[2,3]CND常伴有内耳畸形和内听道(internal auditory canal,IAC)狭窄,但也有内耳和IAC形态正常者。关于CND的临床资料,特别是听力学资料报道较少,而CND又与人工耳蜗植入效果密切相关,因此本文报道一组CND小儿的临床特征,以提高对本病的认识。
1 资料与方法
1.1 研究对象 2007年1月~2008年4月因未通过新生儿听力筛查或家长发现听力异常来首都医科大学附属北京同仁医院门诊就诊且内耳MRI及听力学检查结果完整的20例(37耳)小儿。男13例,女7例,年龄10个月到4岁(中位年龄19个月)。5例患侧植入人工耳蜗。
1.2 仪器及测试方法 短声ABR、CM、DPOAE、行为听力测试均于本底噪声≤30 dB(A)的隔声室内进行,声导纳于相对安静的房间内进行。受试儿水合氯醛镇静睡眠后进行。
1.2.1 短声ABR测试 测试仪器为美国INTELLIGENT HEARING的SMART EP组件,其刺激声信号为100μs交替极性短声,最大输出为100 dB n HL。刺激速率为19.3次/秒,耳机为ER-3 A插入式耳机;记录电极置于前额正中发际,参考电极置于同侧乳突,地极于鼻根部。极间电阻为1~3 kΩ,带通滤波为100~3 000 Hz,分析窗宽为12 ms,叠加次数为2 048次,伪迹剔除设置为31μV。阈值为引出可重复的、肉眼可识别的波Ⅴ的最小刺激强度。无反应为两次100 dB n HL均未引出可重复波形。对于80 d B n HL无反应或波形缺失耳,则以100 dB n HL疏波和密波进行CM测试并验证[4]。
1.2.2 DPOAE测试 测试仪器为美国INTELLIGENT HEARING的SMART DPOAE组件。两个初始纯音信号的强度为L1=L2=70 d B SPL,频率比f2/f1=1.22,测试信号频率范围为0.7~6 k Hz,每个测试频率点叠加24次。DPOAE的判定标准:在所有测试频率中,2、3、4 k Hz三个频率点的信噪比均≥3 dB且超出其1倍标准差,即为记录到DPOAE,反之则为未记录到。
1.2.3 行为听力测试 所用设备为GSI-61听力计、视觉奖励器以及一些玩具。根据受试儿年龄选择不同的儿童行为听力测试方法。一般6~24月龄行视觉强化定向条件反应测试(visual reinforcement audiometry,VRA),25月龄~6岁儿童行游戏测听(play audiometry,PA)。但在测试过程中根据小儿智力、身体发育水平以及听力情况选择适宜的测试方式。各频率的行为听阈为能够得到两次以上可靠反应的最小强度。听力损失按WHO(1997)标准进行分级,轻度聋为0.5、1、2和4 k Hz平均行为听阈26~40 dB HL,中度聋为41~60 dB HL,重度聋为61~80 dB HL,极重度聋为81 dB HL以上。
1.2.4 内耳MRI检查 设备为美国GE公司1.5T核磁共振扫描仪。首先在横断面、冠状面、矢状面定位,行横断面自旋回波(SE)T1权重像(T1WI)和横断面、冠状面快速自旋回波(FSE)T2权重像(T2WI)扫描。再行双侧IAC斜矢状面3D FIESTA序列,观察面神经、蜗神经及前庭上、下神经。CND定义为蜗神经细小或缺失,缺失为蜗神经在横断面、冠状面或斜矢状面上都不显示,细小为蜗神经形态显著小于同侧的面神经或前庭上、下神经,或者显著小于对侧的蜗神经[1]。IAC狭窄定义为其最大直径小于3 mm[5]。内耳畸形的影像学表现参照以前的文献报道[6]。
1.2.5 婴幼儿有意义听觉整合量表(infant and toddler meaningful auditory integration scale,ITMAIS)(附录)评估 由经过培训的听力学专业人员使用IT-MAIS对患儿术后听觉能力的发育进行评估,评估前由评估人员对患儿家长进行必要的指导。评估人员逐一询问量表中的10个问题,由家长对患儿在日常生活中听力方面的自发性反应作出详细的描述,并鼓励家长提供尽量多的例子,评估人员详细记录家长对每一问题的回答。评估采用面对面询问方式,分别在术前及开机后1、3、6、12个月时对患儿的听觉能力情况进行评估。
2 结果
2.1 病史 20例中2例出生时有窒息史,1例合并唇裂,1例合并蛛网膜下腔囊肿,1例脑发育不全,余无特殊。
2.2 影像学结果 20例患者中,3例(15%,3/20)为单侧病变,17例(85%,17/20)为双侧病变。单侧病例中2例对侧耳经影像学及听力学检查证实为正常(图1),另1例对侧内耳MRI示外、中、内耳结构正常,但听力学检查为极重度感音神经性聋。
37耳中,单纯CND者20耳(54.05%),合并耳蜗畸形者6耳(16.22%),仅前庭畸形者5耳(13.51%),耳蜗及前庭均畸形者6耳(16.22%)。
37耳中,蜗神经细小32耳(86.48%),蜗神经缺失5耳(13.51%);IAC狭窄17耳(45.95%),前庭神经发育异常7耳(18.92%)。
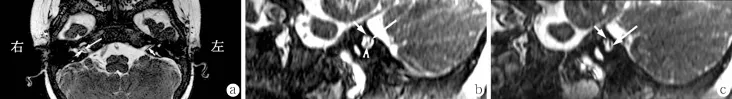
图1 单侧CND患者的内耳MRI
2.3 听力学测试结果 32耳(86.49%,32/37)ABR最大输出(100 dB nHL)无反应,5耳(13.51%,5/37)在非常高的刺激强度仅有分化不良的波Ⅴ,分别为100 dB n HL 2耳,90 dB n HL 1耳,80 dB n HL 2耳。9耳有行为听阈结果者均为极重度感音神经性聋。
为便于描述DPOAE/CM结果,将37耳按是否合并内耳畸形以及内耳畸形的类型分为三组,第一组为伴耳蜗畸形或同时伴前庭畸形者,共12耳(32.43%),DPOAE和CM均未引出,第二组为仅伴有前庭畸形者5耳(13.51%),60%(3/5)耳DPOAE和CM均未引出,40%(2/5)耳DPOAE和/或CM引出;第三组为单纯蜗神经病变不伴内耳畸形者20(54.05%)耳,45%(9/20)耳DPOAE和CM均未引出,55%(11/20)耳DPOAE和/或CM引出。
人工耳蜗植入后IT-MAIS评估:5例患耳植入人工耳蜗,只有2例(均为蜗神经细小者)有开机一年以上完整的评估结果,其中1例开机时得分为0,术后一年为1分;另1例开机时为0,随着开机时间的增长,得分持续增加,其开机1月、3月、2年时得分分别为15、18和35分,与蜗性聋儿相当。
3 讨论
3.1 内耳、蜗神经发育与内听道发育的关系 本研究37耳CND中,只有17耳IAC狭窄,文献也有蜗神经形态正常而IAC狭窄的报道[7],说明IAC狭窄与否不是判断蜗神经形态是否完好的可靠指征。内耳MRI的斜矢状位(即IAC横断面)能够清晰地显示IAC内前庭上、下神经、面神经和蜗神经的形态及相对大小,因此只有内耳MRI才能可靠地反映蜗神经的发育情况[8]。IAC与蜗神经形态之间的不相关性可能与蜗神经和IAC发育的时间顺序有关。孕7周时Corti器及前庭蜗神经开始发育,孕9周时听泡的间叶细胞开始软骨化以及骨化,大约于孕24周时,前庭蜗神经通过骨化抑制作用形成IAC[9]。这一时期内如果前庭蜗神经发育不全,骨化抑制作用就会减弱或消失,从而导致IAC狭窄。IAC形成后,前庭蜗神经正常形态的维持需要耳蜗毛细胞分泌的神经营养因子[10],当各种原因导致该神经营养因子缺乏时,蜗神经就会变性、萎缩,直径编小而IAC此时已发育完成,其形态将保持正常不发生改变。因此根据IAC的大小可大致判断蜗神经形态异常发生的时间:如果IAC狭窄,则说明蜗神经的病变发生于发育的较早时期,至少在孕24周以前;如IAC大小正常,则说明蜗神经异常发生于IAC骨化以后,大约为孕24周以后。
本研究中有3例为单侧发病,其中2例对侧耳影像学及听力学检查均正常,另1例对侧耳影像学检查正常,但听力学检查为极重度感音神经性聋,表明CND可以单耳发病,其原因目前尚难以解释。因此临床上对单侧极重度感音神经性聋没有腮腺炎等特殊病史,而中耳、内耳结构正常者,应行内耳MRI检查以排除CND的可能。
3.2 CND患者的听力学表现 本组病例9耳有行为测听结果者均为极重度感音神经性聋,而短声ABR反应阈从80~100 dB n HL甚至无反应,各病例结果之间的差异可能与蜗神经纤维残余数量和残存功能的程度不同有关。
人类颞骨组织病理研究结果表明CND可以单独出现,也可以与内耳畸形合并出现[11]。因此CND的听力学表现也因是否合并内耳畸形而各不相同。本研究结果显示,当CND单独存在时(即第三组),DPOAE和/或CM的引出率为55%;当合并有前庭畸形时(即第二组),40%耳DPOAE和/或CM引出,加之其严重异常的短声ABR结果,这种听力学表现与听神经病一致,但蜗神经形态完好与否显著影响人工耳蜗植入的效果[11,12]。因此,人工耳蜗植入前,为保证植入的效果,进行内耳MRI检查以排除CND是必要的。当CND合并有耳蜗畸形时(即第一组),所有病例DPOAE和CM均未引出,加之短声ABR严重异常,这与蜗性聋患者的听力学表现一致。提示当听力学检测结果为蜗性聋者,应排除同时存在蜗神经病变的可能,在选择人工耳蜗植入适应证时尤为重要。
3.3 CND与人工耳蜗植入 CND是蜗神经发育细小及蜗神经缺失的总称[1]。人工耳蜗植入的成败取决于是否存在足够数量的神经纤维。蜗神经发育不全势必在很大程度上影响人工耳蜗植入效果。一般认为蜗神经缺失是人工耳蜗植入的绝对禁忌证[8]。多数文献报告不管蜗神经狭窄还是缺失,植入人工耳蜗效果都不佳。Teagle等[12]报告5例植入人工耳蜗的CND患者开放项言语识别得分均<30%,其中2例已停止使用装置,2例虽坚持使用装置,但只用于声音的识别,还有1例又行对侧非CND耳的植入后取得了显著的效果。Walton等[11]比较了CND与典型耳蜗性聋患者的人工耳蜗植入效果,术后一年前者的言语测试及电诱发听性脑干反应(electrically evoked auditory brainstem response,EABR)结果显著差于后者[13]。也有个案报道CND效果较为满意者[14]。本组病例中5例植入人工耳蜗,仅2例术前及术后一年以上资料完整,其中1例术后一年ITMAIS得分仅为1分,另1例随着开机时间的延长,其IT-MAIS得分持续增加,开机1年时与耳蜗性聋人工耳蜗植入者得分相当[15]。这2例同为蜗神经狭窄,而人工耳蜗植入的效果却炯然不同,其原因可能是他们蜗神经残余数量和功能不同,或者二者在听觉通路更高水平还存在着其它的功能差异。因此为保证人工耳蜗植入效果,迫切需要一些在术前就能预测术后效果的评估手段。据报道EABR[11]、电诱发的蜗内复合动作电位(electrical-evoked intracochlear compound action potential,ECAP)[12]与术后言语测试结果存在较好的相关性。此外内耳及颅脑MRI的异常表现,如脑室周围白质软化、Dandy-Walker畸形(先天性小脑和第四脑室畸形)、II型Arnold Chiari畸形(先天性脑畸形)等也与人工耳蜗术后效果直接相关[12]。
对于双侧CND患者,有研究提倡除口语以外的交流方式[8],另外,随着人工听觉技术的发展,听觉脑干植入、人工中脑植入或将成为CND患者可行的干预方法。
1 Glastonbury CM,Davidson HC,Harnsberger HR.et al.Imaging findings of cochlear nerve deficiency[J].AJNR Am J Neuroradiol,2002,23:635.
2 Nelson E,Hinojosa R.Aplasia of the cochlear nerve:a temporal bone study[J].Otol Neurotol,2001,22:790.
3 Spoendlin H,Schrott A.Quantitative evaluation of the human cochlear nerve[J].Acta Oto-laryngologica,1990(Suppl),470:61.
4 莫玲燕,刘辉,陈静,等.相反极性短声所记录CM在小儿听神经病诊断中的应用[J].听力学及言语疾病杂志,2007,15:356.
5 Olivares FP,Schuknecht HF.Width of the internal auditory canal.A histological study[J].Ann Otol Rhinol Laryngol,1979,88(3 Pt 1):316.
6 Buchman CA,Copeland BJ,Yu KK et al.Cochlear implantation in children with congenital inner ear malformations[J].Laryngoscope,2004,114:309.
7 Adunka OF,Roush PA,Teagle HFB,et al.Internal auditory canal morphology in children with cochlear nerve deficiency[J].Otology&Neurotology,2006,27:793.
8 Buchman CA,Roush PA,Teagle HF,et al.Auditory neuropathy characteristics in children with cochlear nerve deficiency[J].Ear Hear,2006,27:399.
9 Larsen W.Human Embryology[M].2nd.New York:Churchill Livingstone,1997.385~411.
10 Malgrange B,Belachew S,Thiry M.Proliferative generation of mammalian auditory hair cells in culture[J].Mech Dev,2002,112:79.
11 Walton J,Gibson WP,Sanli H,et al.Predicting cochlear implant outcomes in children with auditory neuropathy[J].Otol Neurotol,2008,29:302.
12 Teagle HF,Roush PA,Woodard JS,et al.Cochlear implantation in children with auditory neuropathy spectrum disorder[J].Ear Hear,2010,31:325.
13 Rance G,Barker EJ.Speech perception in children with auditory neuropathy/dyssynchrony managed with either hearing aids or cochlear implants[J].Otol Neurotol,2008,29:179.
14 Zanetti D,Guida M,Barezzani MG et al.Favorable outcome of cochlear implant in VIIIth nerve deficiency[J].Otol Neurotol,2006,27:815.
15 陈雪清,王靓,孟黎晖,等.婴幼儿人工耳蜗植入术后听觉能力的发育[J].临床耳鼻咽喉头颈外科杂志,2005,19:442.
(2010-11-02收稿)
(本文编辑 雷培香)
Cochlear Nerve Deficiency in Children
Mo Lingyan*,Yan Fei,Liu Hui,Chen Jing,Chen Xueqing,Huang Lihui,Han Demin
[*Beijing Tong Ren Hospital,Capital Medical University Beijing Institute of Otolaryngology;Key Laboratory of Otolaryngology Head and Neck Surgery(Capital Medical University),Ministry of Education,Beijing,100005,China]
Objective To review the clinical results of a group of children with cochlear nerve deficiency(CND).Methods 20 cases(37 ears)confirmed CND by inner ear magnetic resonance imaging(MRI)were included in this study.The subjects aged from 10 months to 4 years old.Their case history,imaging results and audiological data were retrospectively analyzed.Results Most of the cases had no particular history.The inner ear MRI ranged from isolated CND to accompanied cochlear and/or vestibular malformation.Click ABR varied from no response at the maximum output level to the lowest threshhold of 80 d B n HL.DPOAE and/or CM were present in 45%of the ears with CND only while they were absent in all of the ears with cochlear malformation.2 were implanted with cochlear implants on the affected ear and with detailed results of infant and toddler meaningful auditory integration scale(IT-MAIS)measurement up to 1 year after the switch on.The results in one of them were comparable to that of the children with cochlear loss while other was nonuser of the device.Conclusion Depending on the presence or absence of inner ear malformation and other factors,there is variability in imaging and audiological results in children with CND.
Cochlear nerve deficiency; Auditory neuropathy;Inner ear malformation
10.3969/j.issn.1006-7299.2011.05.004
R764.4
A
1006-7299(2011)05-0402-04
△ 北京市卫生系统高层次卫生技术人才培养基金(2009-3-29)、国家“十一五”科技支撑计划(2007BAI18B12)、科技部国际合作课题(2009DFA32200)及“十一五”国家科技支撑计划重点项目(2008BAI50B08)资助
1 首都医科大学附属北京同仁医院 北京市耳鼻咽喉科学研究所 耳鼻咽喉头颈科学教育部重点实验室(首都医科大学)(北京 100005);
2 首都医科大学附属北京同仁医院放射科
莫玲燕,女,北京人,博士,主任医师,主要从事临床听力学研究工作。
CND患儿多无特殊病史,根据是否伴有内耳畸形及内耳畸形的种类,其听力学表现多样,诊断主要依据影像学检查,应注意鉴别诊断,以便制定合理有效的干预措施。
