肿瘤患者全胃切除连续间置空肠代胃消化道重建术观察
2011-05-30苏志伟詹利永
苏志伟 詹利永
浙江省嘉兴市妇幼保健院普外科,浙江 嘉兴 314000
根治性全胃切除术是最常见的胃癌手术方式之一,沿用至今已有一百余年的历史[1]。全胃切除后消化道重建的通畅功能通过简单的食道空肠吻合即可满足,但全胃切除术后,患者常有进食量减少及食欲减退,又由于食物排空过快,与消化液接触搅拌不够而造成吸收不佳,终致患者体质量减轻和明显营养不良,生活质量普遍下降[2]。为了防止这些问题的出现,选择操作简便、术后并发症少、手术死亡率低和能保证患者一定生活质量的手术是我们的共同取向。本科室自2000年1月—2010年3月采用连续间置空肠代胃术应用于全胃切除消化道重建42例,明显改善患者生活质量,现报告如下。
1 资料和方法
1.1 临床资料
本组42例患者,男性28例,女性14例。年龄35~75岁,平均年龄54岁。全组经上消化道钡餐、胃镜及病理检查确诊。肿瘤部位:贲门及胃体区14例,胃体及胃窦区20例,侵犯全胃者5例,胃体区3例。组织学类型:腺癌38例,未分化癌2例,胃恶性淋巴瘤1例,胃间质瘤1例。临床病理分期:Ⅱ期3例,ⅢA期27例,ⅢB期10例,Ⅳ期2例。大体分型:BorrmannⅡ型12例,BorrmannⅢ型22例,BorrmannⅣ型8例。单纯性全胃切除34例,联合脏器或扩大全胃切除8例。
1.2 手术方法
本组42例患者均实施全胃切除,消化道重建采用连续性空肠间置代胃术式,手术具体步骤:⑴全胃切除术后,取在Treitz韧带远端40 cm处行食管-空肠端侧吻合。⑵输出襻肠段在距食管-空肠吻合口35 cm处与十二指肠残端行侧端吻合。⑶空肠-十二指肠吻合口下方5 cm处之输出襻与距Treitz韧带下方20 cm处输入襻之间Braun式侧吻合。⑷分别于空肠-十二指肠吻合口远侧2 cm处及输入支肠段距食管-空肠吻合口5 cm处各用丝线作适度缝扎。Braun吻合距Treitz韧带10 cm,食管-空肠吻合口选用强生25号吻合器吻合,十二指肠、空肠吻合采用手工法吻合。重建方式如图1。
1.3 随 访
按Visick分级指数将随访患者分为Ⅳ级:Ⅰ级为基本正常;Ⅱ级有轻度症状;Ⅲ级有严重症状;Ⅳ级为不能耐受。对术后并发症(返流性食管炎、倾倒综合征、Roux-en-Y综合征)的发生率、体征的变化以及血系列化指标进行记录,并于术后12个月进行胃肠道钡餐检查,以观察代胃肠管扩张情况。
1.4 统计学处理
运用SPSS13.0统计软件,计量资料用表示,各组或组间比较用方差(Student-Newman-Keuls)分析或χ2检验,以P<0.05为差异有统计学意义。
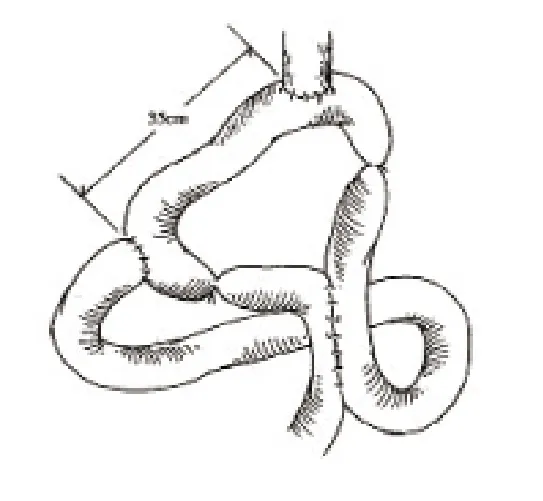
图 1 功能性间置空肠代胃术Fig.1 Digestive tract reconstruction by continuous jejunal interposition after total gastrectomy
2 结 果
42例患者术后均恢复良好,痊愈出院,无吻合口狭窄及吻合口漏发生,无返流性食管炎症状出现,亦无倾倒综合征发生。对所有病例均进行随访,随访时间为术后6、12个月,患者的VISICK指数为Ⅰ~Ⅱ级,即术后无症状;3例患者术后3个月内偶有餐后胸骨后不适,口服黏膜保护剂后症状消失,6例患者术后6个月内出现咽喉部的烧灼感,4例口服吗丁啉片后逐渐缓解。25例出现长时间站立、负重后剑突下牵扯感,稍休息后缓解。所有随访病例均无倾倒综合征出现。其中有3例因糖尿病需严格控制饮食造成体质量明显减轻外,其余病例体质量及血生化指标较术前均有明显的提高;经胃肠道吞钡造影检查发现本级病例在术后3~4个月内代胃肠管明显扩张,食物滞留量和胃代替物排空时间较为满意。术后6、l2个月检测体重、血红蛋白、血浆总蛋白、白蛋白、外周血淋巴细胞计数等,发现血红蛋白、外周血淋巴细胞数术后较术前有所提高,但差异无统计学意义(P>0.05,表l);术后l2个月与6个月相比,各指标均有所改善,经t检验差异无统计学意义(P>0.05)。
3 讨 论
有研究认为,全胃切除后食物排空时间可能是影响体质量恢复的一个重要因素[3-4],且胰-食物不同步可能是造成全胃切除术后营养不良的主要原因[5-6]。詹文华[7]认为,理论上,全胃切除后消化道重建应该符合下列基本原则:⑴形成食物贮库;⑵保持十二指肠食物通道的连续性;⑶防止反流性食管炎;⑷食物贮库向小肠呈梯度排空。
在临床,常用的全胃切除消化道重建术基础术式常有:Lahey法(袢式Braun吻合法)、单纯Roux-en-Y吻合术和空肠间置吻合术。Rouxen-Y吻合术能减少碱性肠液的反流,但食物排空较快,易产生倾倒综合征;Roux-en-Y加袋术是Roux-en-Y的改良,增加了代胃容量,延缓了食糜的排空时间,但因十二指肠被旷置,食物不经十二指肠导致胆胰失同步化而影响消化和吸收。因此,全胃切除后,建立一个有充分贮存功能的代胃,并保持摄入食物通过十二指肠更符合生理状况,有利于营养物质的消化、吸收[8]。但自1897年Schlatter等[9]首创食管-空肠端侧吻合术后,至今还没有一种方法使食物摄入、消化、吸收问题达到完美无缺的程度。1999年国内郝希山等[10]在袢式吻合的基础上加以改良,创用功能性连续空肠间置代胃术,此术式仍保持食物从十二指肠通过,间置肠段有储存作用和较好的消化吸收功能,较少或不发生“无胃综合征”(反流性食管炎、倾倒综合征、腹胀及腹泻等),改善了患者术后营养状况和生活质量,手术安全、简便,是一种理想的消化道重建术式。我科室从2000年起至今,按其重建方式完成42例病例,全部病例手术顺利完成,术后没有发生吻合口漏、大出血或其他严重并发症,术后短期内即可达到满意的饮食效果,反流性食管炎、倾倒综合征、营养不良、滞留综合征等发生率低。术后12个月时予以钡餐检查11例,代胃容量均在300 mL以上,排空时间为30~120 min。代胃的空肠达40 cm,即使存在一部分碱性十二指肠液反流到代胃内,也较难进入食管,能有效地防止反流性食管炎的发生。42例患者中,术后6个月出现反流性食管炎11例,术后12个月后出现仅为4例,分别为26.19%和9.52%。术后6和l2个月时检测体重、血红蛋白、血浆总蛋白、白蛋白、外周血淋巴细胞计数与术前相比,血红蛋白、外周血淋巴细胞数较术前有所提高,但差异无统计学意义(P>0.05);术后12个月与6个月相比,各指标均有所改善,但差异均无统计学意义(P>0.05)。连续间置空肠代胃不需切断肠管,术中污染少,肠管血运好,减少吻合口漏发生。手术操作简便省时,若食管空肠和十二指肠吻合采用管状消化道吻合器,操作更省时省力。
连续性间置空肠代胃术是根据消化道解剖生理的特点,以近段空肠原位构建一个保留神经生理功能的“代胃”:将35 cm的空肠段顺行置于食管与十二指肠之间的胃床上,并分别与食管及十二指肠断端吻合;在两吻合口旁侧分别适度结扎空肠以阻断肠腔。由于这段空肠系膜完好、肠壁神经传导和肌肉运动功能得以保存,防止由此导致代胃空肠功能紊乱和排空延迟[11],使术后患者拥有一个具有良好储存及运输功能的代胃,对预防术后并发症(返流性食管炎、倾倒综合征、Roux-en-Y综合征)有较好的作用。由于空肠不受迷走神经切断的影响,并保持了空肠的连续性,与十二指肠吻合后,避免了十二指肠旁置的缺点,食糜仍通过十二指肠,胃肠激素(如胆囊收缩素、肠抑胃肽等)得以正常分泌,进而激惹、刺激胰酶和胆汁的消化作用,防止胆胰失同步化,改善患者术后营养状态,为术后进一步放、化疗争取时间。输入袢和输出袢两端的适度缝扎和Braun吻合,尽可能的减少了术后食物和胆汁的反流;间置空肠的代胃作用,增加食物储存,降低术后倾倒综合征。连续间置空肠代胃术对全胃切除术后患者有提高生活质量和改善营养的潜在价值[12]。

表 1 全胃切除连续间置空肠代胃术前术后随访12个月营养指标Tab.1 The nutritional indices on preoperative and postoperative of digestive tract reconstruction by continuous jejunal interposition after total gastrectomy followed up for 6 and 12 months
从理论上本案例肯定了食物经过十二指肠的必要性。然而,确定一种统一的标准重建术式对胃癌患者并非适宜[13]。对于是否保留十二指肠通道仍有争议,尽管有些学者认为保留十二指肠更符合生理状况,有利于患者的营养吸收,但是多数学者认为保留十二指肠通道并不能使患者有更好的营养状况和更低的术后并发症[14]。同时我们认为,若幽门上、下存在根治欠理想的淋巴结转移或胃窦周围可能存在癌残留复发者,经十二指肠的重建术式应慎重,以防止十二指肠空肠吻合口梗阻而影响生存期。
[1]朱正纲.全胃切除与消化道重建术在胃癌治疗中的临床意义[J].中国普外基础与临床杂志, 2006, 13(1): l5-16.
[2]尹浩然.从术式演变谈全胃切除术后消化道重建的原则[J].中华胃肠外科杂志, 2004, 7(1): 12-13.
[3]ADACHI S, INAGAWA S, ENOMOTO T, et al.Subjective and functional results after total gastroemy: prospective study for long term comparison of reconstruction procedures[J].Gastric Cancer, 2003, 6: 24-29.
[4]ODA Y, NISHIJIMA J, OKU K, et al.Usefulness of an cstimation of physiologic ability and surgical stress (E-PASS)scoring stem to predict the incidence of postoperative cornpfications in gastrointestinal surgery[J].World J Surg,2005, 29: 1029-1033.
[5]CAO X D, WANG Y N.Choice and evaluation of operational types of alimentary reconstruction after total gastrectomy[J].J Chinese Cancer, 2006, 16: 240-244.
[6]ZHERLOV G, KOSHEL A, ORLOVA Y, et al.New type of jejunal interposition method after gastroctomy[J].World J Surg, 2006, 30: 1475-1480.
[7]詹文华.消化道重建[J].中国实用外科杂志, 2004, 24(9):514-516.
[8]陈俊青, 詹文华.全胃切除术后消化道重建是否需要保留食物十二指肠通道功能性[J].国外医学外科学分册,2005, 32(2): 111-114.
[9]ZONCA P, MALY T, HEROKOVA J, et al.Reconstruction after total gastrectomy[J].Lek Listy, 2002, 103(11): 414-417.
[10]郝希山, 李强, 尹健.全胃切除术后不同代胃术术式的评价[J].外科理论与实践, 2003, 8(1): 34-36.
[11]KONO K, LIZUKA H, SEKIKAWA T, et al.Improved quality of life with jejunal pouch reconstruction after total gastrectomy[J].Am J Surg, 2003, 85(2): 150.
[12]PAN Y, LI Q, WANG D C, et al.Beneficial effects of jejunal continuity and duodenal food passage after total gastrectomy:a retrospective study of 704 patients[J].Eur J Surg Oncol,2008, 34(1): 17.
[13]陈俊青.正确掌握胃肠癌根治切除的消化道重建[J].中国实用外科杂志, 2004, 24(9): 513.
[14]曹学东, 王亚龙.全胃切除后消化道重建方式选择与评价[J].中国癌症杂志, 2006, 16(3): 240-242.
