HPLC双指标研究大孔树脂纯化甘草酸的优化工艺及图谱分析
2011-05-26宋丽军赵文昌
宋丽军, 赵文昌
(广东医学院药学院,广东东莞 523808)
HPLC双指标研究大孔树脂纯化甘草酸的优化工艺及图谱分析
宋丽军, 赵文昌*
(广东医学院药学院,广东东莞 523808)
目的 在大孔树脂纯化甘草酸工艺研究基础上,探讨进一步纯化甘草酸的优化方法。方法 采用高效液相色谱法检测甘草酸、甘草苷,优化AB-8大孔吸附树脂纯化甘草酸最佳上样量,采用HPLC图谱分析提取物成分变化。结果
HPLC图谱显示优化后提取物未见甘草苷,峰A~D等未知成分部位的峰明显减小;甘草酸纯度由26.3%达到35.8%。结论 所建立的甘草酸、甘草苷双指标优化甘草酸的大孔树脂富集纯化工艺的方法简便、合理,可有效去除甘草提取物中甘草苷及某些杂质成分的干扰。
甘草酸;甘草苷;大孔树脂;高效液相色谱法;工艺优化
甘草Glycyrrhiza Radix et Rhizoma是一味应用极广的中药材,素有“十方九草”之称。国内外学者对甘草的化学成分和药理作用进行了许多研究,认为主要有效成分是甘草酸和黄酮类化合物[1]。甘草酸具有抗炎、抗病毒等多种药理作用,为得到纯度较高的甘草酸提取物,一般常用煎煮法[2],超声提取法[3],稀氨水回流提取[4]等方法提取,采用大孔树脂法[5-6]、酸沉反复结晶、双水相萃取等工艺纯化,其中大孔树脂法一般可从大孔树脂的种类和用量、药液的吸附流速、洗脱用乙醇的浓度和流速、洗脱液收集点、洗脱乙醇用量等方面优选纯化工艺。但是我们按上述参数优选大孔树脂富集纯化甘草酸的工艺后发现,甘草酸有效部位中仍含有非目标成分甘草苷,从而影响有效部位的纯度。中药成分复杂,理化性质各异,针对大孔树脂吸附解脱前后的多指标成分变化控制工艺参数选择的研究较少。为此我们进行深入研究,首次建立HPLC法测定甘草酸、甘草苷双重指标考察优选甘草酸纯化工艺的方法,仅通过对上样量的优化,达到有效去除甘草苷及未知成分部位干扰的目的。目前大孔树脂纯化工艺中关键技术参数-上样量的选择主要是检测目标成分单一指标确定上样量[7],本实验建立的双重指标检测可对其它中药采用大孔树脂纯化工艺研究关键技术参数的方法选择提供参考和依据。
1 实验部分
1.1 仪器与试药 Agilent 1200 Series高效液相色谱系统(四元梯度泵、自动进样器、G1315A紫外-DAD检测器、ChemSation色谱工作站);超声波清洗器(昆山市超声仪器有限公司)。AUW 220D十万分之一电子分析天平(日本岛津公司)。甘草酸铵(批号:110731-200511)、甘草苷对照品(批号:111521-200202),中国药品生物制品检定所。甘草药材购于广东大参林连锁药店有限公司东莞市大岭山分店,经鉴定符合《中国药典》2010年版规定。AB-8大孔吸附树脂(天津市光复精细化工研究所)。乙腈(Sigma公司,色谱级);Milli-Q Biocel超纯水系统 (广州东锐科技有限公司);其余试剂均为分析纯。
2 方法与结果
2.1 树脂的预处理 树脂以2BV 5%NaOH 80℃浸泡6 h,淋净碱后以蒸馏水洗至流出液呈中性,再以2BV 95%乙醇浸泡24 h,充分溶胀,用乙醇洗至紫外吸收小于0.03,再以蒸馏水洗至无醇,待用。
2.2 HPLC测定样品中甘草酸、甘草苷 方法参见文献[8],测定甘草酸的色谱条件为色谱柱Kromasil 100-5 C18(4.6 mm ×250 mm,5 μm);流动相 甲醇-0.06 mL/L醋酸铵(冰醋酸调pH为4)66∶34;体积流量:0.7 mL/min;波长250 nm;柱温室温。测定甘草苷的色谱条件为色谱柱同上;流动相 乙腈-0.5%冰醋酸(1∶4),体积流量:0.7 mL/min;波长276 nm;柱温室温。
2.3 甘草氨水初提物的制备 称取甘草饮片适量,HPLC分别测定甘草饮片中甘草酸、甘草苷,8倍生药量0.3%稀氨水回流提取2次,1 h/次,合并提取液,浓缩样品液至4倍生药量,加稀盐酸调pH值至2,静置30 min,离心20 min(3 000 r/min),沉淀60℃烘干,即得甘草氨水初提物。按2.2项下测定甘草酸粗粉中甘草酸、甘草苷。
2.4 甘草酸的纯化
2.4.1 以甘草酸为指标确定上样量,制备甘草提取物T1根据对AB-8大孔吸附树脂纯化甘草酸的上柱液浓度、pH、吸附速率、吸附时间等工艺指标的优化考察,将甘草酸粗粉稀释10倍,调 pH6.5,吸附速率为 1 mL/min,分别以0.5 ~8BVmL上经过预处理的AB-8大孔树脂柱(2 cm×15 cm)吸附30 min,再用蒸馏水洗柱,收集残液,准确记录残液体积,HPLC测定残液中甘草酸的浓度。结果见图1。
从图1中可以看出当上样量为4BV时,甘草酸泄漏开始显著增加,因此初步确定上样量为4BV,并制备甘草提取物T1。
2.4.2 甘草酸-甘草苷为指标确定最佳上样量 根据2.4.1 项的结果,取 0.5、1、1.5、2、3、4 BV 甘草酸粗粉 10 倍稀释液,调pH 6.5,吸附速率为1 mL/min,上经过预处理的AB-8大孔树脂柱(2 cm×15 cm)吸附30 min,根据对洗脱及浓度、洗脱速率、洗脱剂用量等工艺指标的优化考察结果,用4BV蒸馏水洗柱至洗脱液无色,再分别以7BV 50%乙醇溶液洗脱各树脂柱,体积流量2 mL/min,收集洗脱液,浓缩,HPLC测定甘草苷,结果见图2。

图1 以甘草酸为指标对上样量考察

图2 以甘草苷为指标对上样量二次考察
从图2中可以看出当上样量为1BV mL时,甘草苷在洗脱液中开始显著增加,因此综合对甘草酸、甘草苷两个指标的考察,确定最佳上样量为1BV,并制备甘草提取物T2。
2.5 甘草药材、甘草氨水初提物、甘草酸提取物T1、T2的HPLC图谱比较 本实验采用中国药典[8]HPLC方法测定甘草酸,不同样品测得甘草酸的HPLC图谱相似,而采用中国药典[8]HPLC方法测定甘草苷,图谱中变化明显。故以样品的甘草苷图谱进行比较,见图3~图7。
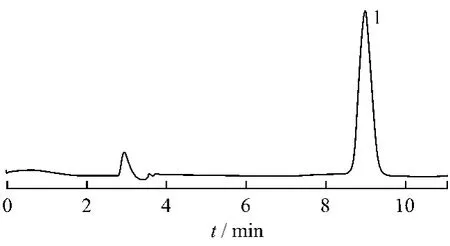
图3 甘草苷对照品HPLC图谱

图4 甘草药材HPLC图谱

图5 甘草氨水初提物HPLC图谱

图6 甘草酸提取物T1 HPLC图谱
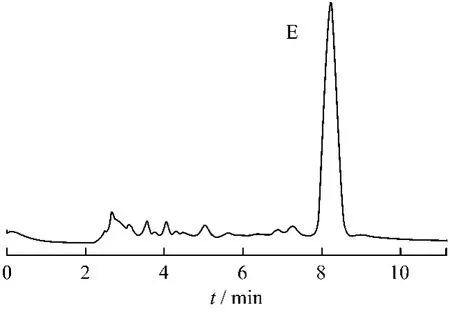
图7 甘草酸提取物T2 HPLC图谱
图4显示甘草药材除具有明显的甘草苷的色谱峰(峰1)外,还有未知成分峰A~E。经过氨水初提,峰B~D部位峰高明显降低;经过大孔树脂纯化工艺1,T1的图谱中只有峰A、E及甘草苷比较明显;采用大孔树脂纯化工艺2,T2的图谱中只有峰E比较明显,甘草酸提取物基本已检测不到甘草苷,未知成分部位的峰A~D等亦不明显。
2.6 HPLC测定甘草饮片、甘草酸粗粉、甘草酸提取物(T1、T2)甘草酸、甘草苷比较 HPLC分别测定甘草酸提取物T1、T2中甘草酸、甘草苷,结果见表1。
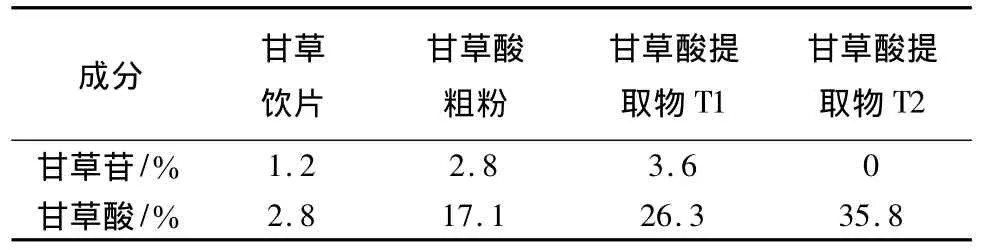
表1 HPLC测定不同样品中甘草酸、甘草苷(x ± s,n=3)
计算结果显示,通过工艺优化处理,综合选择最佳上样量,甘草酸提取物甘草酸纯度由26.3%达到35.8%。
3 讨论
3.1 大孔树脂法为目前进行中药有效成分、有效部位富集纯化常用方法,常以目标成分作为单指标筛选工艺中上样量、洗脱剂等关键技术参数的选择依据,并形成一定研究模式。但值得注意的是中药成分复杂,只考虑单成分的吸附、洗脱,其它成分过柱的行为不清楚,会成为影响所得产品纯度的潜在因素。这一点在已有的大孔树脂工艺筛选模式中很少为人们所注意到。本研究表明单纯只考虑甘草酸单一成分,确定上样量等纯化条件后,洗脱液中确实仍含甘草苷及未知杂质成分,从而影响纯化效果。
3.2 本实验采用HPLC测定富集目标成分-甘草酸、去除非目标成分-甘草苷,优化甘草酸大孔树脂纯化工艺的关键技术参数-上样量,HPLC图谱、测定结果显示,该方法简便、合理,可有效去除非目标成分,提高甘草酸提取物的纯度。
3.3 比较甘草酸提取物T1图谱和甘草酸提取物T2图谱,采用最佳上样量不仅去除甘草苷,也减少了图谱中其它未知杂质成分的流出。所以,甘草酸提取物T2的甘草酸纯度有所提高。
3.3 采用HPLC测定药材、提取物T1及T2甘草苷的量,样品色谱图中峰E(出峰时间约8 min)始终存在,值得进一步深入研究。
[1]肖培根.新编中药志:第一卷[M].北京:化学工业出版社,2000.
[2]吴伟康,奉建芳,黄小蕊.甘草提取工艺的初步研究[J].中草药,2001,32(3):210-212.
[3]冯斯停,唐其柱,易方方.甘草酸提取纯化技术研究现状[J].中国药师,2006,9(1):61-63.
[4]贺小贤,陈 合.甘草酸提取工艺研究[J].陕西科技大学学报,2004,22(6):26-29.
[5]王 洋,王跃生,闫 寒.大孔吸附树脂对甘草酸的吸附与解吸性能研究[J].中国中药杂志,2006,34(4):295-297.
[6]刘 倩,仰榴青,吴向阳.大孔吸附树脂纯化甘草酸的研究[J].中药材,2003,26(5):48-50.
[7]李 红,李炳奇,刘 红.XDA-1型树脂对甘草黄酮吸附-解吸效果的研究[J].中成药,2007,29(6):830-833.
[8]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:80.
[9]高素莲,王雪梅.甘草中皂甙和黄酮类化合物的提取分离[J].安徽大学学报,2000,24(4):70-74.
[10]马 明,石 巍.从甘草中提取甘草酸和黄酮类化合物的研究[J].化工时刊,2000,(6):8-11.
[11]李炳奇,汪河滨,李学禹.超声法联合提取甘草黄酮和甘草酸的研究[J].山东中医杂志,2005,24(1):38-40.
R284.2
B
1001-1528(2011)07-1252-03
2010-06-07
宋丽军(1969—),女,副主任药师,博士,主要从事中药新药研究与质量标准制定。Tel:(0769)22896547,E-mail:songlijun6981@126.com
*通信作者:赵文昌(1967—),男,博士,主要从事缓控释制剂研究。Tel:(0769)22896561,E-mail:zhaowenchang@126.com
