BCA法测定食品中的微量铜
2011-04-06冯志明
刘 璇,冯志明
(湖南师范大学化学与化工学院,湖南 长沙 410008)
BCA法测定食品中的微量铜
刘 璇,冯志明*
(湖南师范大学化学与化工学院,湖南 长沙 410008)
研究BCA(2,2'-联喹啉-4,4'-二甲酸二钠盐)与铜的显色反应,建立测量食品微量铜的光度分析方法。在盐酸羟胺存在条件下,pH11.0缓冲介质中,BCA试剂与铜在物质的量的比为2∶1的条件下反应生成的紫色络合物,λmax=562nm,ε562nm=7.72×103L/(mol·cm),铜含量在0~4.8μg/mL内符合比尔定律;经测定茶叶和海带中的铜含量,结果与原子吸收法的测定结果相符。结果表明:该方法稳定准确,可用于食品中微量铜的测定。
铜;测定;BCA法;分光光度法
铜是人体必需的微量元素,对机体造血、新陈代谢、细胞生长、某些酶的活性及内分泌等功能有重要作用。饮用水及食品中均含有一定量的铜,但如果人体摄入的铜过量将对人体构成危害。近年由于农业上大量使用含铜杀虫剂和除霉剂,加上工业“三废”的污染,使许多食品中铜含量超标。因此,食品中铜的允许限量一般不超过5~20mg/kg[1]。测定食品中铜的含量是食品检验中的一项重要工作。目前,食品中微量铜的测定常用原子吸收光谱法[1-5]和光度法[6-10]。前者虽灵敏度高、选择性好,但仪器昂贵、分析费用高,而后者操作简便、精密度良好、仪器价格低,易于普及。
茶叶和海带中微量铜的测定多采用原子吸收法(atomic absorption spectrometry,AAS)[11-13]。文献虽报道了许多新型有机显色剂用于光度法测定铜,但用于食品中铜的分析时,大量钙、镁、铁和锌的干扰仍然较重[14-17]。为了进一步提高光度法测定铜的选择性,研究了新试剂BCA与铜的显色反应。BCA(2,2'-联喹啉-4,4'-二甲酸二钠盐)是测定蛋白质含量的一种常用试剂[18]。在碱性条件下,通过盐酸羟胺将二价铜离子还原为亚铜离子,亚铜离子和BCA钠盐反应生成紫色络合物(图1)。文献报道了BCA法测定血清和生物样品中的铜[19]、药物中的地尔硫卓[20]和饮料中的鞣酸[21],但BCA法测定茶叶和海带中微量铜的报道较少。

图1 BCA与亚铜离子形成的紫色配合物Fig.1 Chemical structure of BCA-Cu+ complex (violet in color)
本实验研究了以BCA为显色剂在水中直接比色测定食品中微量铜的方法,通过测定其在562nm处的吸光度建立茶叶和海带中微量铜的测定方法。
1 材料与方法
1.1 材料与试剂
茶叶和海带洗净于80℃烘干后备用。
BCA 美国Sigma公司;其他试剂均为分析纯,实验用水为二次蒸馏水。
1.2 仪器与设备
722S型分光光度计 上海菁华科学仪器有限公司;AA7000W原子吸收光谱仪 北京东西分析仪器有限公司;PHS-25型酸度计 上海雷磁科学仪器有限公司;电子分析天平 上海精密科学仪器有限公司;UV-2000双光束紫外分光光度计 北京莱伯泰科仪器公司。
1.3 溶液的配制
BCA试剂(1g/100mL):分别称取2.50g BCA、5.00g碳酸钠(Na2CO3·H2O)、2.40g碳酸氢钠(NaHCO3)、1.00g氢氧化钠(NaOH)、0.40g酒石酸钾钠(Na2C4H4O6· 2H2O),适量水溶解后,用2g/100mL NaOH溶液和固体NaHCO3调节pH11.0,定容至250mL。
Cu(Ⅱ)标准溶液(10μg/mL):称取0.5000g纯铜,置于100mL烧杯中,加入10.0mL浓硝酸,置于电炉上加热溶解,并蒸发至近干,冷却后加水,加热溶解;冷却后定容至500mL即为1000μg/mL的Cu(Ⅱ)标准溶液储备液。取2.50mL该储备液稀释至250mL,即为10μg/mL的Cu(Ⅱ)标准溶液。
盐酸羟胺溶液(10mg/mL):称取2.50g盐酸羟胺,适量水溶解后定容至250mL。
1.4 样品处理
准确称取烘干并磨细的海带或茶叶5.00~10.00g,放入250mL锥形瓶中,先加入5.0mL硝酸,加热蒸发至近干,稍冷,再加入2.0mL硫酸,继续加热,少量多次加入硝酸以维持氧化条件,直至溶液无色透明,继续加热至产生硫酸雾,硝酸完全除去,冷却,加适量水,温热溶解可溶盐,若有沉淀应过滤(为提高消解效果,常加入少量H2O2)。冷却后滴加NaOH溶液,用酸度计控制pH值约为11.0,转入100mL容量瓶中定容,摇匀即得样品测试液。
1.5 测定方法
BCA比色法:于25mL容量瓶中加入一定量的铜标准液,然后加入3.00mL盐酸羟胺溶液,振荡;再加入5.00mL BCA 试剂,用水稀释至刻度,充分摇匀后放置15min,待显色完全后在分光光度计上,以相应的试剂空白(用等量的二次蒸馏水代替铜标准液,其他试剂加入同上)作参比,用1cm比色皿于562nm处测量溶液的吸光度,以此进行铜的定量分析。
原子吸收法:按照GB/T 5009.13—2003《食品中铜的测定方法》进行。测定条件:火焰类型:乙炔/空气;测定波长324.75nm(铜空心阴极灯);灯电流2mA;狭缝0.2nm。
2 结果与分析
2.1 吸收光谱
按照实验方法在不同波长处,绘制铜络合物对蒸馏水的吸收光谱曲线(图2)。结果表明BCA与Cu(Ⅰ)离子形成的紫色络合物λmax=562nm。本实验选择的测定波长为562nm。
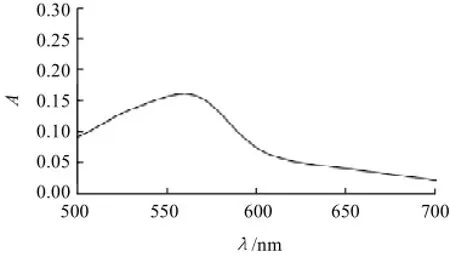
图2 BCA与亚铜离子形成的紫色配合物的吸收光谱Fig.2 Visible absorption spectrum of BCA-Cu+complex
2.2 单因素试验
影响吸光度的因素较多(各试剂用量、pH值、温度等),本实验采用单因素轮换法确定最佳反应条件。
2.2.1 pH值的影响
用固体NaOH或NaHCO3调节酸度进行测定,结果表明:溶液pH值为11.0~11.5时,吸光度A562nm较大且稳定(图3)。本实验选用pH11.0的Na2CO3-NaHCO3缓冲液进行测定。

图3 酸度对吸光度的影响Fig.3 Effect of acidity on absorbance at 562 nm of BCA-Cu+complex
2.2.2 温度的影响
在不同的温度(10~60℃)条件下按照实验方法进行测定,结果表明:40℃以下吸光度变化很小,温度对其影响不大。本实验选择在室温条件下进行。
2.2.3 显色时间的影响
反应在室温条件下生成配合物的速度比较快,测定结果表明:15min后显色完全,A562nm达到最大且稳定,显色完全后体系至少可稳定30min。
2.2.4 盐酸羟胺的影响
仅改变盐酸羟胺用量进行测定,结果表明:当盐酸羟胺的用量为3mL时,A562nm最大(图4)。本实验选用3.00mL盐酸羟胺。

图4 盐酸羟胺用量对吸光度的影响Fig.4 Effect of hydroxylamine hydrochloride amount on absorbance at 562 nm of BCA-Cu+complex
2.2.5 BCA试剂用量的影响
仅改变BCA试剂的用量进行测定,结果表明:当BCA试剂在用量为5~6mL时,吸光度A562nm最大(图5)。本实验选用5.00mL BCA试剂。

图5 BCA试剂用量对吸光度的影响Fig.5 Effect of BCA reagent amount on absorbance at 562 nm of BCA-Cu+complex
2.3 工作曲线和检测限
在最佳实验条件下,分别取0.50、1.00、1.50、2.00、2.50、3.00、5.00、7.00、10.00、12.00mL Cu (Ⅱ)标准溶液按实验方法进行测定并绘制出工作曲线(图6)。实验结果表明,Cu(Ⅱ)的质量浓度在0~4.8μg/mL范围内与A呈良好的线性关系,线性回归方程和相关系数分别为A=0.1229C-0.0032,相关系数r=0.9998。由工作曲线斜率求得ε562nm=7.72×103L/(mol·cm)。
2.4 共存离子的影响
按照实验方法,Cu(Ⅱ)为1μg/mL且相对误差小于等于±5%时,共存离子的允许量(μg)为:Ca2+(100)、Mg2+(100)、Fe3+(5)、Zn2+(42)。Na+、F-、Cl-、不干扰。
2.5 样品分析
吸取一定量的样品测试液于25mL容量瓶中,加入2.00mL质量浓度为10g/100mL NaF溶液,按照实验方法操作,结果见表1。

表1 BCA法与原子吸收法测定样品中铜的结果Table 1 Results of copper content in kelp and tea determined by BCA and AAS methods
由表1可见,两种方法测定结果的相对误差均在5%范围内。海带样品组中,BCA法测得的铜含量为6.5229 μg/g,而原子吸收法的结果为6.6400μg/mL,经F检验,统计量F=10.29<F表[22];经t检验,t=2.44<t表[22],两组检验结果表明BCA法和AAS法对海带中铜的测定结果无明显差异。茶叶样品组中,BCA法测得的铜含量为12.8346μg/g,而原子吸收法的结果为12.9994μg/mL,经F检验,统计量F=5.33<F表[22];经t检验,t=1.38<t表[22],两组检验结果表明BCA法和AAS法对茶叶中铜的测定结果无明显差异。

表2 样品中铜的回收实验结果Table 2 Spike recovery rates of copper in kelp and tea determined by BCA method
由表1、2数据看出,本法测定结果与AAS法结果相吻合,加标回收率在99.8%~107.4%之间。因此,本实验建立的测定食品中微量铜的检测方法结果准确、可靠。
3 结 论
用BCA法测定食品中微量铜,不仅方法简便易行、选择性好,其最大的优点是:显色反应是在水溶液中完成,不需要通过萃取或加大量的有机溶剂来增加溶解度,而且反应不需要加热,在室温条件下就可完成,反应时间较快,这不仅简化了操作、减少了误差,而且应用于实际样品的测定效果理想。
[1]黄伟坤. 食品检验与分析[M]. 北京∶ 中国轻工业出版社, 1989∶ 203.
[2]中华人民共和国标准汇编. GB/T 5009.13—1996 食品中铜的测定方法[S]. 北京∶ 中国标准出版社, 1997∶ 52-54.
[3]万正杨, 闫江虹. 微波消解-原子吸收分光光度法测定茶叶中的微量元素[J]. 中国卫生检验杂志, 2006, 16(12)∶ 1459-1460.
[4]董丙坤, 徐慧琴. 原子吸收分光光度法测定蔬菜水果中的微量元素铜[J]. 河南农业, 2008(22)∶ 51-52.
[5]龚亚成, 卿三华. 原子吸收分光光度计测定铜含量的不确定度评定[J]. 中氮肥, 2009(6)∶ 61-64.
[6]李卫岗, 曹乃斌, 范稚莉. 进出口食品中微量铜的测定[J]. 中国国境卫生检疫杂志, 2004, 27(6)∶ 365-366.
[7]翟庆洲, 李景梅, 李牧. 光度法测定铜的进展[J]. 长春理工大学学报, 2008, 31(3)∶ 85-89.
[8]蔡湘雯, 张毅忠, 周岱. 催化动力学光度法测定食品中的微量铜[J].广州化工, 2009, 37(4)∶ 141-144.
[9]虞学俊, 李在均, 潘教麦. 光度法测定食品中微量铜[J]. 理化检验∶化学分册, 2005, 41(12)∶ 937-938.
[10]李国清, 林玉妹. 析相光度法测定食品中微量铜的研究[J]. 泉州师范学院学报∶ 自然科学, 2007, 25(2)∶ 65-67.
[11]李桂华, 侯法菊, 崔建军, 等. 原子吸收法测定海带微量元素的含量[J]. 食品科技, 2006(5)∶ 100-102.
[12]张举成, 刘卫, 易中周, 等. 湿法测定红河州野山茶中微量元素[J].食品研究与开发, 2008, 29(2)∶ 106-108.
[13]TAUTKUS S, KAZLAUSKAS R, KAREIVA A. Determination of copper in tea leaves by flame atomic absorption spectrometry[J]. Chemija, 2004, 15(4)∶ 49-42.
[14]SARMA L S, KUMAR J R, REDDY K J, et al. Development of an extractive spectrophotometric method for the determination of copper (Ⅱ) in leafy vegetable and pharmaceutical samples using pyridoxal-4-phenyl-3-thiosemicarbazone (PPT)[J]. J Agric Food Chem, 2005, 53 (14)∶ 5492-5498.
[15]汤轶男, 房贻龄, 侯波, 等. 以二溴茜素紫为显色剂吸收比-分光光度法测定地面水中痕量铜(Ⅱ)[J]. 理化检验∶ 化学分册, 2009, 45(7)∶768-771.
[16]董学畅, 肖敏, 张汝良, 等. DIPF光度法测定食品和水样中微量铜的研究[J]. 云南民族学院学报∶ 自然科学版, 2000, 9(2)∶ 90-91.
[17]翟庆洲, 杨丽娟, 徐安丽, 等. 对乙酰基偶氮胂吸光光度法测定微量铜[J]. 理化检验∶ 化学分册, 2000, 36(10)∶ 453-454.
[18]WALKER J M. The protein protocols handbook[M]. University of Hertfordshire Hatfield UK∶ Humana Press, 1996.
[19]BRENNER A J, HARRIS E D. A quantitative yest for vopper using bicinchoninic acid[J]. Analytical Biochemistry, 1995, 226(1)∶ 80-84.
[20]SABINO LARISSA Z L, MARINO DANIELE C, MOYA H D. Determination of diltiazem based on the reduction of Cu (II)-BCA complexes in micellar medium[J]. Canadian Journal of Chemistry, 2010, 88(6)∶533-539.
[21]MOYAA H D, DANTONIB P, ROCHA F R P, et al. A multicommuted flow-system for spectrophotometric determination of tannin exploiting the Cu (Ⅰ)/BCA complex formation[J]. Microchemical Journal, 2008, 88(1)∶ 21-25.
[22]陈声宗. 化工过程开发与设计[M]. 北京∶ 化学工业出版社, 2005∶ 334-335.
Spectrometric Determination of Trace Copper in Foods by BCA (2,2'-Biquinoline-4,4'-dicarboxylic acid disodium salt) Method
LIU Xuan,FENG Zhi-ming*
(College of Chemistry and Chemical Engineering, Hunan Normal University, Changsha 410008, China)
The colour reaction between BCA (2,2'-biquinoline-4,4'-dicarboxylic acid disodium salt) and copper was developed for determining trace copper in foods. In the presence of pH 11.0 buffer solution and hydroxylamine hydrochloride, BCA could react with copper (II) to form a purple complex with a ratio of 2∶1. The molar absorbance constant was 7.72 × 103L/(mol·cm) at 562 nm. The absorbance obeyed Beer sin the range of 0-4.8μg/mL Cu (Ⅱ). The established method was used for the determination of trace copper in tea and kelp. The determination results are consistent with the results from atomic absorption spectrometry (AAS) method. In conclusion, this method has the advantages of good accuracy, stability and can therefore be applied to the determination of trace copper in foods.
copper;determination;BCA method;spectrophotometry
O657.32
A
1002-6630(2011)14-0277-04
2010-11-07
湖南省教育科研项目(09C641)
刘璇(1986—),女,硕士研究生,主要从事应用化学研究。E-mail:xuan11221122@163.com
*通信作者:冯志明(1962—),男,副教授,硕士,主要从事食品生物技术研究。E-mail:fengzhiming@163.com
