Nd-Fe-B-O四元体系的热力学性质研究
2011-03-17韩义勇覃东海吴庆敏张修海
韩义勇 覃东海 吴庆敏 张修海
(1广西玉柴机器股份有限公司,广西玉林537005; 2广西大学有色金属材料及其加工新技术教育部重点实验室,广西南宁530004)
Nd-Fe-B磁体自1983年问世以来,因其具有高的剩磁、矫顽力和最大磁能积,且原料资源丰富、成本低廉,已广泛应用于计算机的磁盘驱动器、音圈电机、打印机、各种微型电机、核磁共振成像设备、电声器件、磁分离设备、磁力机械以及磁悬浮列车、宇宙飞船、人造卫星等领域。Nd-Fe-B磁体的理论磁能积为512kJ·m-3(64MGOe),是稀土永磁材料中最有代表性的一类材料,也是目前实现产业化磁能积最高的一类磁体[1-3]。
目前,Nd-Fe-B磁体的研究主要集中在制备工艺方面,对Nd-Fe-B体系的热力学性能研究很少,但是,Nd-Fe-B体系的热力学性质对改进制备工艺有重要的指导意义。根据热力学定律,对于一个相变或化学反应过程,如果吉布斯自由能(ΔG)小于零,则反应能够自动进行,否则,反应不能自动进行。况且,过程的吉布斯自由能越小,反应越容易进行[4]。
根据Nd-Fe-B三元相图,选择一种合金成分(如图1所示)分析它相变过程中的热力学性能。图1中,δ相、γ相和α相是Fe的3种同素异构状态,分别称为 δ-Fe、γ-Fe和α-Fe,L相是液相,ф是 Nd2Fe14B相(主相),η是Nd2FeB3相。根据周守增等人的研究[5],在Nd-Fe-B三元体系中可能发生的相变有Fe2B、NdB4、Nd2Fe14B和 Nd2FeB3。众所周知,氧是一种很活泼的化学元素,很容易与Nd、Fe和 B元素发生氧化还原反应,氧对Nd-Fe-B磁体的制备有着重要的影响。因此,本文将研究Nd-Fe-B-O四元体系的热力学性质。
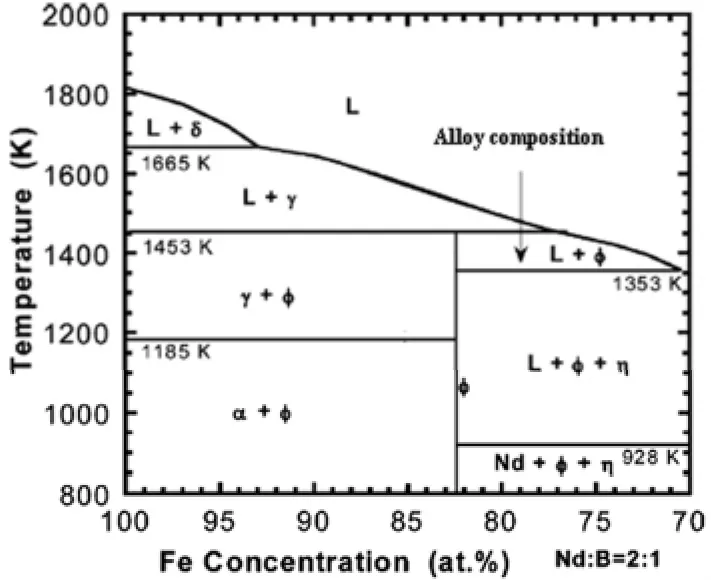
图1 Nd-Fe-B三元体系的平衡结晶相图
1 热力学模型
1.1 吉布斯自由能的状态方程
根据Van’t Hoff等温反应方程,对式(1)的可逆反应,A和B是反应物,C和D是生成物,它们的活度分别表示为:αA、αB、αC、αD,则在等压状态下,反应的吉布斯自由能如式(2)所示,标准状态下的吉布斯自由能如式(3)所示。


1.2 活度计算
在熔液体系中,组元i的活度定义为:

式(4)中,fi是组元i的活度系数,i%是组元i的质量百分含量。在多组元体系中,活度系数fi还必须考虑不同组元之间的相互作用,fi可用下式(5)计算。
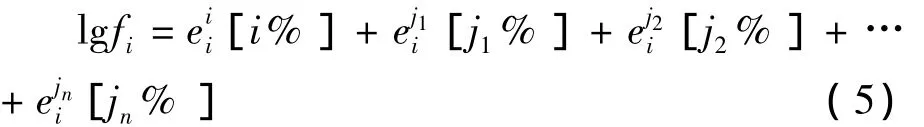

2 Nd-Fe-B-O四元体系的热力学数据计算
根据 Nd-Fe-B三元相图,合金的成分选为 Nd12.0Pr1.4B6.0Al0.3Cu0.1Co0.1Fe79.9,由于要考虑氧的影响,假定熔炼过程中氧的含量为0.1wt%。在这个多元体系中,由于Fe的含量为79.9wt%,因此,把Fe作为熔剂,其他元素作为熔质。由于其他元素相对于Fe的含量较小,把熔液当稀熔液处理,稀熔液符合亨利定律(Henry Law)。在这个多元体系中,主要的相变和氧化反应如下所示。


根据相关的热力学数据[7],结合式(3),可以计算出上述相变和氧化反应的标准吉布斯自由能ΔG0与温度T之间的关系如下所示:

由于Fe是熔剂,因此,αFe值为1.0,由于固态的活度是 1.0,因此,αFe2B、αNdB4、αNd2Fe14B、αNd2FeB3、αB2O3、αFe2O3和 αNd2O3的值都是 1.0。根据式(2),可计算出每个相变和氧化反应的吉布斯自由能ΔG如下所示:

根据相关的热力学数据[7],可以查到在Nd12.0Pr1.4B6.0Al0.3Cu0.1Co0.1Fe79.9这个多元体系中,不同组元之间的相互作用系数如下所示:

根据式(4)和(5),可以计算 αB为0.060 054、αNd为0.12、αO为0.000 687 4,再根据ΔG0和ΔG之间的关系,可以求得这个多元体系中主要相变和氧化反应的吉布斯自由能ΔG与温度T之间的关系如下所示:

3 Nd-Fe-B-O四元体系的热力学性质分析
根据图1的Nd-Fe-B三元体系的相图可知,以Nd2Fe14B为主相的Nd-Fe-B磁体的熔炼温度低于1 600K,因此,只要分析298K~1 600K之间的相关热力学数据就可以了。根据吉布斯自由能ΔG与温度T之间的关系式可知,ΔG与T之间呈线性的关系,因此,只要计算出多元体系中主要相变和氧化反应在298K和1 600K温度的ΔG值(如表1所示),就可以分析整个熔炼凝固过程中的热力学性质。

表1 主要相变和氧化反应在298K和1 600K温度的ΔG值
众所周知,Nd2Fe14B相是 Nd-Fe-B永磁体唯一的硬磁相,也就是说,Nd-Fe-B磁体的磁性能主要是由 Nd2Fe14B相来决定,因此,讨论Nd2Fe14B相与其他相及几个氧化物的热力学关系对改善Nd-Fe-B磁体的制备工艺有着重要的指导意义。根据表1的热力学数据,图 2比较了 Fe2B、NdB4、Nd2Fe14B(主相)、Nd2FeB34个主要相变的ΔG,图3比较了Nd2Fe14B(主相)相变与Nd2O3、Fe2O3和 B2O33个氧化反应的ΔG。由图2可知,ΔGNd2Fe14B<0,说明 Nd2Fe14B相的生成可以自动进行; ΔGNd2Fe14B<ΔGFe2B,说明 Nd2Fe14B相的生成比Fe2B 相的生成容易;ΔGNd2Fe14B> ΔGNdB4,且ΔGNd2Fe14B>ΔGNd2FeB3,说明 Nd2Fe14B 相的生成比NdB4相和 Nd2FeB3相的生成难;因此,在Nd-Fe-B磁体的制备过程中,要尽量避开NdB4相和 Nd2FeB3相的相变温度,即当制备过程中达到NdB4相和 Nd2FeB3相的转变温度时,要控制温度,尽快离开这些温度点。由图3可知,ΔGNd2Fe14B< ΔGB2O3,ΔGNd2Fe14B< ΔGFe2O3,ΔGNd2Fe14B<ΔGNd2O3,说明 Nd2O3、Fe2O3和 B2O33个氧化反应比 Nd2Fe14B相的相变更容易进行,也表明了Nd、Fe和B元素非常容易氧化,因此,在Nd-Fe-B磁体的制备过程中,要尽量降低体系中的含氧量。

图2 Fe2 B、NdB4、Nd2 Fe14 B(主相)、Nd2 FeB3 4个主要相变的ΔG对比

图3 Nd2 Fe14 B(主相)与Nd2 O3、Fe2 O3和B2 O3 3个氧化反应的ΔG对比
4 结论
本文根据Van’t Hoff等温反应方程和活度方程,建立了Fe-Nd-B-O四元热力学体系,通过对Nd-Fe-B合金体系主要合成反应吉布斯自由能变化的计算和分析,得出以下几点结论:
1)在Nd-Fe-B合金体系熔炼及冷却过程中,生成Nd2Fe14B相的相变反应是可以自发进行的,这是制备Nd-Fe-B永磁体的先决条件;
2)Nd2Fe14B相的生成比 Fe2B容易,但比NdB4和Nd2FeB3的生成难,因此,在Nd-Fe-B合金体系熔炼及冷却过程中,要尽量避开生成NdB4和Nd2FeB3化合物的温度点;
3)元素Nd、Fe和B都是容易被氧化的元素,它们氧化物的生成反应比Nd2Fe14B相的相变反应更容易,因此,在Nd-Fe-B磁体制备过程中,要尽量降低合金中的氧含量。
[1] 张修海,熊惟皓,李燕芳,等.烧结Nd-Fe-B永磁材料的研究进展[J].机械工程材料,2008,11:5-9
[2] 罗阳.全球NdFeB磁体产业的变化与发展[J].电气技术,2008(6):5-11
[3] F Viala,F Jolya,E Nevalainen,et al.Improvement of coercivity of sintered NdFeB permanent magnets by heat treatment[J].Journal of Magnetism and Magnetic Materials,2002,242-245: 1329-1334
[4] 李正,何叶青,胡伯平,等.烧结Nd-Fe-B中的热力学影响[J].物理学报,2005,54(11): 5400-5405
[5] 周寿增.超强永磁体——稀土铁系永磁材料[M].北京:冶金工业出版社,2004
[6] 梁连科,杨怀,李宪文,等.冶金热力学及动力学[M].沈阳:东北工学院出版社,1990
[7] 叶大伦.实用无机物热力学数据手册[M].北京:冶金工业出版社,2002
