毛细管电泳法同时测定盐酸萘甲唑林滴鼻液中有机汞抑菌剂硫柳汞及其活性成分
2011-01-29张福成空军总医院药学部北京004河北医科大学药学院石家庄05007
徐 荣,李 岑,张福成,蒋 晔#(.空军总医院药学部,北京 004;.河北医科大学药学院,石家庄 05007)
用于硫柳汞的分析方法主要有化学滴定法[1]、原子吸收光谱法[2,3]、比色法[4]及高效液相色谱法[5,6]等。采用化学滴定法、比色法分析硫柳汞的专属性差且灵敏度较低;原子吸收法则需要在分析前对硫柳汞进行消解,操作复杂;高效液相色谱法分析硫柳汞是较为理想的方法,其具有灵敏度高,专属性强等优点。但是其无法与带有相反电荷的盐酸萘甲唑林同时检测,且分析时间较长。目前,同时对滴鼻液中盐酸萘甲唑林及硫柳汞进行检测的研究未见报道。本文采用毛细管区带电泳法同时分析测定了盐酸萘甲唑林滴鼻液中的硫柳汞及带有相反电荷的盐酸萘甲唑林,现报道如下。
1 仪器与材料
仪器:高效毛细管电泳仪(北京彩陆科学仪器有限公司)、高压电源(北京彩陆科学仪器有限公司)、紫外检测器(北京彩陆科学仪器有限公司)、未涂层石英毛细管(50 μm i.d.×46 cm,有效长度37 cm,河北永年光导纤维厂)。药品和试剂:盐酸萘甲唑林对照品(批号:100111-200103)由中国药品生物制品检定所提供;硫柳汞为原料药,纯度 >99.5%;盐酸萘甲唑林滴鼻液由天津金虹胜利药业有限公司生产(批号:100201、100202、100401);水为重蒸水;其他试剂均为分析纯。
2 方法
2.1 电泳条件
运行缓冲溶液为20 mmol·L-1磷酸(pH=6.5);运行电压20 kV;检测波长240 nm;高度差进样(20 cm),进样时间10 s;温度25℃。每次开机后毛细管柱用0.1 mol·L-1的氢氧化钠溶液冲洗10 min,水冲洗10 min,运行缓冲液冲洗10 min,每次进样前用0.1 mol·L-1氢氧化钠溶液、水和运行缓冲液分别冲洗3 min。所有溶液在使用前均用 0.45 μm的纤维树脂膜滤过。
2.2 溶液配制
对照品溶液的配制:精密称取盐酸萘甲唑林对照品约80 mg,硫柳汞对照品约20 mg,分别置于10 mL量瓶中,用甲醇使其溶解并稀释至刻度,摇匀,分别制成8.14 mg·mL-1和1.96 mg·mL-1的溶液作为对照品储备液。供试品溶液:盐酸萘甲唑林滴鼻液制剂可作为供试品溶液直接进样进行分析,不需任何处理。
2.3 系统适用性实验
在“2.2”项电泳条件下,空白辅料、混合对照品和供试品溶液色谱图见图1。由图可知,辅料中其他成分对盐酸萘甲唑林和硫柳汞检测无干扰,且待测组分离度良好。
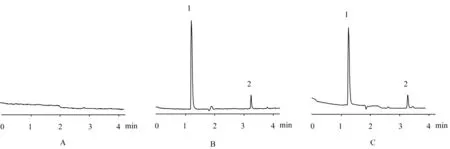
图1 空白辅料、混合对照品及供试品的电泳图Fig 1 Electropherograms of blank excipients,mixed reference substance and sample
2.4 线性关系
分别精密量取盐酸萘甲唑林和硫柳汞对照品储备液5 mL和0.5 mL置10 mL量瓶中,加水稀释至刻度,摇匀,制成1号混合对照品溶液;再从1号工作液中量取5 mL置10 mL量瓶中,加水稀释至刻度,摇匀,得2号工作液,依此法对倍稀释得3、4、5号系列标准溶液。按“2.2”项下电泳条件进样,记录色谱峰面积,以对照品的峰面积A对浓度C进行线性回归,盐酸萘甲唑林和硫柳汞的回归方程分别为A=2.70×105C-9.80×102和 A=1.44×102C+29.5。结果表明:盐酸萘甲唑林和硫柳汞分别在 0.122~3.87 mg·mL-1和 6.15~196 μg·mL-1的浓度范围内线性关系良好,r2分别为 0.9997和0.9993。盐酸萘甲唑林和硫柳汞的检测限分别为7 μg·mL-1和 2 μg·mL-1;定量限分别为24.0 μg·mL-1和6.15 μg·mL-1。
2.5 加样回收率
精密量取3份已知含量的样品,分别精密加入高、中、低3个浓度的对照品溶液,加水稀释至刻度。照“2.2”项下的方法操作,3个浓度的回收率结果见表1。
2.6 重现性、精密度及稳定性试验
取供试品溶液(批号:100202),连续进样5次,依法测定峰面积。结果盐酸萘甲唑林和硫柳汞的RSD分别为2.1%和2.6%。精密称取同一批样品(批号:100202)6份,按“2.2”项下条件测定,结果盐酸萘甲唑林和硫柳汞的RSD分别为1.5%和2.0%。取同一批供试品溶液(批号:100202),在室温下放置,分别于 0、1、2、4、6、8 h时测定含量。结果样品含量均无明显变化,盐酸萘甲唑林和硫柳汞峰面积的RSD分别为1.6%和2.1%。

表1 回收率实验结果(n=3)Tab 1 Results of recovery test(n=3)
2.7 样品含量测定
取3批供试品溶液,按2.2项下电泳条件进样,计算盐酸萘甲唑林和硫柳汞的含量,结果见表2。
3 讨论
盐酸萘甲唑林滴鼻液是一种用于过敏性及炎症性鼻充血、急慢性鼻炎的临床常用药物,其有效成分为盐酸萘甲唑林(naphazoline hydrochloride),其检测已有较多报道[7-9]。为了保证制剂多次使用后的安全性和稳定性,制剂处方中含有少量硫柳汞(thimerosal)作为防腐剂。硫柳汞是一种含乙基汞的有机汞化合物,虽然长期以来一直被广泛用做生物制品及药物制剂包括许多疫苗的防腐剂,但由于有机汞的毒性问题越来越受到人们的关注,且硫柳汞在光照及其他条件下有可能降解或不稳定[7],浓度不足也会影响到其抑菌性能,因此,为了更好的控制滴鼻液的质量,对药用制剂中硫柳汞含量进行检测及控制是非常必要的。在实验条件下,盐酸萘甲唑林和硫柳汞分别在电渗流前后出峰,达到很好的分离,且在240 nm的检测波长下,检测灵敏度适于2种物质的同时检测。该方法方便、快速,全部分析过程在5 min内完成,并且具有专属性强、低消耗、环境友好等优势,是一种可应用于盐酸萘甲唑林滴鼻液质量控制及抑菌剂限量的新方法。

表2 盐酸萘甲唑林滴鼻液中盐酸萘甲唑林及硫柳汞含量测定结果(n=3)Tab 2 Determination results of contents of naphazoline hydrochloride and thimerosal in Naphazoline Hydrochloride nasal drops(n=3)
3.1 缓冲盐pH的影响
考察了磷酸盐缓冲体系 pH 值分别为 5.5、6、6.5、7、7.5、8时盐酸萘甲唑林和硫柳汞的分离情况以及检测的灵敏度等参数。实验发现,当pH值为5.5时,硫柳汞的响应值相对较低,峰形也较差,这可能跟硫柳汞在酸性环境下不稳定有关。随着pH值增加,响应值增加,同时电渗流的迁移速度加快,2种物质分别在电渗流前后出峰。但 pH值越大,电流越大,产生的焦耳热增多,噪音增大。实验选择pH值为6.5,此时缓冲液具有较好的缓冲能力,2种物质的分离度和迁移时间都比较适宜,且电流大小适当。
3.2 缓冲盐浓度的影响
实验考察了缓冲溶液 pH=6.5时,不同浓度的磷酸二氢钠(10、20、30 mmol·L-1)对分离和检测能力的影响。结果表明,随着缓冲盐浓度增加,电渗流迁移速度加快,样品的迁移时间逐渐缩短,且增加缓冲盐的浓度,电流过大,基线不稳,不利于分离测定。综合考虑,选择20 mmol·L-1为缓冲盐的最佳浓度。
3.3 运行电压的考察
考察了电压为10~25 kV时对分离效果的影响。实验表明,随着电压的增加,出峰时间缩短,峰形尖锐,20 kV时分离最佳,峰形较好。当电压大于20 kV时,基线不稳,分离度下降。因此选择最佳运行电压为20 kV。
3.4 检测波长的选择
由于制剂处方中作为防腐剂的硫柳汞含量较低,其含量相对主成份盐酸萘甲唑林来说,相差1个数量级,因此本实验未采用盐酸萘甲唑林的最大吸收波长作为检测波长,而选择了240 nm进行检测,该波长为硫柳汞的最大吸收波长,提高了低浓度的硫柳汞检测的灵敏度同时也满足了检测盐酸萘甲唑林的灵敏度要求。
3.5 关于硫柳汞的使用安全
硫柳汞作为防腐剂的应用已具有60多年的历史。但其毒性作用目前还在争论之中。硫柳汞化学结构中含有乙基汞(其化学结构为乙基汞硫水杨酸钠),长期以来一直被广泛用做生物制品及药物制剂包括许多疫苗的防腐剂,虽然1930年上市时的数据表明低剂量的硫柳汞在人体及动物实验上并无明显伤害,但随着1950年日本水俣地区有机汞中毒事件的发生,有机汞的毒性问题受到人们的关注,特别是1970年,伊拉克发生了因含有机汞杀虫剂污染稻米而造成数千人死亡事件,有机汞化合物的使用和污染问题成为关注的课题。硫柳汞在一定条件下可降解,不仅降低其抑菌性能,同时降解产物也会对人体安全带来危害。世界卫生组织(WHO)、美国儿科协会(AAP)、美国公共卫生署(PHS)等机构已启动减少和消除疫苗中使用硫柳汞的计划,由此可见关于硫柳汞的使用安全越来越受到重视,对于制剂中硫柳汞的使用及含量控制也有待于进一步研究。
[1] 中国生物制品标准化委员会.中国生物制品化学检定规程[M].北京:化学工业出版社,2000.
[2] 金于兰,陈哲文,马福容,等.冷原子吸收法检测硫柳汞含量[J].中国生物制品学杂志,2005,18(5):422.
[3] Collado MS,MantovaniE,Goicoechea HC,etal.Simultaneousspectrophotometric-multivariate calibration determination of several components of ophthalmic solutions:phenylephrine, chloramphenicol, antipyrine,methylparaben and thimerosal[J].Talanta,2000,52(5):909.
[4] 全爱顺,辛暨华.比色法测定硫柳汞含量的试验考察[J].中国生物制品学杂志,1998,11(3):172.
[5] Chen Y,Pietrzyk RA,WhitsonPA.Quantificationof urinary uric acid in the presence of thymol and thimerosal by high-performance liquid chromatography[J].J Chromatogr A,1997,763(1-2):187.
[6] 汪海峰,鞠兴荣,黄凯云.高效液相色谱法测定疫苗中硫柳汞[J].理化检验化学分册,2005,41(10):743.
[7] 国家药典委员会.中华人民共和国药典(二部)[S].2010年版.北京:中国医药科技出版社,2010.
[8] 李国成,刘春霞,余晓霞,等.HPLC测定鼻炎灵滴鼻液中盐酸萘甲唑林和马来酸氯苯那敏含量的方法研究[J].国际医药卫生导报,2010,16(2):192.
[9] 胡浩咏.UV法与HPLC法测定盐酸萘甲唑林滴鼻液中盐酸萘甲唑林含量的比较[J].广东药学,2004,14(3):16.
