加压条件下稀硝酸吸收氮氧化物的实验研究
2011-01-28景香顺李玉平冒翠娥迟正平孟庆海田景彩张玉桂苏元元
景香顺,李玉平,冒翠娥,郑 楠,迟正平,孟庆海,姜 鑫,田景彩,张玉桂,苏元元
(1.北京理工大学化工与环境学院,北京100081;2.北京中兵北方环境科技发展有限责任公司,北京100070)
引 言
氮氧化物(NOx)已经成为中国当前主要的大气污染物之一,如果不及时加以控制,势必会对人体健康和生态环境造成巨大的威胁,因此,开展对NOx废气的治理已经迫在眉睫。废气脱硝是当前治理NOx最重要的方法,废气脱硝技术有干法和湿法两大类[1]。湿法脱硝技术具有工艺设备简单、操作温度低、耗能少、处理费用低等优点,适合火炸药和其他工业生产过程中产生的高浓度NOx废气的处理。硝酸吸收法由于能够副产硝酸,具有一定的经济效益,已成为被广泛研究和应用的NOx湿法处理技术。但是,常规硝酸吸收法的吸收效率较低,通过增大吸收压强可显著提高NOx的吸收效率[2]。陈曦等人[3]研究了加压条件下水吸收NOx的规律,得到的吸收液为浓度极低的硝酸,既不适合回收又不能直接排放,还会带来二次污染。本实验研究了加压条件下硝酸吸收NOx的规律,得到的吸收液为一定浓度的硝酸,可以回收利用,具有一定的实用价值。
1 实 验
1.1 实验装置
实验装置和实验步骤参见文献[3]。与文献介绍不同的是在其原有装置的基础上,利用在吸收柱外表面上缠绕的电加热带、温度传感器和数显式温度调节仪来实现温度的定量控制。同时吸收液由水变为一定浓度的稀硝酸。
1.2 NOx 浓度的检测
本研究使用的NOx模拟废气浓度较高(2 000~20 000mg/m3),采用中和滴定法测定。一定量的NOx在封闭容器(采用注射器)中被过量的H2O2和NaOH 的混合溶液吸收,NOx全部被H2O2氧化为HNO3,HNO3再与NaOH 反应生成NaNO3,用盐酸标准溶液滴定剩余的NaOH,根据盐酸消耗量求得NOx的浓度。
2 结果与讨论
用质量分数分别为35.4%、41%、45.3%和51.2%的硝酸作吸收剂,在压强分别为0.4、0.6和0.8MPa 下,NOx进 口 浓 度(C)在2 000 ~20 000mg/m3进行吸收试验,结果见图1。
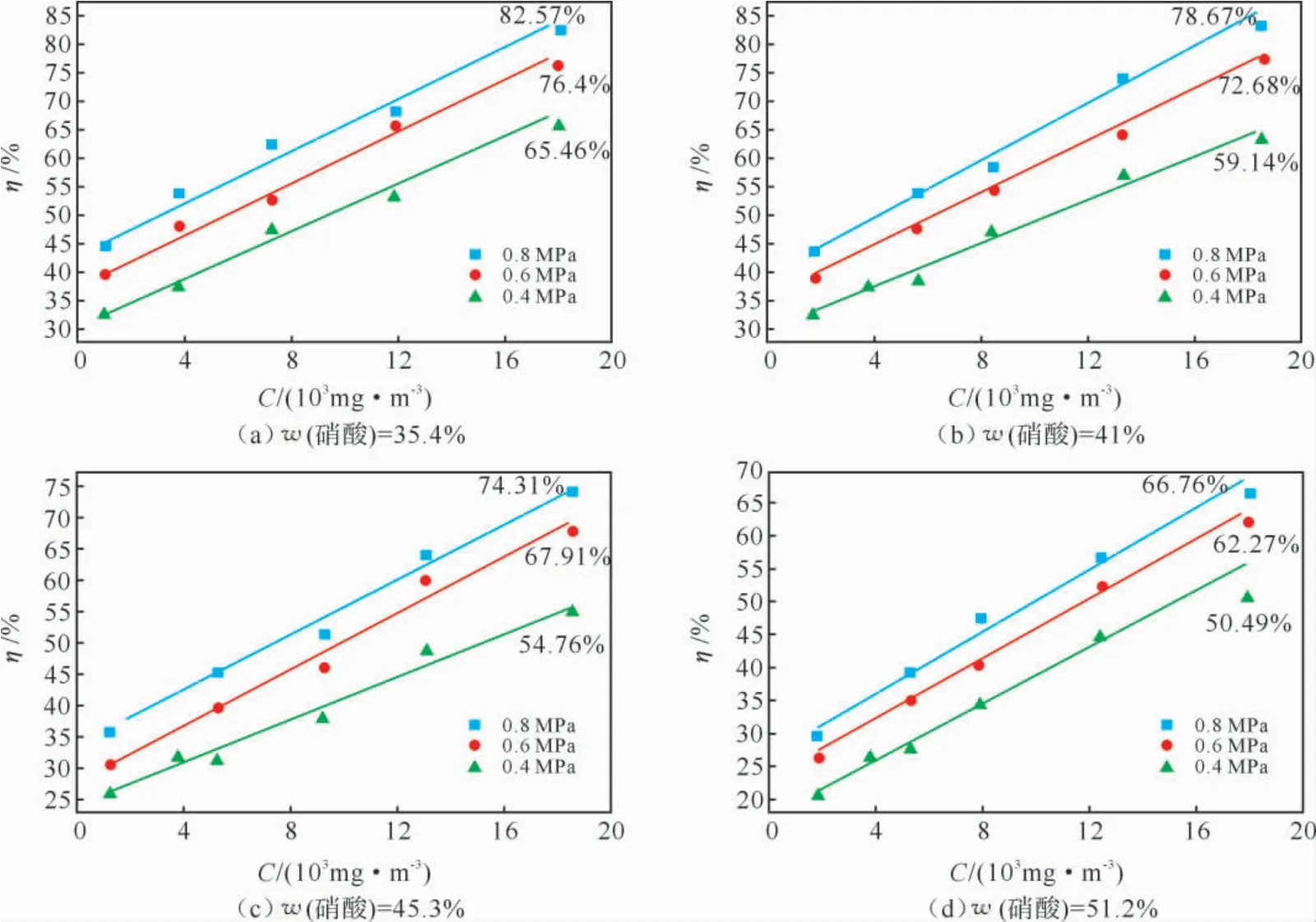
图1 进口浓度对吸收效率的影响Fig.1 Effect of inlet gas concentration on NOxabsorption efficiency
2.1 进口NOx浓度对吸收效率的影响
由图1可知,吸收柱进口处气体中NOx的浓度对吸收效率(η)的影响很大,在同一硝酸浓度和同一压强条件下,吸收效率随着进口NOx浓度的增大而提高。
硝酸吸收NOx的过程比较复杂,主要发生以下反应:

综合反应(2)、(3)和(4)可得总方程式:

用膜理论分析本填料塔中NOx的吸收过程:NOx的气相进口浓度越高,填料塔内NOx的平均气相浓度就越高,使得吸收过程的传质推动力增大,传质速率也增大,因而吸收效率提高。
由式(1)~(5)可知,在NOx的吸收过程中主要是NO2被吸收,而其中的NO 很难被吸收,且在NO2的吸收过程中还会放出NO。要想提高NOx的吸收效率,必须将NO 氧化为NO2,提高NO 的氧化反应,即反应(1)的反应速率。文献[4]表明,NO 浓度较低时NO 的氧化是整个吸收过程的速度控制步骤。此反应为不可逆的三级反应[5],因此,其化学反应速率主要决定于反应物的浓度,反应物浓度越大,化学反应速率越快(这个现象可用碰撞理论[6]来解释)。因此,提高NOx的进口浓度可以提高NO 的平均气相浓度,进而提高反应(1)的速率,加快NOx的吸收
2.2 压强对吸收效率的影响
压强对NOx吸收效率的影响非常明显。从图1可以看出,在硝酸质量分数和NOx进口浓度相同的条件下,吸收效率随着压强的升高而提高。这是因为在相同条件下,随着压强的升高,NOx的浓度升高,同时提高了气液传质速率和NO 的氧化速率,进而提高吸收效率。同时,压强的升高可延长吸收和反应时间。随着系统压强的升高,气体摩尔体积减小,当以常压计量的气体体积流量一定时,NOx废气在吸收塔内的停留时间增加。在一定的反应速率和吸收速率条件下,停留时间增加,NOx的吸收量也增加,吸收效率提高。
综上所述,压强的升高可提高NOx的吸收效率,但同时也会导致系统的动力消耗增加,运行费用升高。综合考虑动力消耗和尾气排放指标,吸收压强定为0.6MPa。
2.3 硝酸浓度对吸收效率的影响
本实验研究了硝酸质量分数(35%~50%)对吸收效率的影响,结果见图2。从图2可以看出,当硝酸的质量分数为35%~50%时,吸收效率随着硝酸浓度的增大而逐渐下降。
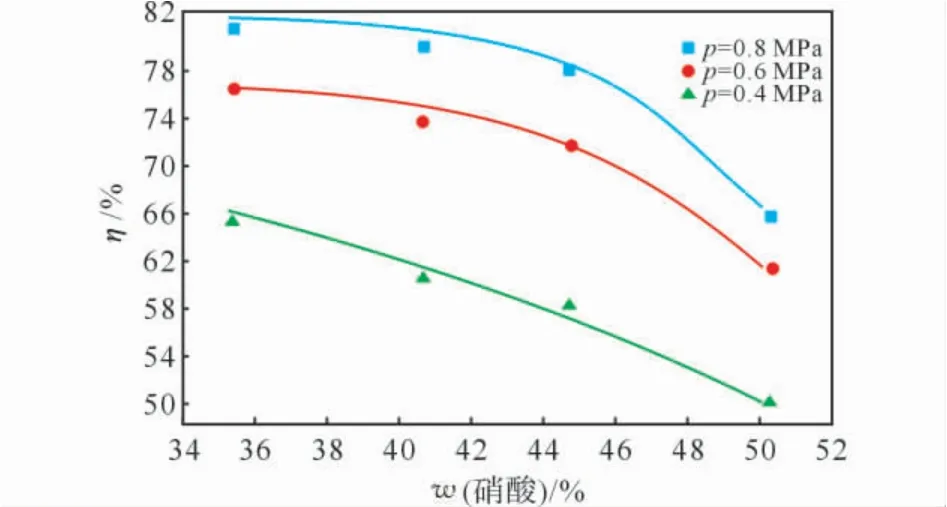
图2 硝酸质量分数对吸收效率的影响Fig.2 Effect of mass ratio of nitric acid on NOx removal
硝酸作为NO2吸收反应的生成物,其质量分数增大不利于NO2的吸收;但作为释放NO 的亚硝酸分解反应的生成物,硝酸质量分数的增大则会抑制亚硝酸的分解,从而有利于NO 的吸收。因此,吸收液中硝酸的质量分数对NOx吸收效率有正反两方面的影响。当硝酸质量分数为35%~50%时,NO2的吸收对吸收效率起主要作用。
在实际工业应用中,可以通过多塔串联、由后向前逐级提高硝酸浓度的方法,在保证NOx去除效率的前提下硝酸回收浓度达50%。
2.4 液气比对吸收效率的影响
在NOx进口浓度约为10 000mg/m3、压强为0.6M Pa、硝酸质量分数为47.3%的条件下研究了液气比对吸收效率的影响,结果见图3。液体流量稳定在18L/h 时,依次将气体流量定为6、4、3、2m3/h,即液气比分别为3、4.5、6、9L/m3;气体流量稳定在3m3/h时,依次将液体流量定为9、12、18、21、27L/h,即液气比分别为3、4、6、7、9L/m3。从图3可以看出,不论以何种方式改变液气比,NOx的吸收效率均随液气比的增大而逐渐提高。在液气比小于6L/m3时,吸收效率的增幅较大,但是液气比大于6L/m3后,吸收效率的增幅则趋于平缓。
液气比增加,即液体流量相对增大,液相湍流程度随之增大,使得气、液界面附近的液膜厚度减小,提高了NOx吸收的液相传质分系数,从而提高NOx的传质速率;同时,液体流量增大,吸收同样量的吸收质引起的液相浓度增幅减小[7],使吸收过程中液相主体浓度降低,传质推动力加大,吸收速率增大。

图3 液气比对吸收效率的影响Fig.3 Effect of liquid-gas ratio on NOxremoval
当液气比增加时,液体流量相对增大,液体喷淋密度也增加,可使填料获得良好的湿润,提高其表面利用率,从而提高NOx的吸收效率。但是,当液气比增大到一定程度以后,填料表面已被液体充分浸湿,再增大液气比对于吸收面积的影响不再明显,因而吸收效率的增幅开始变得缓慢。
从经济上考虑,采用较小的液气比,液体输送的动力消耗降低,吸收系统的操作费用下降;但液气比减小,塔内的传质推动力也随之减小,给定填料层内的吸收效率降低,要达到要求的NOx去除效率就需要较高的填料层,使吸收系统的设备费用增加。因此,液气比定为6L/m3。
2.5 温度对吸收效果的影响
在NOx进口浓度为10 000mg/m3、系统压强0.6MPa、硝酸质量分数为47.3%、气液流量分别为3m3/h和18L/h的条件下,依次将温度设定在20、25、30、35、40、45、50℃进行NOx吸收试验,结果见图4。由图4可知,吸收效率随温度的升高而下降。

图4 温度对吸收效率的影响Fig.4 Effect of temperature on NOx removal
NOx的吸收包含两个主要过程:NOx的物理溶解过程、NO 的气相氧化和HNO2的液相氧化等化学反应过程。温度对这两个过程均有不同程度的影响。物理溶解过程会释放出溶解热,使系统温度升高;气体在液相中的溶解度随着温度的升高而减小,因此温度升高不利于NOx吸收;从化学反应速率理论分析[8],NO 氧化的速率常数随温度的变化具有与一般反应不同的特点,其活化能为负值。此反应在273~600K 的阿伦尼乌斯方程如式(6):即温度升高,速率下降。此外,从化学反应平衡角度分析,NO 的氧化反应是放热反应,反应后的气体温度比反应前高[9],提高温度有利于放热反应平衡向逆反应方向进行,即不利于NO 转化为易溶于水的NO2,导致吸收效率下降。
综上可知,无论是物理溶解还是化学反应,系统温度均会随着吸收的进行而提高,引起吸收效率下降。因此在实际应用中,必要时要采取措施对吸收系统进行降温。
3 结 论
(1)用质量分数35.4%、41%、45.3%和51.2%的硝酸作吸收剂,在表压强分别为0.4、0.6和0.8MPa条件下,NOx浓度在2 000~20 000mg/m3范围内,吸收效率随着进气浓度的增大而提高。
(2)升高压强、增大液气比有利于提高NOx的吸收效率;系统温度升高,吸收效率下降。综合考虑设备费用及运行费用,建议将压强控制在0.6MPa,液气比定为6L/m3,必要时需要采取降温措施。
[1]李晓东,扬卓如.国外氮氧化物气体治理的研究进展[J].环境工程,1996,14(2):34-38.
LI Xiao-dong,YANG Zhuo-ru.Research progress of controlling and eliminating nitric oxide air pollution from abroad[J].Environmental Engineering,1996,14(2):34-38.
[2]祝天熙.硝酸尾气治理方法探讨[J].山西化工,1997,3:8-10.
ZHU Tian-xi.Explore the controlling methods of nitric acid tail gas[J].Shanxi Chemical Industry,1997,3:8-10.
[3]陈曦,李玉平,韩婕,等.加压条件下氮氧化物的水吸收研究[J].火炸药学报,2009,32(4):84-87.
CHEN Xi,LI Yu-ping,HAN Jie,et al.Study of pressurized absorption of nitrogen oxides in water[J].Chinese Journal of Explosives and Propellants,2009,32(4):84-87.
[4]Hüpen B,Kenig E Y.Rigorous modelling of NOx absorption in tray and packed columns[J].Chemical Engineering Science,2005,60(22):6462-6471.
[6]Paiva J L de,Kachan G C.Absorption of nitrogen oxides in aqueous solutions in a structured packing pilot column[J].Chemical Engineering and Processing,2004,43(7):941-948.
[7]傅献彩,沈文霞,姚天扬,等.物理化学[M].北京:高等教育出版社,2006:225-228.
[8]孙志勇,李增生,崔乔云.用硝酸吸收法脱除氮氧化物的实 验 研 究[J].科 学 技 术 与 工 程,2009,9(19):5928-5931.
SUN Zhi-yong,LI Zeng-sheng,CUI Qiao-yun.Study on removing of nitrogen oxides by nitric acid absorption[J].Science Technology and Engineering,2009,9(19):5928-5931.
[9]Yu J Y,Zhang X M,Han L G,et al.NOx Absorption in full scale plant columns with structured packings[J].Chinese Journal of Chemical Engineering,2005,13(5):713-716.
