拉米夫定耐药患者乙型肝炎病毒多聚酶区变异分析及恩替卡韦治疗观察*
2011-01-23高得勇刘亮明王迎迎徐国荣汪妍妍俞小燕
高得勇 刘亮明 王迎迎 徐国荣 汪妍妍 俞小燕
(上海交通大学附属第一人民医院松江分院感染科,上海 201600)
我国有慢性乙型肝炎(慢乙肝)患者约3000万人,预测15%~40%最终发展为肝硬化、肝衰竭或肝细胞癌。研究[1]表明HBV DNA持续高水平是乙肝疾病进展的主要根源。 抗病毒治疗可延缓疾病发展己成为共识,拉米夫定(LAM)在抑制病毒、控制病情、改善预后等方面效果明确,研究[2]发现,慢性乙型肝炎患者长期应用拉米夫定治疗可引起HBV P区基因出现变异,拉米夫定耐药后可引起肝病进展,甚至肝衰竭[3],因此已成为治疗的严重问题。本研究对LAM耐药变异的慢性乙型肝炎患者HBV P区基因逆转录酶区(RT区)进行测序和病情进展情况分析,研究了换用恩替卡韦(ETV)治疗LAM耐药患者的疗效和安全性,以寻求对LAM耐药患者更理想的治疗方法。
1 材料和方法
1.1病例选择 2008年7月至2010年12月在上海市第一人民医院松江分院感染科门诊或住院治疗的慢性乙型肝炎患者,符合2000年全国病毒性肝炎会议修订的慢性乙型肝炎诊断标准[4]。入选标准:拉米夫定耐药组45例,应用恩替卡韦1 mg/d治疗:(1)口服LAM,100 mg/d,疗程48周以上。(2)应用LAM治疗后曾出现HBV DNA阴转或HBV DNA下降大于2 log copies/ml,但在继续治疗过程中HBV DNA升高大于1 log copies/ml,或HBV DNA反跳至1×103copies/ml以上。(3)伴有或不伴有丙氨酸转氨酶(ALT)升高,其中HBeAg阳性者为30例。应用恩替卡韦治疗的慢性乙型肝炎患者对照组30例,接受恩替卡韦治疗,每天0.5 mg顿服,其中HBeAg阳性者为20例。
1.2血清HBV DNA P基因RT区序列分析检测 HBV DNA抽提采用Qiagen公司试剂盒,操作按说明书。纯化后的PCR产物在ABI3730型自动荧光测序仪上进行测序;采用Chromas 2.0软件对HBV DNA P基因片段核苷酸编码的氨基酸差异和变异类型进行分析。
1.3本研究治疗前检测肝功能、乙肝病毒标志物(ELISA法)和HBV DNA(荧光定量PCR法)等作为基线值,治疗12周、24周、36周、48周复查肝功能、检测乙肝病毒标志物和HBV DNA,同时观察临床症状及体征。
1.4HBV血清标志物及肝功能检测 HBV血清标志物采用酶标法检测,由上海罗氏有限公司提供试剂;血清总胆红素、总蛋白、白蛋白、丙氨酸转氨酶采用日本奥林巴斯AU2700全自动生化仪测定。
1.5统计学分析 应用SPSS 13.0 统计软件处理数据,采用t检验和卡方检验。
2 结 果
2.1LAM耐药组HBV多聚酶 RT区变异分析 32例(32/45,71%)出现rtM204V/I变异(YMDD),rtL180M变异占23/45(51%),19例(42%)检测到rtL180M+rtM204V联合变异位点,rtV173L/M变异为3/45(7%),rtV173L变异为3/45(7%),1例(2%)检测到rtL180M+rtM204V+rtM204I联合变异。其中在发生YMDD变异的病例中,50%的伴有rtL180M变异。
2.2LAM耐药组HBV DNA、丙氨酸转氨酶(ALT)、总胆红素(TBil)的改变 96%的患者(43/45)出现HBV DNA的反弹,84%(28/45)患者HBV DNA反弹后峰值水平低于拉米夫定治疗前的水平;87%(39/45)患者的ALT升高,78%(35/45)患者的ALT升高的峰值低于拉米夫定治疗前水平;27%(12/45)患者出现轻度黄疸;TBil的平均水平为(37.2±2.76)μmol/L;所有患者临床表现均轻微。
2.3两组患者治疗后血清ALT复常率和HBV DNA转阴率比较 LAM耐药组和对照组治疗48周后血清ALT复常率分别为88.9%和90%;血清HBV DNA转阴率分别为88.9%和86.7%,两组相比较无统计学差异(P>0.05)。见表1,2。
2.4两组患者治疗后不同时段HBeAg/抗-HBe血清转换率比较 LAM耐药组和对照组患者治疗48周后HBeAg阳性的患者抗-HBe血清转换率分别为10%和25%,两组相比较有明显统计学差异(P<0.05,表3)。
2.5治疗过程中HBV DNA的变化 两组患者在48周治疗阶段HBV DNA(PCR法)中位数(log10copies/ml)变化见表4。LAM耐药组HBV DNA下降幅度达3.76个log10,对照组HBV DNA下降幅度达1.43个log10,LAM耐药组下降幅度较对照组小,两组相比较有明显的统计学差异(P<0.01)。

表1 两组患者治疗后血清ALT复常率的比较[n(%)]
注:与对照组相比较,P>0.05。

表2 两组患者治疗后血清HBV DNA转阴率比较[n(%)]
注:与对照组相比较,P>0.05。

表3 两组患者治疗后不同时段HBeAg/抗-HBe血清转换率比较[n(%)]
注:与对照组相比较,﹡P<0.05。
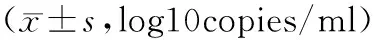
表4 治疗过程中HBV DNA的变化
3 讨 论
拉米夫定在治疗慢性乙型肝炎的过程中能有效抑制HBV DNA的复制,但长期应用易产生耐药[5]。本研究通过回顾性分析45例LAM耐药的慢性乙型肝炎病人的HBV P基因序列,发现LAM耐药相关变异以rtM204V/I(YMDD)变异为主(71%),联合变异以rtL180M+rtM204V为主,并在1例患者中检测到RT区3个位点的联合变异。因此,要全面地检测拉米夫定耐药突变株,除了HBV P基因区常见的rtL180、rtM204位点变异外,还应考虑其他位点的联合变异。HBV P基因区各个不同位点的联合变异,对HBV病毒复制能力和对病毒药敏感度的影响需要进一步的体外实验证实。
通常认为HBV并不具有直接的细胞毒作用,慢性乙型肝炎患者的炎症改变主要是由于病毒诱导的免疫反应所致[6]。本研究中大部分患者的ALT升高(78%,35/45),HBV DNA反弹后的峰值低于拉米夫定治疗前水平(84%,(28/45);提示HBV聚合酶基因突变并没有引起患者的病情加重。我们认为体内耐药株可能是原有的极少数变异株在野生株被明显抑制的条件下由弱势成为优势,因此并没有引起比拉米夫定治疗前更严重的炎症。LAM耐药后引起肝炎发作可能是由于病毒水平与患者免疫状态失衡所致[7-8],当突变病毒增多并达到一定的滴度时,有可能激活抗HBV细胞免疫反应,导致肝细胞坏死和临床肝炎的发生。
对于长期使用拉米夫定耐药者,应予以调整有效的抗病毒药物进行治疗。我国2005年慢性乙型肝炎防治指南[9]建议加用或改用其他已批准的能治疗耐药变异的核苷(酸)类似物。恩替卡韦是新一代的核苷类似物,经口服吸收后进入肝细胞,通过磷酸化作用成为二磷酸和三磷酸恩替卡韦,后者是恩替卡韦在肝细胞内抑制HBV DNA聚合酶的活性形式,三磷酸恩替卡韦的半衰期为14~15 h,作用较持久,与HBV多聚酶的天然底物三磷酸鸟嘌呤核苷竞争,对HBV的复制进行抑制[10],对于初治患者和拉米夫定治疗失效患者均具有显著的抗HBV作用[11]。本研究采用恩替卡韦(1 mg/d)治疗LAM耐药者[12],治疗48周的结果显示,患者的临床症状有明显改善;拉米夫定耐药治疗组患者ALT的复常率、HBV DNA达到检测水平以下的百分率分别为88.9%和90%,应用ETV初始治疗(对照组)的慢性乙型肝炎患者ALT的复常率、HBV DNA达到检测水平以下的百分率分别为88.9%和86.7%,两组相比较差异没有统计学意义,都取得了很好的疗效。对两组HBeAg抗原阳性的患者治疗后不同时段HBeAg/抗-HBe血清转换率进行比较,在两组病人治疗48周结束时,LAM治疗组有3/30(10%)发生了血清学转换,而对照组有5/20(25%)发生了血清学转换,两组比较有明显的统计学差异,提示恩替卡韦治疗LAM耐药伴HBeAg抗原阳性的慢性乙型肝炎患者的HBeAg/抗-HBe血清转换并不高。研究还发现,治疗过程中两组患者HBV DNA的变化情况不同,对照组在治疗过程中HBV DNA的下降幅度明显快于LAM耐药组,两组HBV DNA的变化相比较有明显的统计学意义,说明了恩替卡韦对于拉米夫定耐药的患者虽然抗病毒剂量加倍,但抑制拉米夫定耐药突变HBV复制的能力比抑制慢性乙型肝炎野毒株的速度和能力弱。在我们的研究中发现,应用恩替卡韦治疗LAM耐药患者的过程中,仍有5例病人不能完全清除HBV DNA和ALT没有恢复正常,推测这些患者在恩替卡韦治疗之前可能已经出现了恩替卡韦耐药相关性变异[13]。
本研究表明拉米夫定耐药的慢性乙型肝炎患者多聚酶区基因变异呈现多样性;应用恩替卡韦1 mg/d治疗后患者的血清病毒载量降低,肝功能生化指标改善,证实恩替卡韦治疗拉米夫定耐药的慢性乙型肝炎效果确切。但与恩替卡韦0.5 mg/d初始治疗慢性乙型肝炎患者相比,拉米夫定耐药的患者其血清HBeAg/抗-HBe血清转换及治疗过程中HBV DNA均值的变化幅度均较低。
[1] Chen CJ, Yang HI, Su J, et al. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level[J]. JAMA, 2006,295:65-73.
[2] Kumagai N, Kaneko F, Tsunematsu S, et al. Complexity of the HVR-1 quasispecies and disease activity in patients with hepatitis C[J]. Eur J Clin Invest, 2007,37:566-752.
[3] Peters MG, Hann HW, Martin P, et al. Adefovir dipivoxil done or in combination with camirudine in patients with lamivudine-resistant chrouic hepatitis B[J]. Gastroenterology, 2004,126(1):91-101.
[4] 中华医学会传染病与寄生虫病学分会、肝病学分会.病毒性肝炎防治方案[J]. 传染病信息,2000,13(4):141-150.
[5] Haché C, Villeneuve JP. Lamivudine treatment in patients with chronic hepatitis B and cirrhosis[J]. Expert Opin Pharmacother, 2006,7(13):1835-1843.
[6] Chisari FV,Ferrari C.Heptatitis B virus immumopathogenesis[J]. Annu Rev Imuumol, 1995,13:29-60.
[7] Kazim SN, Sarin SK, Sharma BC, et al. Characterization of naturally occurring and Lamivudine-induced surface gene mutants of hepatitis B virus in patients with chronic hepatitis B in India[J]. Intervirology, 2006,49(3):152-160.
[8] 陈立,张欣欣.核苷(酸)类似物耐药变异对乙型肝炎病毒生物学特征的影响[J].中国实用内科杂志,2007,27(15):1230-1232.
[9] 中华医学会肝病学分会、中华医学会感染病学分会.慢性乙型肝炎防治指南[J].中华肝脏病杂志,2005,13:881-891.
[10] Lok AS, McMahon BJ. Chronic hepatitis B[J].Hepatology,2007,45(2):507-539.
[11] Zoulim F. Entecavir: a new treatment option for chronic hepatitis B[J]. J Clin Virol, 2006,36(1):8-12.
[12] Gish RG, Lok AS, Chang TT, et al. Entecavir therapy for up to 96 weeks in patients with HBeAg-positive chronic hepatitis B[J]. Gastroenterology,2007,133(5):1437-1444.
[13] Tenney DJ, Levine SM, Rose RE, et al. Clinical emergence of entecavir-resistant hepatitis B virus requires additional substitutions in virus already resistant to Lamivudine[J]. Antimicrob Agents Chemother, 2004,48(9):3498-3507.
