2,3-吲哚醌在大鼠体内的药代动力学研究*
2011-01-23侯江涛张婷婷毛小红牟群芳张继国
侯江涛 张婷婷 毛小红 牟群芳 张继国 岳 旺
(1青岛大学,山东 青岛 266021;2泰山医学院,山东 泰安 271016)
2,3-吲哚醌(2,3-indolinedione),是一种存在于海洋和动物体内的内源性活性因子[1],具有抗癌[2],抗病毒[3],抗衰老等多种生物活性。但其体内来源及药物生化代谢尚未报道,本文考察单次静脉注射和口服给予大鼠2,3-吲哚醌后的药代动力学,为深入该药的新药研发提供依据。
1 实验材料与设备
1.1药品与试剂
2,3-吲哚醌对照品:上海新生源生物医药有限公司;
内标物奎硫平:美迪西普亚医药科技(上海)有限公司;
甲醇(Burdick & Jackson,HPLC grade);
甲酸(ACROS ORGANICS,HPLC grade);
水为超纯水。
1.2仪器设备
液相色谱仪(Agilent 1200),质谱仪(6410B,Agilent公司),电喷雾离子源(ESI),串联四极杆质量分析器。数据处理系统为MassHunter软件(Agilent公司)。涡旋振荡器(Vortex-Genie 2,Scientific Industries,Inc);小型台式高速冷冻离心机(5417R,Eppendorf); 微量分析天平(XP26,梅特勒-托利多仪器(上海)有限公司);超纯水机(Millipore)。色谱柱为Venusil XBP PH,5 μm,100×2.0 mm。
1.3实验动物
SD大鼠,购于上海西普尔-必凯实验动物有限公司,雄性,体重:200~330 g。动物饲养:实验动物按照动物房标准操作规程饲养。食物和水食物由上海斯莱克实验动物有限责任公司提供,动物除在特定给药期间,可以自由饮食及饮水。动物房环境温度20-25 ℃ ,相对湿度30%~70%,12小时光照。实验动物在实验前适应1~7天。实验动物必须健康并适应环境,口服给药前禁食10~14小时。给药后4小时后恢复饲料。
2 实验方法
2.1受试物配制
静脉给药溶液的配制:称取适量受试物,溶于5%二甲基亚砜, 40% PEG400 and 55%盐水中,得到浓度为2 mg/ml的澄清溶液,用于静脉注射给药。
口服给药溶液的配制:称取适量受试物,溶于1.25%西黄耆胶水溶液中,得到浓度为5 mg/ml的混悬液,用于口服给药。
2.2动物分组与给药
6只SD大鼠随机分为2组,每组3只。第一组:通过尾静脉注射给予动物受试物溶液,剂量为2 mg/kg体重;第二组: 通过口服灌胃给予动物受试物溶液,剂量为5 mg/kg体重。
2.3血液样本采集与预处理
经眼眶静脉(异氟烷麻醉后)或其他合适的静脉采大约0.25 ml血液,置于含K2EDTA的一次性真空采血管内。采集时间点为:给予受试物前(0hr)和给予受试物后 5 min,15 min,30 min,1 h,2 h,4 h,6 h,8 h和24 h。血液样本采集后置于冰上,并立即取出50 μl全血加入已混有内标(50 ng/ml 奎硫平)的250 ml甲醇溶液中涡旋1分钟后,离心分离上清液(离心条件:15000转/分钟,5分钟,2~8 ℃),收集的100 μl上清液分析前存放于-80 ℃。
2.4标准曲线和质控样品的配制
取适量2,3-吲哚醌储备液,用甲醇:水混合溶液(1∶1,v/v)逐级稀释,配制成浓度为100,40,20,4,2和1 μg/ml的标准溶液,取标准溶液各5 μl平行加入到195 μl 大鼠空白全血或空白尿液中,制得浓度为 2500,1000,500,100,50和25 ng/ml的标准曲线样品。
取适量2,3-吲哚醌储备液,用甲醇:水混合溶液(1∶1,v/v)逐级稀释,配制成浓度为100,80,和8 μg/ml的质控溶液,取质控溶液各5 μl平行加入到195 μl大鼠空白全血中,制得浓度为2000,200和40 ng/mL的质控样品。
2.5样本分析
采用液相色谱串联质谱联用对处理好的样品进行测定。测定条件如下:
色谱条件:
流动相:甲醇-5mM甲酸/氨水(65:35, v/v);
流速:0.3 ml/min;
柱温:35 ℃;
进样量:5 μl。
质谱条件
采用电喷雾离子化源(ESI),正离子模式,喷雾电压4500 V,雾化气为氮气,雾化压力为50 psi;去溶剂气为氮气,温度350 ℃,流速为9 L/min;采用多反应监测(MRM)模式对药物离子浓度进行测定,淫羊藿苷及内标的最优MRM参数见表1。

表1 待测药物及内标的MRM条件
3 实验结果
3.1分析方法
血液样品分析方法(LC/MS/MS)的开发和样品分析将在美迪西普亚医药科技(上海)有限公司分析部门完成。该分析方法符合国内外生物样品分析的有关规定[4-6]。
3.2药代动力学结果
Sprague Dawley大鼠静脉注射及口服给予2,3-吲哚醌后的血药浓度数据见表2和图1。
3.3药代动力学参数
通过不同时间点的血药浓度数据,运用WinNonlin 5.2计算药代动力学参数,结果见表3。
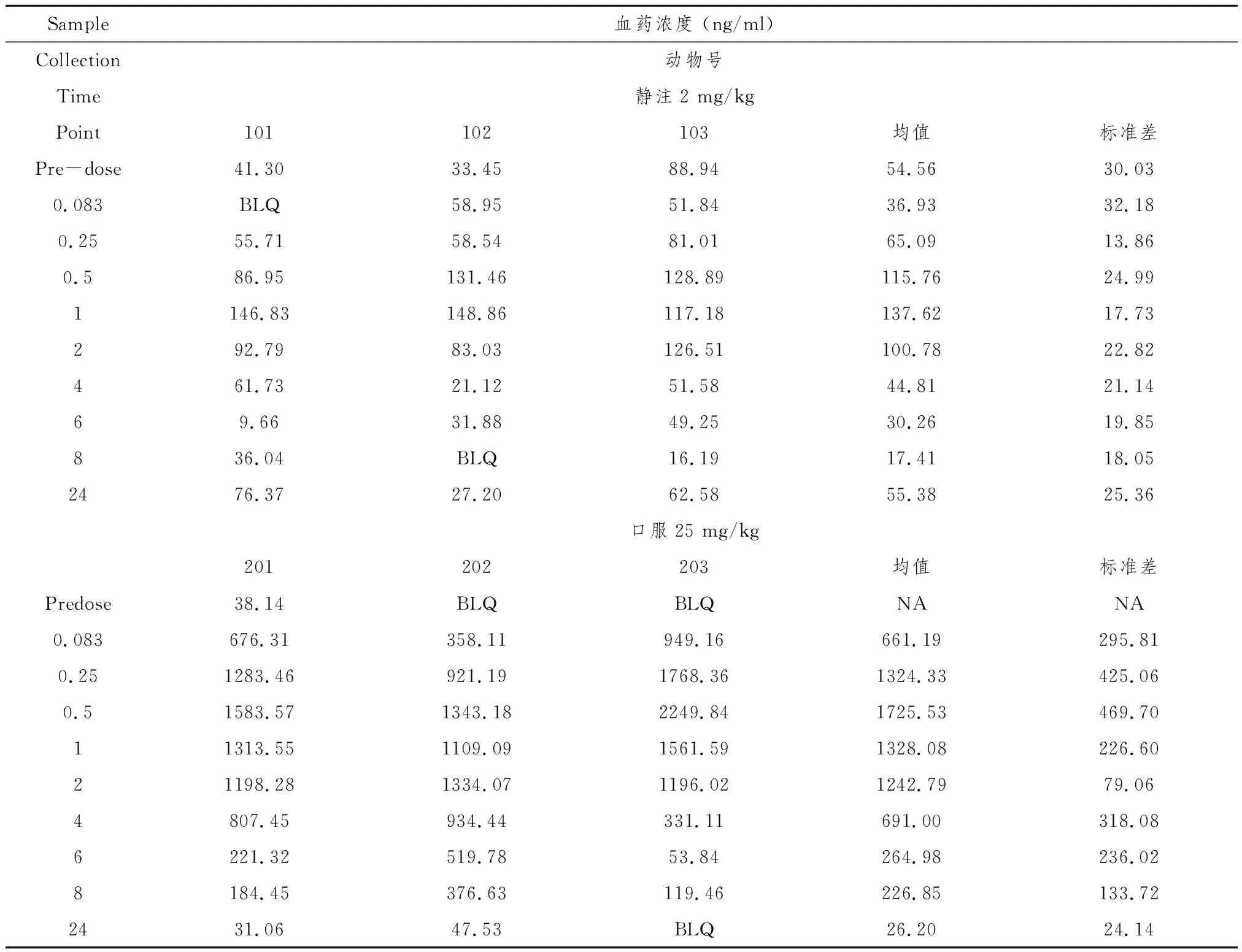
表2 雄性SD大鼠静注及口服给予2.3-吲哚醌后的血药浓度
BLQ:低于最低检测线,LLOQ=25 ng/ml
NA:不适用Not applicable
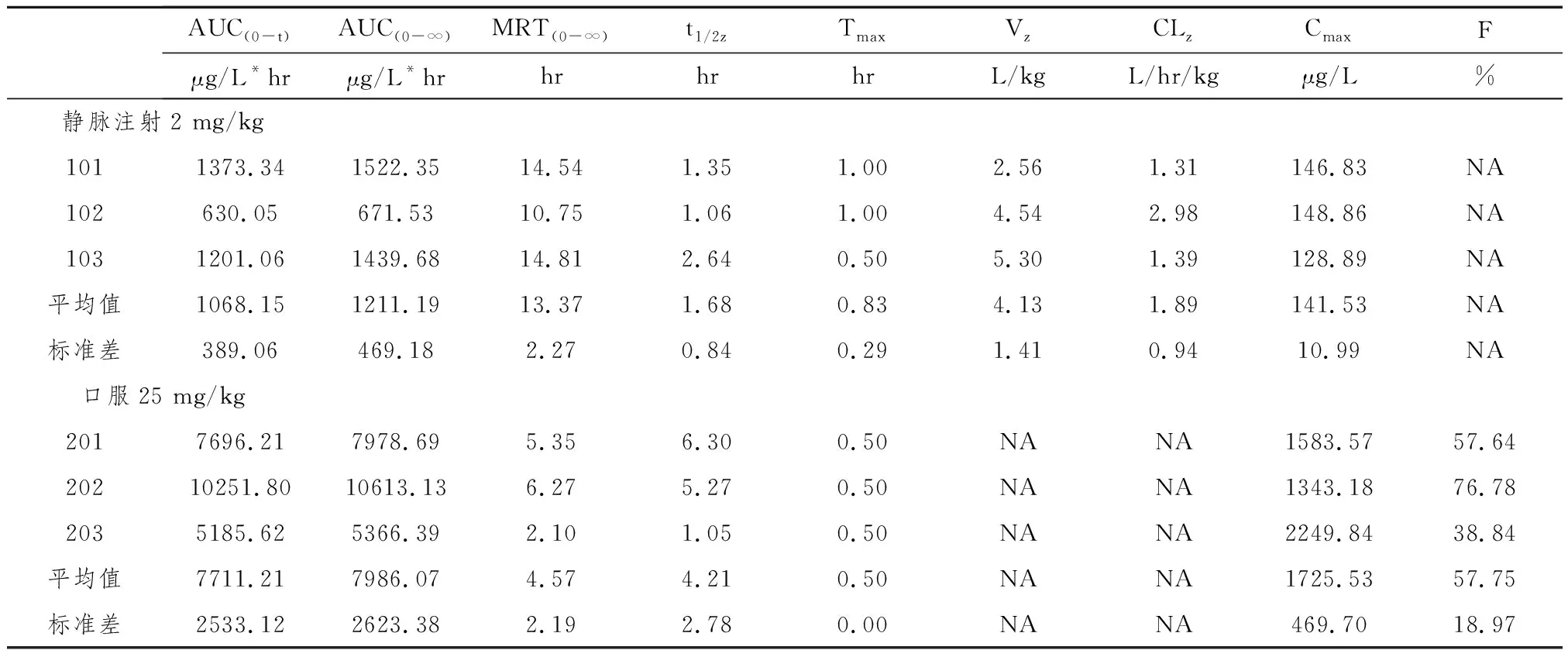
表3 雄性SD大鼠静脉及口服给予2.3-吲哚醌后的主要药动学参数
*:生物利用度以AUC(0-t)进行计算。

图1 雄性SD大鼠静脉及口服给予2.3-吲哚醌后的平均±标准差浓度-时间曲线(n=3)
3 讨 论
2,3-吲哚醌为内源性物质,本文从空白血液中可检测到一定量的2,3-吲哚醌(如图3),本方法所测得的浓度数据为内源性2,3-吲哚醌及给药后暴露于血液中的2,3-吲哚醌之和。
从静脉药时曲线可见,静脉的给予后血药浓度与内源性比较接近,可能是给药后2,3-吲哚醌迅速分布至组织所致,本药的表观分布容积较大也与之对应。且在采血末端时间点有反跳,可能是内源性2,3-吲哚醌的干扰。
初步研究表明,2,3-吲哚醌口服的生物利用度较高,为57.75%,提示口服给药可作为该药的首选给药方式,这对于该药物的临床应用具有重要价值,并为该内源性药物的研发提供了重要的药动学依据。
[1] Glover V, Halket JM, Watkins PJ, et al. Isatin: identity with the purified monoamine oxidase inhibitor tribulin. J Neurochem,1988,51:656
[2] 岳旺,王蕾,刘占涛,等.一种抗癌防癌海洋活性药物的制备方法.专利申请号:200410023871.1
[3] 岳旺,刘占涛,王蕾,等.吲哚-2,3-二酮在制备抗病毒或免疫增强剂药物中的应用.专利号:ZL10105691
[4] Shah VP, Midha KK, Findlay JW, et al. Bioanalytical method validation-A revisit with a decade of progress[J]. Pharm Res, 2000, 17: 1551-1557.
[5] Karnes HT, March C. Precision, accuracy and data acceptance criteria in biopharmaceutical analysis[J]. Pharm Res, 1993, 10: 1420-1422.
[6] 萧参, 陈坚行. 生物药剂分析方法的认证[J]. 中国药学杂志, 1993, 24: 425-426.
