IP方案联合沙利度胺二线治疗晚期小细胞肺癌的临床观察
2011-01-10王彩玲王俊生
王彩玲 王俊生
小细胞肺癌(small cell lung cancer,SCLC)的发病率近年呈逐年上升趋势,已经占到肺癌总数的20% ~30%,越来越多地威胁着人类的健康。虽然小细胞肺癌初次化疗可获很高的有效率,但是因其倍增时间快,增值比率高,易广泛转移,此外,本身或治疗后的获得性耐药,大多数患者会出现病情进展或复发转移,需要二线挽救方案治疗。近年来由于动物及体外和体内实验发现沙利度胺(反应停)具有抑制血管生成等作用而具有抗肿瘤的潜能,因此逐渐受到人们的重视。2005年6月~2O09年10月期间,我们应用沙利度胺联合伊立替康(CPT-11)、顺铂(DDP)方案二线治疗复发晚期小细胞肺癌43例,现总结报告如下。
1 资料与方法
1.1 一般资料
43例患者均为2005年6月~2O09年10月我科收治的晚期小细胞肺癌患者,男性29例,女性14例,年龄30~74岁,中位年龄58岁。所有患者均经气管镜活检、经皮肺穿活检或术后病理检查诊断证实,至少有1个病灶可测量。其中转移病灶分布:纵膈转移27例,锁骨上淋巴结转移21例,肝脏转移11例,双肺转移13例,骨转移9例,胸膜转移8例,皮下转移1例。43例均在应用顺铂和足叶乙苷一线化疗2个周期以上病变进展,其中31例应用EP方案后缓解期超过3个月后进展,12例为EP方案化疗中进展。所有患者1个月内未接受任何治疗,Karnofsky评分>60分,化疗前均常规进行血常规、肝肾功能及心电图等检查,达到可化疗指标,无化疗禁忌证,预计生存期>3个月。
1.2 治疗方法
伊立替康(CPT-1l,江苏恒瑞医药股份有限公司生产)60 mg/m2加入生理盐水静脉滴注,第1,8天;顺铂25 mg/m2第2~4天。每3周重复为1个周期。沙利度胺起始剂量100 mg/d,睡前1次服用,1周后渐加量至600 mg/d,若患者无不能耐受的副作用,维持600 mg/d口服。化疗止吐采用托烷司琼或格拉司琼;出现腹泻症状,则应用易蒙停治疗,化疗期间如发生Ⅲ~Ⅳ度骨髓抑制,立即给予造血细胞集落刺激因子。连续用药2个周期以上进行疗效评价。
1.3 疗效及毒性评价标准
对于近期客观疗效按WHO实体瘤疗效评定标准进行疗效评估,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和疾病进展(PD)。以CR+PR为有效率(RR)、以CR+PR+SD为疾病控制率(DCR)。不良反应评价标准按WHO抗癌药物不良反应分度标准评价分为0~Ⅳ度。
1.4 统计学处理
采用χ2检验。
2 结果
2.1 临床疗效
43例患者中有2例患者因严重腹泻仅接受1个周期治疗,不能评价疗效,其余41例均接受2个周期以上治疗,计158个周期,最多6个周期,平均3.85个周期。41例均可评价疗效,其中CR 2例,PR 18例,SD 14例,PD 7例,总有效率为48.78%(20/41),疾病控制率为82.93%(34/41)。中位疾病进展时间4.2个月,中位生存期为9.4个月(1.5~32.7个月)。其中采用EP方案一线化疗后中进展的12例患者中,有效率为16.67%(2/12),无1例达CR;而缓解期超过3个月的29例患者,疗效为62.07% (18/29),疗效有明显差异(P<0.05)。
2.2 不良反应
常见不良反应为迟发性腹泻、血液学毒性(主要为中性粒细胞减少和血小板减少)和消化道反应(恶心、呕吐),但多为Ⅰ~Ⅱ度,患者可耐受。全组无治疗相关死亡患者,见表1。
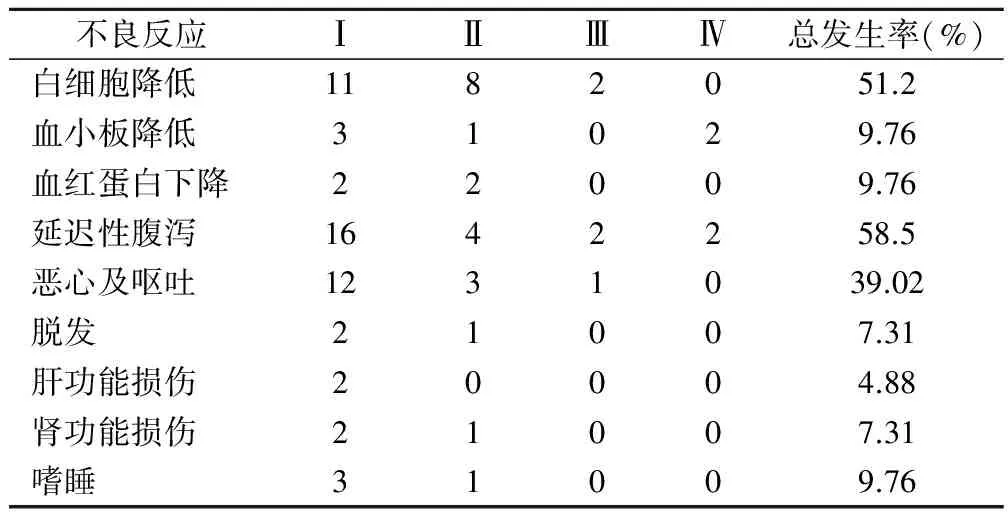
表1 联合化疗的主要不良反应(例)
2.3 安全性监测
用药后每月行心电图、血常规及肝肾功能监测,3例患者出现嗜睡,适当减量服用沙利度胺后好转,16例既往睡眠差,服用沙利度胺后睡眠改善,食欲增加。
3 讨论
小细胞肺癌具有独特的生物学行为,肿瘤细胞倍增时间短、生长比率高,较早发生全身转移[1]。目前治疗以全身化疗为主,初始化疗以EP或CE作为标准方案,近期缓解率达到60%~70%[2]。复发性小细胞肺癌的中位生存期4~5个月,目前二线治疗的目的主要是减轻症状和改善生存质量。CPT-11是1种半合成喜树碱的可溶性衍生物,主要作用在真核细胞DNA的拓扑异构酶工,阻碍DNA复制及转录,引起不可逆的DNA键断裂,最终导致细胞死亡。由于在增生和静止的肿瘤细胞中拓扑异构酶工含量均增高,故CPT-11对缓慢和迅速生长的肿瘤细胞均有杀伤作用[3]。国内外研究报道伊立替康治疗复发难治小细胞肺癌,缓解率为31%~68.2%[4]。国外Jagasia等发现CPT-11与VP-16、铂类没有交叉耐药,与顺铂联合使用后具有协同增效作用,这在Ⅱ期临床研究中得到证实[5]。近年来发现沙利度胺具有抗血管生成作用。动物角膜血管生成试验也证明,沙利度胺具有抗血管生成作用,有可能通过阻断血管内皮生长因子(VEGF)而实现[6]。还有一些动物实验表明沙利度胺能够降低肉芽组织的血管生成[7]。因此晚期小细胞肺癌患者,可通过应用沙利度胺抗肿瘤血管的生成,抑制肿瘤的生长和转移,从而改善临床症状,提高生存质量。
我组观察了IP方案联合沙利度胺二线治疗晚期小细胞肺癌41例,有效率约为48.78%,与文献报道结果相近[8]。 本研究还表明,在EP方案化疗中进展的12例患者中,疗效为16.7%,而缓解期超过3个月的31例患者,疗效为61.3%,表明IP在初始治疗缓解期超过3个月的小细胞肺癌患者治疗,疗效较好,也与文献相符[9]。
IP方案联合沙利度胺作为二线治疗方法仍能能取得较好的近期疗效,且临床反应率高。该方案最常见不良反应为中性粒细胞减少和腹泻。中性粒细胞减少也是剂量限制性毒性,对老年患者、既往接受过多次化疗、KPS评分偏低的晚期患者存在一定风险,故该方案使用过程中应予重视。本组试验Ⅲ 、Ⅳ度腹泻发生率为9.76%,大剂量口服洛哌丁胺(易蒙停)治疗有效,此外补液,加用抗生素及生长抑制八肽等治疗,均能控制,2例患者因为Ⅳ度腹泻退出试验组。该方案恶心、呕吐的消化道反应较轻,耐受性良好,全组无1例治疗相关死亡患者,对于晚期小细胞癌患者较为安全。
综上所述,我们认为CPT-11联合DDP、沙利度胺作为二线治疗SCLC的方案有着较高的有效率,较好的临床受益性,可以耐受的不良反应,值得临床进一步研究推广。
[1]石远凯.肺癌诊断治疗学〔M〕.北京:人民卫生出版社,2008:313.
[2]J~kman DM,Johnson BE.Small cell lung cancer〔J〕.Lancet,2005,366(9494):1385.
[3]Vanhoefer U,Harstrick A,Achterrath W,et al.Irinotecan in the treatment of colorectal cancer:clinical overview〔J〕.J Clin Oncol,2001,19(5):1501.
[4]Hirose T,Horiehi N,Ohmofi T,et al.Phase Ⅱ study of irinoteean and earboplatin in patients with the refractory or relapsed small cell lung cancer〔J〕.Lung Cancer,2003,40(3):333.
[5]Jagasia MH,Langer CJ,Johnson DH,et al.Weekly irinotecan and cisplatin in advanced non-small cell lung cancer:A multicenter phase 1I study〔J〕.Clin Cancer Res,2001,7(1):68.
[6]Kenyon BM.Effects of thalidom ide and related metabolites in a mouse comeal of nevoscularization〔J〕.Exp Eye Res,1997,64:971.
[7]Or R.Thalidom ide reduces vascular density in granulationtissue of subcutaneously implantsd polyvingyl alcohol pongees in guinea pigs〔J〕.Exp Hematol,1998,26:217.
[8]Nishiwaki Y,Kawahara M.Irinotecan plus cisplatin complatin corn-pared with etoposide pule cisplatin for extehsive small cell lung cancer〔J〕.N Engl J Med,2002,346(2):126.
[9]赵 征,廖子君.IP方案二线治疗复发性小细胞肺癌的临床观察〔J〕.现代肿瘤医学,2009,13(5):2118.
