亚甲基蓝在海洋沉积物上的吸附行为*
2011-01-10杨桂朋曹晓燕
郑 轩,杨桂朋,曹晓燕
(中国海洋大学海洋化学理论与工程技术教育部重点实验室,山东青岛266100)
近年来,随着我国印染工业的发展,每年有大量的含染料废水流入各类水体中,染料已成为当前最主要的水体污染源之一,并受到越来越多的关注[1-2]。染料作为一种结构稳定的有机化合物,具有抗酸、抗碱、抗光、抗微生物等特性,在环境中有较长的滞留期,而且很容易在生物体内高度富集,并通过生物链最终进入人体,危及人类健康。研究表明,许多染料对哺乳动物有很强的毒性,甚至有致癌作用。水体中所含染料大多为芳香族化合物,由于其成份复杂、化学需氧量(COD)高、色度深、性质稳定、不易降解,这给治理带来了很大困难[2-4]。国内外大多通过不同的物理、化学和生物过程来分离染料和水体,以达到净化的作用,具体主要包括吸附、微生物降解、化学氧化、絮凝沉淀、过滤和膜分离等方法。与其它方法相比,吸附是比较有效并且经济的一种净化方法,它可以较好的克服其它方法所存在的如成本高、产生二次污染和去除效率低等缺点和局限性[5-6]。目前,国内外对工业废水中染料的研究较多,大多采用加入各种不同的固体颗粒物通过吸附的方法去除工业废水中的染料[7-10]。而对于染料在天然水体中特别是海水中的吸附行为的研究甚少,对于与其它有机污染物共存时在海洋沉积物上的吸附行为研究还未曾发现。据统计每年世界上都会生产超过7×105t染料,种类超过10 000种,它们当中有大约10%~15%未经过处理就排放到天然水体环境中[11-12]。染料进入天然水体后,很容易进入水生生物体内,对水生生物具有很强的毒性,并会使水质变差,破坏水体生态系统,在水环境中会造成长期的不利影响,所以对于染料在天然水体中迁移变化的研究是十分有必要的[13-14]。海洋沉积物通过富集重金属及其他有毒难降解有机物而成为水环境中污染物的蓄库。但是当环境条件发生改变时,吸附在沉积物上的污染物便可能会发生解吸进入水体,这不仅会对上覆水体的水质产生较大污染,还会对底栖生物产生负效应,同时对位于食物链上端的生物和人类产生影响[15]。由此可见,水体中污染物对水生生物和环境的影响以及对它们的评价和控制,都与海洋环境中的液—固界面化学性质密切相关。所以研究染料在海洋沉积物上的吸附行为有助于更好的了解它在天然水体中的迁移变化规律。
亚甲基蓝(MB)作为染料的典型代表,整个分子对称分布,性质稳定[2]。本文以MB作为研究对象,对其在不同站点不同处理方式的海洋沉积物上的吸附行为进行了比较研究,并考察了其它环境因素(介质和温度)以及3种表面活性剂(Tw een20,CTAB,SDBS)的存在对吸附的影响,为进一步了解染料在海洋中的迁移变化规律,综合治理海洋污染提供理论根据。
1 实验部分
1.1 沉积物样品的采集与处理
吸附实验所用的沉积物取自中国沿海,站位和各成分含量列于表1中。采集的沉积物样品分别用H2O2、HC1处理,与只用蒸馏水处理的沉积物做对比。具体处理方法如下[16-17]:
原始样:只用少量蒸馏水洗涤,然后抽滤,自然干燥,研磨过筛取40~80目样品密封备用。
HCl处理:将一定量的沉积物样品和一定量的蒸馏水混合,用HCl来调节悬浊液的p H=2,浸泡搅拌1 d,然后将样品用蒸馏水洗至p H=4,抽滤,自然干燥,研磨过筛取40~80目样品密封备用。盐酸处理后,除去了大部分碳酸盐。
H2O2处理:在一定的沉积物中加入30%H2O2和0.02 mol/L HNO3溶液,置于(85±2)℃水浴中2 h,然后再加入30%H2O2,用0.02 mol/L HNO3溶液调节p H=2,再置于(85±2)℃水浴中4 h,最后将样品用蒸馏水洗涤,抽滤,自然干燥,研磨过筛取40~80目样品密封备用。此处理由于氧化掉了沉积物中部分有机碳,因而使单位质量沉积物的有机碳含量降低。
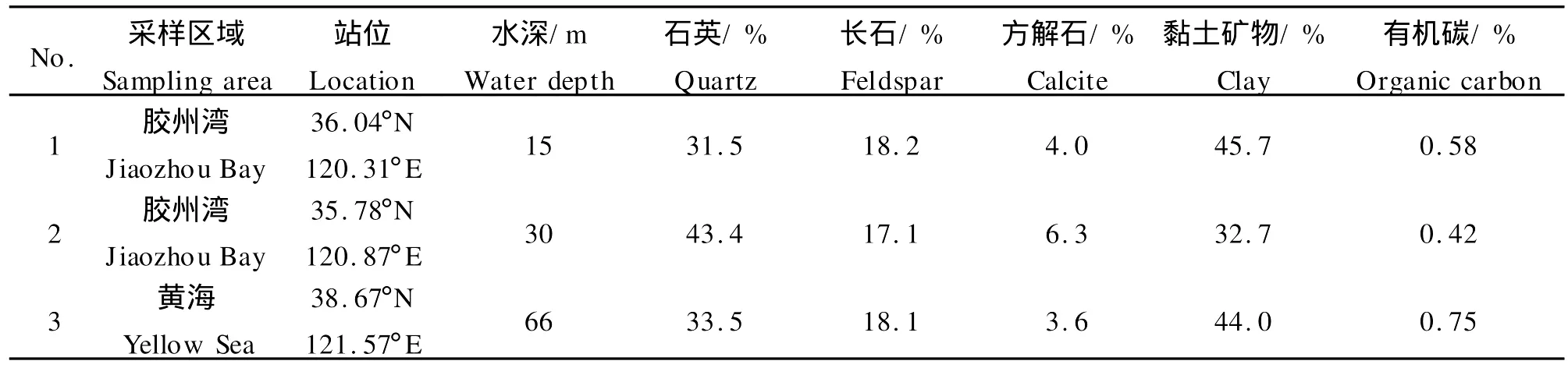
表1 沉积物采集的站点及主要成分组成Table 1 Sampling stationsof sediments and percentages of their compositions
1.2 实验介质溶液的配制
天然海水(Natural seaw ater简写为NSW):取自青岛石老人附近海域,经过0.45μm混合纤维滤膜过滤。盐度为33.4,p H为8.1;稀释海水(Diluted Seawater简写为DSW):海水与蒸馏水以1∶1的比例混合稀释而成,盐度为16.7;蒸馏水(Distilled water简写为DW):盐度为0;使用NaOAc-HOAc缓冲溶液将稀释海水和蒸馏水的p H值皆调节到与天然海水相同。
实验中所用浓度范围可能要高于天然海水环境下各种有机污染物的浓度,但从仪器分析灵敏度以及模拟实验的角度出发,提高浓度是必要的。
1.3 标准溶液的配制
亚甲基蓝(MB),美国Fluka试剂公司,在25℃时水中溶解度>100 g/L。可以采取直接称量加入法,用万分之一分析天平准确称量MB(0.100 0±0.000 2)g,溶于1 L不同介质(NSW,DSW,DW)中,配得最后浓度为100 m g/L的标准溶液。吐温20(Tw een20)和十六烷基三甲基溴化铵(CTAB),纯度(99%,Acros Organic(美国);十二烷基苯磺酸钠(SDBS),纯度(99%,Tokyo Kasei Kogyo Co.,日本。3种表面活性剂的溶解度都很好,可以采用直接加入法,配得最后浓度为500 mg/L的标准溶液。其它试剂均为国产分析纯。
1.4 吸附平衡试验
在吸附动力学的实验中,准确称量沉积物(0.050 0±0.000 1)g若干份于150 mL磨口三角瓶中,各加入相同体积的MB标准溶液及一定量的不同介质(NSW,DSW,DW)使悬浮液总体积为50 m L。溶液p H调至(8.10±0.03),整个实验中保持恒定。样品于(25±0.5)℃下在恒温振荡器中振荡。定时取样10 mL后,固液相离心分离(5 m in,4 000 r/min),取上清液用UV-2550紫外可见分光光度计(岛津公司,日本)测定MB的浓度。3种介质最大吸收波长均为665 nm。根据起始浓度与平衡浓度之差并扣除空白(颗粒物空白用不加MB的沉积物溶液,以消除沉积物中有机质溶出对测定的影响;有机物空白,用不加沉积物的MB溶液,以消除瓶壁吸附对测定的影响),计算MB吸附量,作吸附平衡曲线。实验证明MB的挥发、光解、微生物降解等均可忽略不计。吸附热力学实验方法同上所述,区别在于所加入的MB的量不同。
2 结果与讨论
2.1 吸附平衡时间
由图1可见,25℃时MB的吸附平衡时间为4 h。为了保证MB在沉积物上达到完全吸附,本实验在10 h之后检测其浓度。从图1a还可看出,不同介质中MB的吸附量差异显著,在NSW中饱和吸附量明显小于在DW中饱和吸附量。图1b显示了3种表面活性剂的加入对吸附平衡时间的影响不大,但是对饱和吸附量有一定的影响。

图1 25℃下MB在3种介质条件下(a)和在海水介质中与3种表面活性剂共存时(b)在3号站位水处理沉积物上的吸附平衡时间Fig.1 So rption equilibration time of MB on No.3 station H2 O-treated sediment in three kinds of media at 25℃(a)and with 40 mg/L surfactants(CTAB,SDBS,Tween20)in NSW at 25℃(b)
2.2 吸附等温线
MB在3个站点用不同方式处理的沉积物上的吸附等温线如图2所示,可以明显地看出吸附等温线是非线性的。非线性吸附常用Freundlich等温式描述,它是溶质由液相到固相表面吸附的经验关系式,涉及到表面的不均匀性和吸附位的指数分布以及吸附能量,与黏土矿物的表面作用和微孔吸附有关[18-22],其表达式为:

其中Cs表示单位沉积物吸附的MB的量(mg/g);Ce是溶液中MB的平衡浓度(m g/L);K与n为Freundlich经验常数,K可以反映吸附强度,而n可以体现某一特定吸附过程中的能量大小及变化。
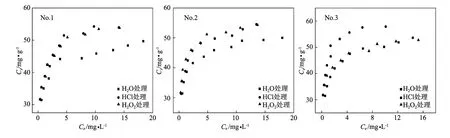
图2 25℃下海水介质中MB在3个站点3种处理方式沉积物上的吸附等温线Fig.2 Sorption isotherm s of MB on sediments treated by three methods at three sites in NSW at 25℃
用Freundlich吸附模式回归分析后的吸附方程式和相关系数(R2)如表2所示。由图2和表2可以看出MB在海洋沉积物上的吸附行为可以很好的用Freundlich等温式拟合,这说明黏土矿物的表面作用和微孔吸附在吸附过程中起到了重要作用。各个站位用不同方式处理的沉积物吸附能力略有不同。与H2O处理样品相比,盐酸处理会将沉积物中的碳酸盐、大部分氧化物、金属离子去除[16],3个站点的吸附能力:HCl处理样>H2O处理样,这说明碳酸盐和氧化物等对吸附并不起到促进作用,反而会阻碍MB在黏土矿物上的吸附;H2O2处理会将大部分覆盖在沉积物表面上的有机质氧化[17],有机碳含量相对下降,而3个站点的吸附能力:H2O2处理样≥H2O处理样,这说明有机碳含量与吸附量并没有相关性,有机质的分配作用并不是吸附的主要机理。综上所述,可以得出结论:有机质的分配作用对于MB在沉积物上的吸附能力影响不大,吸附主要是以黏土矿物的表面作用和微孔吸附为主。由于海洋沉积物中黏土矿物的种类繁多,吸附能力和机理也各有差异,如表1所示3个站点的沉积物中黏土矿物的种类和含量各有区别,所以3个站点的沉积物对MB的吸附能力也各不相同。

表2 25℃下海水介质中MB在3个站点3种处理方式沉积物上的Freundlich吸附等温式Table 2 Freundlich isotherm s of MB on sediments treated by threemethods at three sites in NSW at 25℃
2.3 影响因素
2.3.1 介质的影响 选取3号站点H2O处理沉积物来研究介质对MB在沉积物上吸附行为的影响,图3a描述了3种介质中MB的吸附等温线,表3列出了拟合方程和相关系数。从图3a和表3可以看出MB在3种介质中的吸附能力顺序依次为:DW>DSW≈NSW,这说明在DW中MB的吸附能力要强于在NSW中。原因可能如下:海水中含有大量不同种类的离子及有机物质,它们会与MB之间产生竞争吸附,使沉积物表面上的有效吸附位点减小,MB的吸附量会随之减小[1,23-24]。
2.3.2 温度的影响 从图3b和表3可以看出,在本实验温度范围内,MB的吸附行为很好地符合Freundlich吸附等温式,温度对MB在沉积物上的吸附影响并不明显。
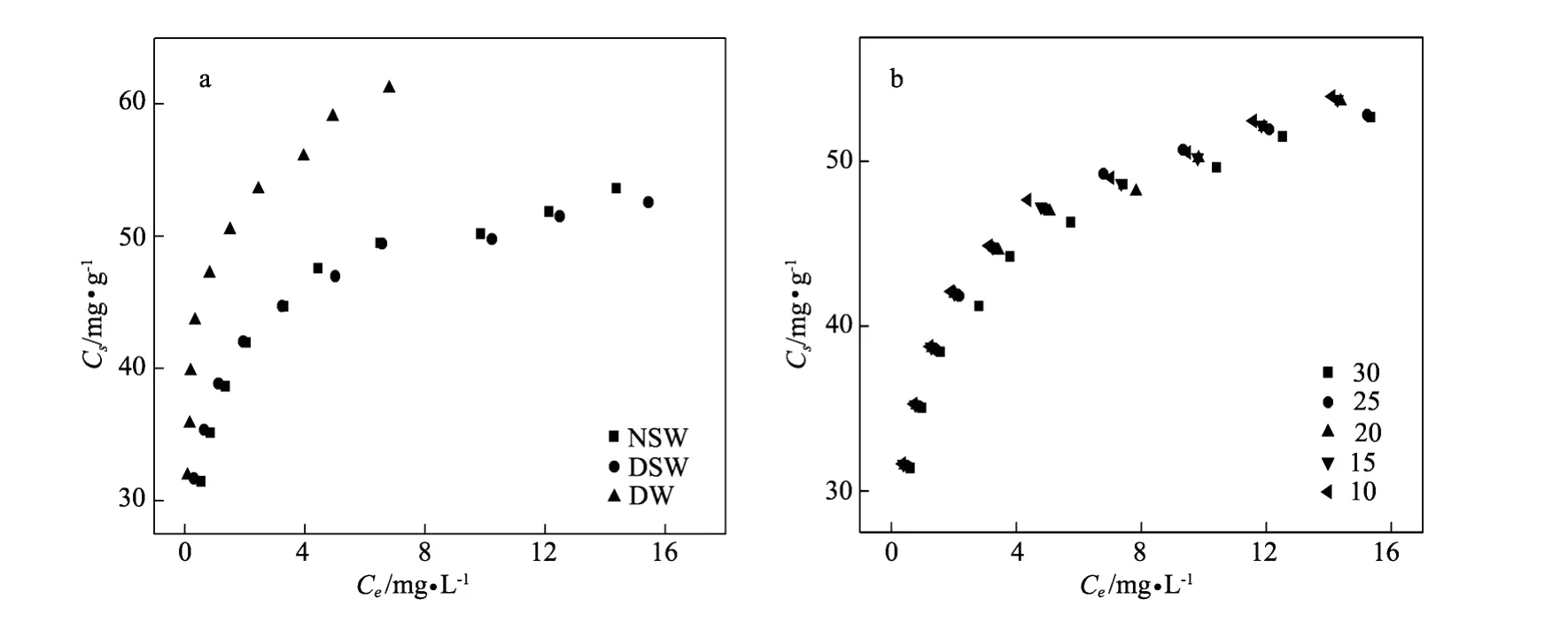
图3 MB在25℃3种介质条件下(a)和在NSW中不同温度条件下(b)在3#水处理沉积物上的吸附等温线Fig.3 Sorption isotherm s of MB on 3#H2 O-treated sediments in three media at 25℃(a)and in NSW at different temperatures(b)
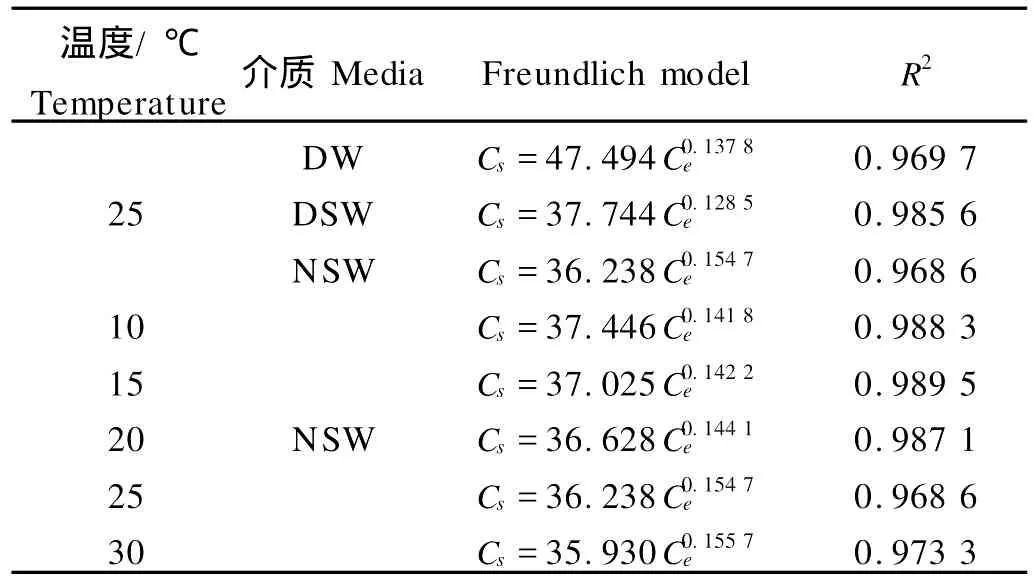
表3 25℃3种介质条件下和海水介质不同温度条件下MB在3号站点水处理沉积物上的Freundlich吸附等温式Table 3 Freundlich isotherms of MB on 3#H2 O-treated sediments in three media at 25℃and in NSW at different temperatures
2.3.3 表面活性剂的影响 表面活性剂是一类加入量很少就能使液体表面张力降低的有机化合物,素有“工业味精”之美称,广泛应用于石油、纺织、农药、医药、采矿、食品、民用洗涤等各个领域。它是由具有亲水性的极性基团和具有憎水性的非极性基团组成的,这2部分分处于表面活性剂分子的两端,形成不对称的结构。表面活性剂具有润湿、起泡、乳化、分散、增溶、均染、洗涤等特性,它在环境中的存在对其它有机污染物的迁移、吸附、脱附等环境行为会产生重大影响[25]。目前,有许多研究利用这一特性进行被污染土壤的清洗与修复。进入海洋水体中的表面活性剂会吸附在沉积物上,从而影响其物理化学及生物性质比如沉积物胶体的稳定性、微生物的新陈代谢等[26],由于大部分表面活性剂不能降解,还会对海洋生态环境产生危害[27]。此外表面活性剂对海洋中的部分无脊椎和高等动物具有中等毒性[28],可抑制沉积物中微生物和植物的生长,妨碍水中鱼的生长和某些晶胞的生长并对海洋产生二次污染,同时也对其他有毒有机物的环境行为产生影响[29-32]。
Tween20、CTAB和SDBS作为典型的表面活性剂,它们的应用非常广泛,并分别属于非离子、阳离子和阴离子3类表面活性剂的代表物质。本文利用以上3种不同类型的表面活性剂作为共存污染物来模拟复合污染体系,研究它们对于MB在海洋沉积物上的吸附所产生的不同影响。为了解不同种类的有机污染物在海洋中共存时吸附行为的研究提供一定的理论基础。
图4~7反映了3种表面活性剂(CTAB,Tween20,SDBS)对MB在沉积物上吸附量及吸附等温线的影响情况。所有吸附等温线都符合Freundlich模型,表4显示了等温线的拟合方程和相关系数。由图4~7和表4可以看出,3种表面活性剂的加入对MB在沉积物上的吸附能力会产生不同的影响。
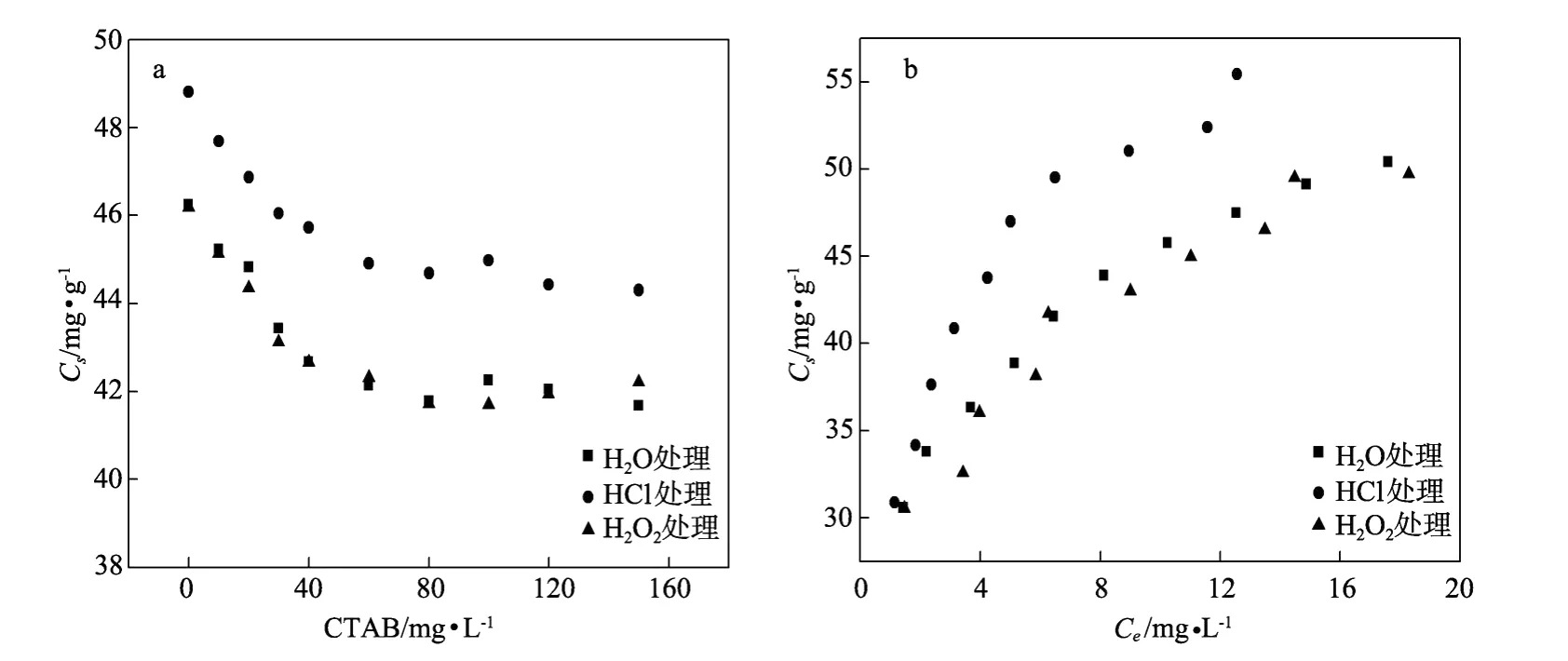
图4 25℃海水介质中,在3#3种处理方式沉积物上不同浓度CTAB的存在对MB(50 mg/L)吸附的影响(a)和40 mg/LCTAB存在下MB的吸附等温线(b)Fig.4 The effect of CTAB on so rp tion of MB(50 mg/L)(a)and sorption isotherms for MB with 40 mg/L CTAB(b)on 3#sediments treated by three methods in NSW at 25℃

图5 25℃海水介质中,在3#3种处理方式沉积物上不同浓度Tween20的存在对MB(50 mg/L)吸附的影响(a)和40 mg/L Tween20存在下MB的吸附等温线(b)Fig.5 The effect of Tween20 on sorp tion of MB(50 mg/L)(a)and sorp tion isotherms for MB with 40 mg/L Tween20(b)on 3#sediments treated by threemethods in NSW at 25℃
通过图4与图2的比较可以看出CTAB的加入对吸附产生了很大的影响。随着CTAB浓度的增加,沉积物对MB的吸附能力越来越小,当CTAB的加入量达到80 m g/L时,MB的吸附量达到最小值,之后CTAB浓度的增加对吸附量的影响不大。由于表面活性剂有增溶作用,它的加入可以增加MB在溶液中的溶解度,使MB更倾向于留在溶液中而使吸附在沉积物上的量减小。另外表面活性剂的加入使得它与MB产生竞争吸附,CTAB占据沉积物上的吸附位点使得MB的表面吸附作用减弱。由于MB自身溶解度较高,所以增溶效应并不明显,影响因素以竞争吸附为主。随着浓度的增加,CTAB在沉积物上的吸附达到饱和,再增加CTAB的浓度,对MB的吸附本身影响不大[33-34]。图5反映的是Tw een20的加入对MB的吸附产生的影响,与图2比较后会发现Tw een20对MB在沉积物上的吸附能力影响不大,随着Tween20浓度的增加,吸附量基本保持不变。Tw een20是一种非离子型表面活性剂,它的吸附主要以有机质分配为原理,并不会与MB产生竞争吸附[35-36]。所以它对MB在沉积物上的吸附影响较小,这与实验结果相符合。同理本文通过对图2和图6的比较来了解SDBS的加入对吸附产生的影响,结果表明SDBS的加入对吸附起到了抑制作用,实验结果与CTAB对吸附的影响较为接近。SDBS是一种阴离子表面活性剂,它既可以通过有机质分配作用也可以通过静电、氢键等作用吸附在沉积物上[37-40]。它可以改变MB的溶解度以及与MB产生竞争吸附,这都会影响MB在沉积物上的吸附,使之吸附量减小。
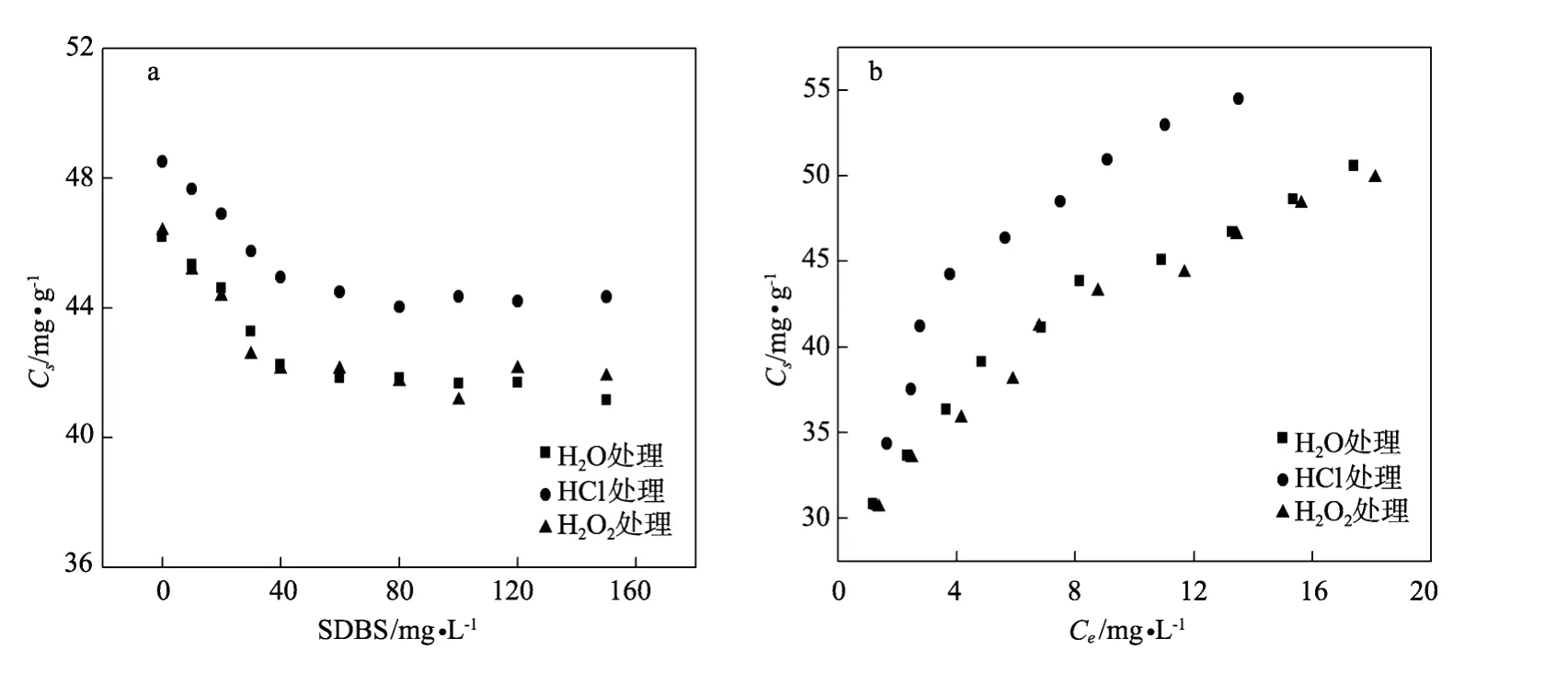
图6 25℃海水介质中,在3#3种处理方式沉积物上不同浓度SDBS的存在对MB(50 mg/L)吸附的影响(a)和40 mg/L SDBS存在下MB的吸附等温线(b)Fig.6 The effect of SDBSon so rp tion of MB(50 mg/L)(a)and sorp tion isotherms for MB with 40 mg/L SDBS(b)on 3#sediments treated by threemethods in NSW at 25℃

图7 25℃蒸馏水介质中,在3#水处理方式沉积物上不同浓度表面活性剂的存在对MB(60 mg/L)吸附的影响(a)和40 mg/L表面活性剂存在下MB的吸附等温线(b)Fig.7 The effect of surfactant on so rp tion of MB(60 mg/L)(a)and sorption isotherms for MB with 40 mg/L surfactant(b)on 3#H2O treatment sediments in DW at 25℃
由于介质的改变会对MB的吸附产生较大的影响,所以作为对比对DW中3种表面活性剂对MB在沉积物上吸附的影响进行研究是非常有必要的。在DW中3种表面活性剂对MB在沉积物上吸附的影响情况如图7和表4所示。将其分别与图3a和表3中MB在DW中的吸附等温线和Freundlich吸附等温式作比较,可以发现在DW中Tw een20对吸附的影响仍然不明显,吸附量基本保持不变,这说明在这两种介质中Tw een20对MB在沉积物上的吸附能力影响不大,对吸附过程和机理的影响也基本一致。与之相对应的是CTAB和SDBS在NSW和DW这两种介质中对MB的吸附影响并不相同。在DW中CTAB仍然对吸附起着阻碍作用,但是与在NSW中相比,它使MB的吸附量减小得更加明显;SDBS则对吸附起促进作用,使MB的吸附量略有增大。产生以上结果的具体原因有待进一步研究。
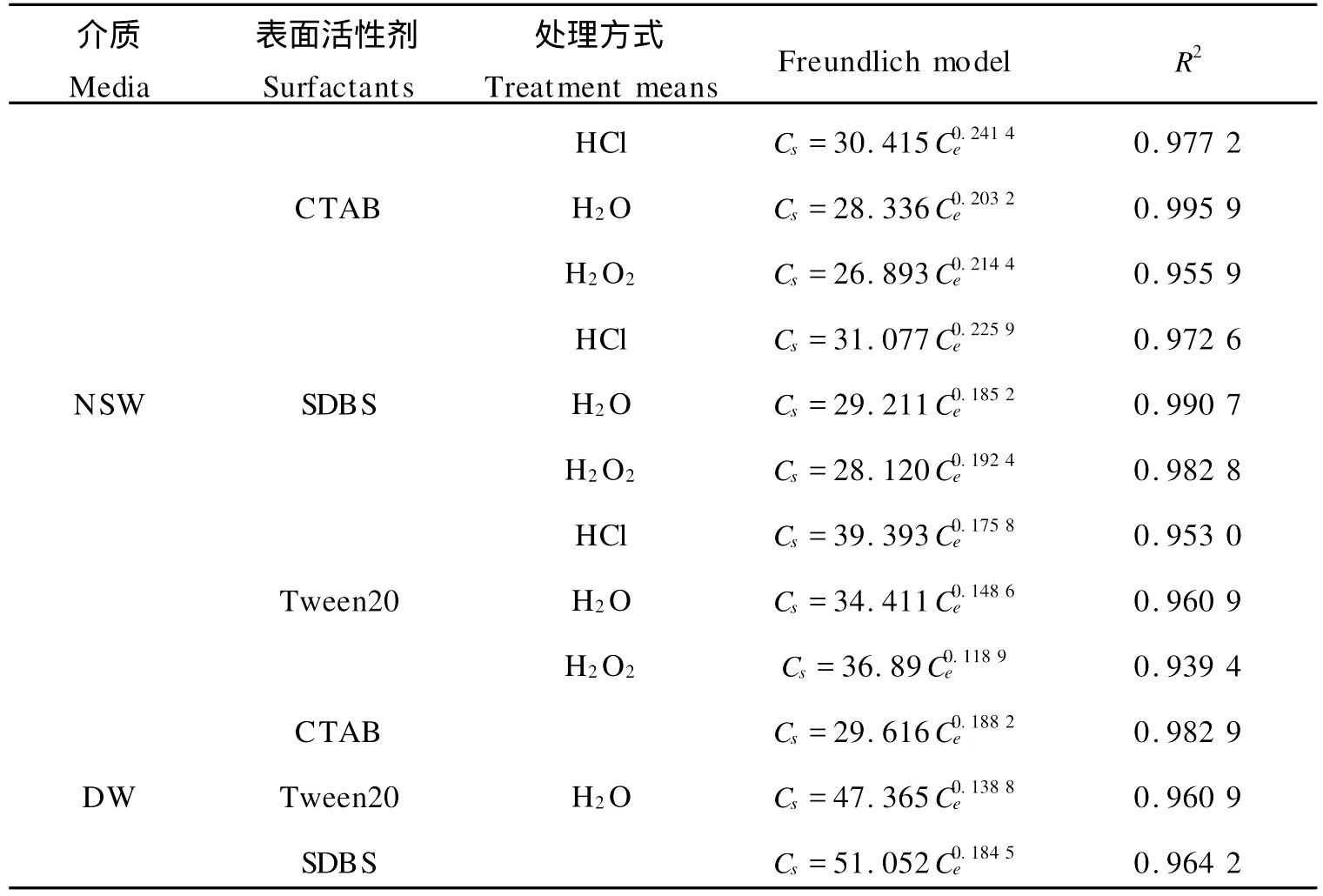
表4 25℃NSW和DW介质中3种表面活性剂存在下MB在3号站点水处理沉积物上的Freundlich吸附等温式Table 4 Freundlich isotherms of MB with three kinds of surfactants on 3#H2 O-treated sediments in NSW and DW at 25℃
3 结论
(1)MB在海洋沉积物上的吸附平衡时间为4 h,在用3种方式处理过的沉积物上的吸附行为都可以用Freundlich等温式很好地描述。沉积物颗粒的表面作用和微孔吸附是影响其吸附行为的主要机理。
(2)介质的不同对MB的吸附行为影响很大,DW中MB的吸附能力要强于NSW中;随着温度的升高,MB的吸附能力变化并不明显。
(3)当加入3种类型的表面活性剂时,MB的吸附能力会产生不同的变化,在NSW和DW 2种介质中,吸附能力的变化也不尽相同。在NSW和DW中,非离子表面活性剂的加入对吸附的影响均不大;阳离子表面活性剂的加入使MB的吸附能力减弱,在DW中抑制作用更加明显;在DW中,阴离子表面活性剂对吸附起到促进作用,而在NSW中,却对吸附有抑制作用。
[1] 李生英,魏云霞,马明广.改性腐殖酸对染料甲基紫的吸附研究[J].安徽农业科学,2008,36(19):8285-8391.
[2] 路英杭,冯翰林,孙中溪.铝硅酸盐对亚甲基蓝的吸附行为[J].济南大学学报:自然科学版,2009,23(1):18-21.
[3] Wu S H,Tseng R S.Kineticsof color removal by adsorp tion from water using activated clay[J].Environ Technol,2001,22(6):721-729.
[4] Jin X Y,Jiang M Q,Shan X Q,et al.Adsorption of methylene blue and orangeⅡonto unmodified and surfactant-modified zeolite[J].J Colloid interf Sci,2008,328(2):243-247.
[5] Gupta V K,Mittal A,Krishnan L,et al.Adsorption treatment and recovery of the hazardous dye,Brilliant Blue FCF,over bottom ash and de-oiled soya[J].J Colloid interf Sci,2006,293(1):16-26.
[6] Han R P,Wang Y,Zou W H,et al.Comparison of linear and nonlinear anaysis in estimating the Thomas model parameters for methylene blue adsorption onto natural zeolite in fixed-bed column[J].J Hazard Mater,2007,145(1-2):331-335.
[7] Ghosh D,Bhattacharyya K G.Adsorption of methylene blue on kaolinite[J].Appl Clay Sci,2002,20:295-300.
[8] Yao Y J,Xu F F,Chen M,et al.Adsorption behavior of methylene blue on carbon nanotubes[J].Bioresource Technol,2010,101(9):3040-3046.
[9] Poots V J P,M c Kay G,Healy J J.The removal of acid dye from effluent using natural adsorbents-ⅡWood[J].Water Res,1976,10(12):1067-1070.
[10] Doˇgan M,Alkan M,Onganer Y.Adsorption of methylene blue from aqueous solution onto perlite[J].Water Air Soil Pollut,2000,120(3-4):229-248.
[11] Cengiz S,Cavas L.Removal of methylene blue by invasive marine seaweed:Caulerpa racemosa var.cylindracea[J].Bioresource Technol,2008,99:2357-2363.
[12] Senthilkumaar S,Kalaamani P,Porkodi K,et al.Adsorption of dissolved Reactive red dye from aqueousphase onto activated carbon p repared from agricultural waste[J].Bioresource Technol,2006,97(14):1618-1625.
[13] 周琪,赵由才.染料对人体健康和生态环境的危害[J].环境与健康杂志,2005,22(3):229-231.
[14] Selkirk J K,Soward SM.Compendium of abstracts from longterm cancer studies reported by the national toxicology p rogram of the national institute of environmental health sciences from 1976 to 1982(includes up-to-date addendum)[J].Environ Health Perspect,1993,101:295-394.
[15] 王菊英.海洋沉积物的环境质量评价研究[D].青岛:中国海洋大学,2004.
[16] Zhao X K,Yang G P,Wu P,et al.Study on adsorp tion of chlorobenzene on marine sediment[J].J Colloid Interf Sci,2001,243(2):273-279.
[17] Yang G P,Zhang ZB.Adsorption of dibenzothiophene onmarine sediments treated by a sequential p rocedure[J].J Colloid Interf Sci,1997,192(2):398-407.
[18] 吴萍,杨桂朋,赵润德.苯酚在海洋沉积物上的吸附作用[J].海洋与湖沼,2003,34(4):346-354.
[19] Wang JM,Huang C P,Allen H E,et al.Adsorp tion characteristics of dye onto sludge particulales[J].J Colloid interf Sci,1998,208(2):518-528.
[20] Johnson M D,Huang W L,Dang Z,et al.A distributed reactivity model for sorption by soils and sediments.12.Effects of subcritical water extraction and alterations of soil organic matter on sorption equilibria[J].Environ Sci Technol,1999,33(10):1657-1663.
[21] Fytianos K,Voudrias E,Kokkalis E.Sorption-desorption behaviour of 2,4-dichlorophenol by marine sediments[J].Chemosphere,2000,40(1):3-6.
[22] Vasanth Kumar K,Sivanesan S.Isotherms for malachite green onto rubber wood(Hevea brasiliensis)saw dust:comparison of linear and non-linearmethods[J].Dyes Pigments,2007,72(1):124-129.
[23] 贾海红,韩宝平,马卫兴,等.壳聚糖对4种染料的吸附行为研究[J].淮海工学院学报:自然科学版,2008,17(3):48-51.
[24] 张劲强,董元华.阳离子强度和阳离子类型对诺氟沙星土壤吸附的影响[J].环境科学,2007,28(10):2383-2388.
[25] 董国君,苏玉,王桂香.表面活性剂化学[M].北京:北京理工大学出版社,2009
[26] Rao P H,He M.Adsorption of anionic and nonionic surfactant mixtures from synthetic detergents on soils[J].Chemosphere,2006,63:1214-1221.
[27] Fernandez N,Chacin E,Gutierrez E,et al.An analysis of the absorption of alkyl benzene sulphonate by algal residues[J].Process Biochem,1996,31(4):333-336.
[28] KloepperSams P,Torfs F,Feijtel T,et al.Effects assessments for surfactants in sludge-amended soils:a literature review and perspectives for terrestrial risk assessment[J].Sci Total Environ,1996,185:171-185.
[29] Prats D,Rodriguez F,De La Muela M.Las inmarine sediments.Proceedings of the 26th Symposium on Tensite Detergents[J].Barcelona,1995:177-190.
[30] Jones-Hughes T,Turner A.Sorption of ionic surfactants to estuarine sediment and their influence on the sequestration of phenanthrene[J].Environ Sci Technol,2005,39:1688-1697.
[31] Ko SO,Schlautman M A,Carraway E R.Partitioning of hydrophobic organic compounds to sorbed surfactants.1.Experimental studies[J].Environ Sci Technol,1998a,32:2769-2775.
[32] DiVincenzo J P,Dentel S K.Sorption-desorption of 1,2,4-trichloro-benzene on soil:anionic surfactant and cationic polyelectrolyte effects[J].J Environ Qual,1996,25:1193-1202.
[33] Aroguz A Z,Gulen J,Evers R H.Adsorption of methylene blue from aqueous solution on pyrolyzed petrified sediment[J].Bioresource Technol,2008,99(6):1503-1508.
[34] A tun G,Tun ay M,Hisarli G,et al.Adsorption equilibria between dye and surfactant in single and binary systems onto geological materials[J].Appl Clay Sci,2009,45(4):254-261.
[35] 杨桂朋,李芯芯,曹晓燕.Tween20在海洋沉积物上的吸附行为[J].中国海洋大学学报:自然科学版,2008,38(2):309-314.
[36] 杨成建,曾清如,张静,等.非离子表面活性剂在土壤/沉积物中的吸附模型研究[J].农业环境科学学报,2007,26(4):1396-1401.
[37] 饶品华,徐菁利,张文启,等.表面活性剂在土壤粒子上的吸附及影响因素综述[J].安徽农业科学,2009,37(14):6542-6545.
[38] 曹罡,莫汉宏,安凤春.阴离子表面活性剂对2,4-D在土壤中吸附的影响[J].环境化学,2002,21(4):356-359.
[39] Haigh SD.A review of the interaction of surfactants with organic contaminants in soil[J].Sci Total Environ,1996,185(1-3):161-170.
[40] Jones H T,Turner A,Sorption of ionic surfactants to estuarine sediment and their influence on the sequestration of phenanthrene[J].Environ Sci Technol,2005,39(6):1688-1697.
