纯化及羧化多壁碳纳米管吸附铀的研究
2011-01-09刘淑娟李金英罗明标张麟熹
刘淑娟,李金英,罗明标,杨 佳,张麟熹
1.中国原子能科学研究院,北京 102413;
2.东华理工大学 应用化学系,江西 抚州 344000
纯化及羧化多壁碳纳米管吸附铀的研究
刘淑娟1,2,李金英1,罗明标2,*,杨 佳2,张麟熹2
1.中国原子能科学研究院,北京 102413;
2.东华理工大学 应用化学系,江西 抚州 344000
对商品多壁碳纳米管(MWNTs)进行纯化及硝酸羧化处理,并对其分别进行热重及红外表征。研究了纯化和羧化MWNTs对溶液中铀的吸附行为,考察了介质酸度、温度、吸附时间、溶液中铀的初始质量浓度对吸附容量的影响。实验结果表明,有质量比约为10%的羧基成功接枝于MWNTs,羧化MWNTs比纯化MWNTs表面更为粗糙,且出现羧基的特征红外波数为2 913cm-1及1 641cm-1。在pH=3.0~6.0范围内,2种MWNTs对铀的吸附量随着pH和平衡浓度的增大而升高,反应时间与温度对吸附容量的影响不大。2种MWNTs的等温吸附及热力学模型研究表明,吸附反应符合Freundlich和Langmuir方程,在最佳条件下,静态平衡吸附量分别为47.81mg/g和89.09mg/g。
多壁碳纳米管;表征;吸附铀;吸附模型
铀是核能发展中至关重要元素之一,目前环境中其主要来源主要有:铀矿山开采的固体和液体废物,含铀矿物(如含铀磷矿)的矿渣,核燃料加工及乏燃料后处理废物,核试验落下灰及贫铀弹使用等几个方面。由于其具有放射性,一旦暴露于环境中,将会对人类健康及生态系统构成严重的危害[1-2]。目前溶液中铀的处理方法主要有沉淀、共沉淀法、溶剂萃取法、离子交换法和吸附法等[3-5]。其中,吸附法因其去除率高、处理工艺简单等被广泛研究与应用。传统铀吸附材料在实际应用中存在吸附容量低、选择性不佳、吸附稳定性差或吸附速度较慢等缺陷,寻找新型吸附铀材料以克服传统吸附材料的不足意义重大。与普通块体材料相比,纳米材料具有更多的表面原子,显示出更强的吸附能力,这为寻找吸附核素的新材料在纳米方向提供依据。
MWNTs是一种统一结构的一维管状无机纳米材料,其具有高比表面积,相对于一般的吸附材料在重金属离子吸附方面表现出较高的吸附性能。研究表明,MWNTs表面含氧官能团越多,其吸附金属阳离子能力越强,在其表面引入羟基(—OH)、羧基(—COOH)等亲水性基团有利于增加水相中与金属离子的有效接触面积;另外这些基团中含氧配体可与重金属离子产生配位作用,从而提高金属离子的吸附能力[6-8]。
当前MWNTs应用于分离富集放射性核素的研究不多,且吸附机理也没有统一的看法,其中Fabiobelloni[9]研究表明,MWNTs在核电厂废液的处理、污染地的环境修复、废物固化、废物储存等方面具有潜在的应用价值。
本工作拟对商品MWNTs进行纯化和硝酸改性,研究引入含氧配体的MWNTs对铀的吸附性能,以期为MWNTs在放射性核素的分离富集方面应用奠定基础。
1 实验部分
1.1 试剂和仪器
铀标准溶液 1g/L,HAc-NaAc缓冲溶液(pH=5.9),氯乙酸-乙酸钠缓冲溶液(pH =2.5)。0.05%偶氮胂Ⅲ,分析纯,上海璞光实业有限公司;十二烷基磺酸钠,分析纯,上海蓝源生物科技有限公司;多壁碳纳米管,中科院成都有机化学研究所。
721E可见分光光度计,上海光谱仪器有限公司;KQ 3200E超声仪,中国玉环曙峰公司;STA409PG型综合热分析仪,德国耐驰公司,Nicolet 380型傅里叶变换红外仪,上海赛默非公司;R-3000拉曼光谱仪,长春博盛公司。
1.2 实验方法
1.2.1 MWNTs的纯化 称取10g商品MWNTs,加入120mLw=47%的HF搅拌12h,洗至中性后,加入200mL 3mol/L HNO3溶液中65℃下回流48h,再次洗至中性,在80℃真空烘箱内干燥24h,再于管式炉中程序升温加热,先在250℃下空气中加热2.5h,然后于450℃下氮气保护加热2.5h。
1.2.2 MWNTs的羧化 称取上述纯化好的MWNTs 5g,加入100mL浓度为60%的HNO3溶液,60℃下搅拌、回流48h后,洗至中性,在80℃真空烘箱内干燥24h。
1.2.3 纯化及羧化MWNTs的表征 分别称取10mg处理过的纯化及羧化MWNTs,置于综合热分析仪上,从0℃开始加热到700℃,测试其失重情况。分别称取10mg纯化及羧化MWNTs放到单晶硅片表面,在激发光源照射下,观察其拉曼光谱峰。同样分别称取10mg纯化及羧化MWNTs在傅立叶红外仪中做红外表征观察其化学键的变化。
1.2.4 铀的吸附和测定 称取0.02g MWNTs若干份分别放入聚碳脂瓶中,并加入10mL不同pH值的含铀2mg溶液,震荡20min,过滤,取0.5mL滤液按标准曲线显色,以试剂空白为参比,测其吸光度,然后在最佳酸度下进行同样吸附实验来分别探讨震荡时间、温度条件对MWNTs吸附容量影响,并考察该吸附等温模型。在不同温度下考察铀浓度变化情况来获得该吸附反应的热力学参数,铀浓度分析采用偶氮胂Ⅲ为显色剂可见光度法[10]。
2 结果与讨论
2.1 碳纳米管的表征
2.1.1 热重曲线 图1为纯化及羧化 MWNTs热重曲线图。由图1可知,羧化与纯化MWNTs均在475℃左右开始分解,二者质量相比失重率相差10%左右,即经过羧化,大约有10%的羧基接枝到多壁碳纳米管表面。
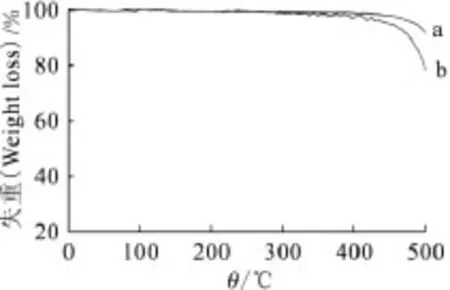
图1 纯化 MWNTs(a)和羧化 MWNTs(b)的热重曲线Fig.1 Thermogravimetric curves of the purified MWNTs(a)and carboxylated MWNTs(b)
2.1.2 拉曼光谱 在激发光源照射下,MWNTs表面的凹凸不平程度可通过反映出来的光强度值不同看出,其中无序峰在1 350cm-1左右,即D(disorder)峰代表碳纳米管表面的不规整性,D峰的峰面积越大,或者它的峰高度越高,说明MWNTs的表面越不规整;位于1 580cm-1左右的吸收峰称为G(graphite),反映sp2杂化碳原子的结构强度,对应于石墨中的E2g振动模式。峰强度代表MWNTs的规整度,G峰的峰面积越大,或者它的峰高度越高,说明碳管的表面越规整;2G峰为石墨烯的倍频峰,在2 600cm-1左右。对于多壁碳纳米管改性表征中,D峰和G峰最重要,羧基化后的样品的两个峰强度比值ID/IG越大,说明 MWNTs羧化越成功,反之越不成功。图2为纯化和羧化MWNTs的拉曼光谱图。由图2可知,MWNTs的特征拉曼峰即D峰和G峰的位置分别在1 352和1 582cm-1,羧化MWNTs的拉曼曲线峰面积比值(ID/IG)比纯化MWNTs的略大,表明其表面更不规则,这主要是因为羧化MWNTs表面成功引入了羧基基团,表明羧化成功。
2.1.3 红外光谱 氟化氢及硝酸处理商品碳纳米管能将其表面的无机杂质去除而达到纯化目的,羧化则是在浓硝酸中,高温回流,使单质碳纳米管发生一定程度脱硝反应,在表面产生含氧基团。图3为纯化和羧化MWNTs的红外光谱。从图3可知,与纯化 MWNTs相比,在波数为2 913cm-1的位置有1个较宽的C—H伸缩振动峰,碳管表面的—COOH振动峰与MWNTs表面苯环的C—H伸缩振动峰位置有较明显的区别,这排除了该位置是碳管表面苯环的伸缩振动峰。另外,在波数为1 642cm-1的位置处,羧化和纯化MWNTs相比有一个更强的尖峰,这是羧基的CO伸缩振动峰,虽然这个峰与碳管表面苯环的伸缩振动峰位置近似重合,但羧化的碳管在该位置的伸缩振动峰更强,可以推断此为羧基的伸缩振动峰。
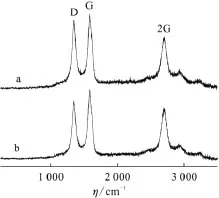
图2 纯化 MWNTs(a)和羧化 MWNTs(b)的拉曼光谱Fig.2 Raman spectra of the purified MWNTs(a)and carboxylated MWNTs(b)
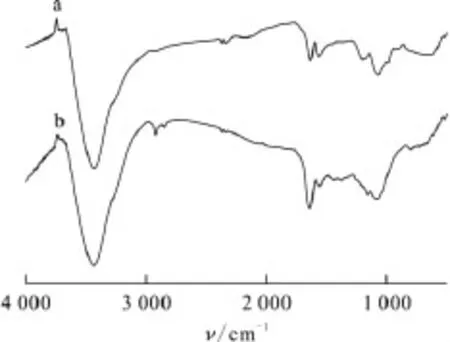
图3 纯化 MWNTs(a)和羧化 MWNTs(b)的红外光谱Fig.3 Infrared spectrogram of the purified MWNTs(a)and carboxylic MWNTs(b)
2.2 酸度影响
pH对吸附剂吸附溶液中的重金属离子吸附有着一定的制约作用,这与氢离子会和重金属离子产生竞争吸附有关。由于pH≤3.0时,溶液中的H+浓度相对较高,占据吸附剂表面的吸附位点多,造成对吸附不明显。当溶液pH>6.0时,其吸附容量降低,这是因为发生水解阻碍了MWNTs的吸附。图4为不同pH值下纯化和羧化MWNTs对铀的吸附影响图。由图4可以看出,溶液pH为3.0~6.0时,吸附容量随着溶液pH的增大而增加;pH=6.0时,纯化和羧化MWNTs的平衡吸附量分别为39.81mg/g和68.71mg/g。

图4 不同pH对UO+吸附Fig.4 Adsorption of uranium ion at different pH value ρ(UO+ )=0.5g/L,θ=15℃,
图4表明经过羧化处理的MWNTs的吸附能力明显的比经过纯化MWNTs的吸附能力要强,这是因为经过酸化改性后的表面增加了羟基(―OH)、羧基(―COOH)等官能团,增加了MWNTs的亲水性,有利于的充分接触,并且这些基团中含氧配体提供电子给的空轨道而与发生配位作用,从而MWNTs吸附能力及吸附容量提高。
2.3 温度与反应时间的影响
考查了在30~50℃时,纯化和羧化MWNTs对铀吸附性能的影响。发现温度对2种MWNTs吸附性能影响不大,但在相同的温度下,羧化MWNTs的吸附容量较高。吸附时间的改变也会使材料对铀的吸附容量相应改变,其影响示于图5。由图5可见,纯化和羧化MWNTs对铀的吸附容量随吸附时间增加有平缓升高的趋势,吸附1h后,纯化MWNTs与羧化处理后的MWNTs均可基本达到吸附平衡,吸附量分别为38.60、60.18mg/g。为便于实验,选择震荡吸附时间为1h研究其它条件对吸附反应影响。
2.4 铀初始浓度的影响
研究了铀不同初始质量浓度对碳纳米管吸附性能的影响,结果示于图6。由图6可知,在一定温度下,随着溶液中UO2+2初始质量浓度的增加,纯化和羧化MWNTs吸附容量会增加,当溶液中的铀初始质量浓度达到400mg/L时,纯化和羧化MWNTs静态平衡吸附量分别为47.81mg/g和89.09mg/g。
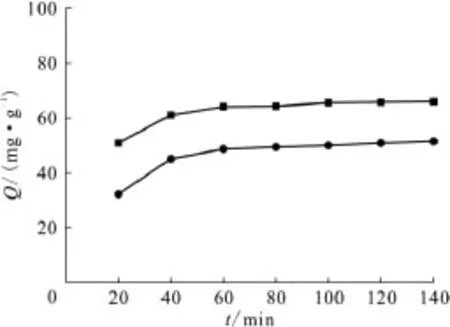
图5 吸附时间影响Fig.5 Influence of adsorption time on the adsorption of uranium ion ρ(UO+)=0.5g/L,θ=15℃,
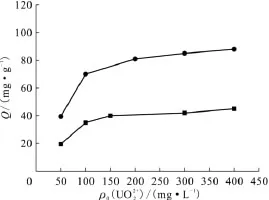
图6 不同初始质量浓度的UO+ 对吸附的影响Fig.6 Impact of different initial UO+mass concentration on the adsorption of uranium ion
2.5 等温吸附模型的研究
一定温度下,由单位吸附剂的吸附量与吸附质平衡浓度之间的变化规律而绘制的曲线称为吸附等温线。吸附等温线被广泛用来表征吸附系统的平衡状态,同时也是获得吸附剂结构、吸附热效应以及其他一些物理化学性能和工艺性能的信息源。纯化和羧化MWNTs的吸附等温线分别示于图7、图8。试验以Langmuir和Freundlich等温吸附方程拟合纯化和羧化MWNTs在最佳吸附介质中对铀的吸附过程:
Langmuir等温线模型:
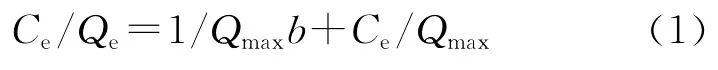
Freundlich等温线模型:


图7 288~308K纯化和羧化MWNTs Langmuir吸附等温线Fig.7 Langmuir adsorption isotherm of purified MWNTs and carboxylic MWNTs at 288-308K
将实验数据与Langmuir和Freundlich吸附等温线2种模型拟合,分别以Ce/Qe-Ce,lgQe-lgCe作图(图7,8),得出各相关系数[11-13],结果列入表1。比较2个等温线方程可知,在本研究的浓度范围内,Langmuir和Freundlich等温线模型都能较好地拟合纯化和羧化MWNTs在最佳吸附介质中对铀的吸附,体现了单层吸附与多层覆盖相结合的吸附模式。其中两种材料Kf值分别为51.50、35.64,说明铀容易被两种 MWNTs吸附。相较而言羧化比纯化MWNTs理论吸附容量更高,这主要是表面引入大量的含氧官能团增强静电斥力,促进其在水中的分散,形成稳定具有高效吸附性能的羧化MWNTs溶胶。
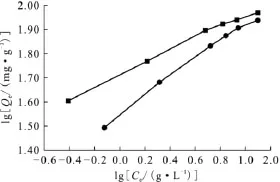
图8 288~308K纯化和羧化MWNTs Freundlich吸附等温线Fig.8 Freundlich adsorption isotherm of the purified MWNTs and carboxylated MWNTs at 288-308K

表1 羧化及纯化MWNTs吸附铀的Langmuir和Freundlich模型参数值Table 1 Values of Langmuir and Freundlich constants of the purified MWNTs and carboxylated MWNTs for reduction uranium(Ⅵ)ions
2.6 吸附热力学研究
研究不同温度纯化和羧化MWNTs对铀吸附以获得该吸附反应的热力学参数。根据方程lnkd=ΔS⊖/R-ΔH⊖/RT,其中kd是热力学稳定常数,根据公式(kd=吸附剂上铀/溶液中剩余铀)计算而来;ΔS⊖(J/(mol·K))和 ΔH⊖(kJ/(mol·K))分别是标准熵和标准焓,T(K)为温度,R(8.134J/(mol·K))是气体常数[14]。
温度对纯化和羧化MWNTs吸附铀的lnkd的影响示于图9。ΔG⊖可通过以下公式计算:ΔG⊖=ΔH⊖-TΔS⊖,结果列入表2。
从图9可以看出,1/T对lnkd作图均为直线,且线型相关性达0.99以上。从表2数据看出,ΔH⊖为正值说明该吸附反应为吸热过程,ΔS⊖正值表示吸附铀后体系混乱度增加,温度于298~328K时ΔG⊖均为负值表示该吸附反应能够自发的进行,说明纯化和羧化MWNTs都能很好的吸附铀,羧化 MWNTs的ΔG⊖值较纯化MWNTs值更小说明羧化MWNTs吸附铀反应更容易进行。

图9 温度对纯化和羧化MWNTs吸附铀的ln kd的影响Fig.9 Effect of temperature on the distribution coefficients of U on the purified MWNTs and carboxylated MWNTs 298~328K,m0(U)=50~200μg,
3 结 论
(1)通过热重、红外光谱实验表征发现约有质量比为10%的羧基成功接枝于羧化后MWNTs,出现羧基的特征红外波数为2 913cm-1及1 641cm-1。
(2)吸附铀实验表明,纯化和羧化MWNTs对铀具有较强的吸附作用,在pH=6.0时,两者最佳静态平衡吸附量分别为47.81mg/g和89.09mg/g。
(3)两种 MWNTs吸附铀的等温吸附模型都符合Freundlich模型,说明MWNTs对铀的吸附为多层覆盖吸附,吸附热力学研究表明,该吸附反应为吸热自发过程。研究表明,纳米材料在核素处理方面可能具有潜在的应用前景。

表2 不同温度下的吸附热力学参数Table 2 Thermodynamic parameters at different temprature
[1]Anke M,Seeber O,Müller R.Uranium Transfer in the Food Chian From Soil to Plants,Animals and Man[J].Chem der Erde-Geochemistry,2009,69:75-90.
[2]商照荣.贫化铀的环境污染影响及其对人体健康的危害[J].辐射防护,2005,25(1):56-61.
[3]夏良树,谭凯旋,王 孟.榕树叶-活性污泥协同曝气吸附铀的热力学[J].核化学与放射化学,2009,31(3):173-178.
[4]Guanghui W,Jinsheng L,Xuegang W.Adsorption of Uranium(Ⅵ)From Aqueous Solution Onto Cross-Linked Chitosan[J].J Hazard Mater,2009,168:1 053-1 058.
[5]Runping H,Weihua Z,Yi W.Removal of Uranium(Ⅵ)From Aqueous Solutions by Manganese Oxide Coated Zeolite:Discussion of Adsorption Isotherms and pH Effect[J].J Environ Radioact,2007,93:127-143.
[6]陆 宾,史宣艳.碳纳米管吸附水体中离子的研究进展[J].安徽化工,2009,35(5):8-10.
[7]曹德峰,刘宝春,葛海峰,等.碳纳米管吸附水体污染物的研究进展[J].广东化工,2008,35(6):54-57.
[8]蔡称心,陈 静,包建春,等.碳纳米管在分析化学中的应用[J].分析化学,2004,32(3):381-387.
[9]Fabiobelloni B.Can Carbon Nanotubes Play a Role in the Field of Nuclear Waste Management[J].Environ Sci Technol,2009,43:1 250-1 255.
[10]常 阳,张麟熹,罗明标.钛纳米管的制备与表征及吸附铀研究[J].材料研究学报,2010,24(4):424-428.
[11]Chegrouche S,Mellah A,Telmoune S.Removal of Lanthanum From Aqueous Solutions by Nature Benite[J].Water Res,1997,(31):1 733-1 737.
[12]Mellah A,Chegrouche S.The Removal of Zinc From Aqueous Solutions by Natural Bentonite[J].Water Res,1997,(31):621-629.
[13]Xiong L,Yang Y,Mai J X,et al.Adsorption Behavior of Methylene Blue Onto Titanate Nanotubes[J].Chem Eng J,2010,(156):313-320.
[14]Fu Q L,Deng Y L,Li H S,et al.Equilibrium,Kinetic and Thermodynamic Studies on the Adsorption of the Toxins of Bacillus Thuringiensis Subsp.Kurstaki by Clay Minerals[J].Appl Surf Sci,2009,(255):4 551-4 557.
Application of Purified and Carboxylic Multi-Walled Carbon Nanotubes for Uranium(Ⅵ)Ions Adsorptive Removal From Aqueous Solution
LIU Shu-juan1,2,LI Jin-ying1,LUO Ming-biao2,*,YANG Jia2,ZHANG Lin-xi2
1.China Institute of Atomic Energy,Beijing 102413,China;
2.Department of Applied Chemistry,East China Institute of Technology,Fuzhou 344000,China
Commercial multi-walled carbon nanotubes(MWNTs) were of purified and carboxylated,and characterized by thermogravimetric analysis(TGA)and infrared spectroscopy(IR).The two nanomaterials were applied for the adsorption of uranium ion.The effects of acidity,temperature,time,and uranium initial mass concentration of the solution on the adsorption capacity were studied.The results show the grafted carboxyl group account for 10%of the carboxylated MWNTs mass,and the specific surface of carboxylic MWNTs is higher than the purified MWNTs,and the characteristic absorption peakνasyn(1 641cm-1)of the carboxyl group is observed in the latter IR spectrum.In the pH value range of 3.0-6.0,the adsorption capacity of uranium on the two materials increases with the increase of the pH and equilibrium concentration,and is little influenced by reaction time and temperature.The adsorption isotherm and thermodynamic model of two materials were investigated.The results show that the adsorption can be described by with Freundlich and Langmuir equation,and the largest theoretic adsorption capacity are 47.81mg/g and 89.09mg/g,respectively.
multi-walled carbon nanotubes;characterization;adsorption uranium;adsorption model
O647.3
A
0253-9950(2011)05-285-06
2010-04-27;
2010-12-05
国防基础科研项目(A3420060146)
刘淑娟(1973—),女,陕西眉县人,博士研究生,核化学专业
*通讯联系人:罗明标(1963—),男,博士,教授,核化学与放射化学、环境分析化学专业
