以吲哚为燃料的微生物燃料电池降解和产电特性
2010-12-26张仁铎李明臣张翠萍刘广立中山大学环境科学与工程学院广东广州510275
罗 勇,张仁铎,李 婕,李明臣,张翠萍,刘广立 (中山大学环境科学与工程学院,广东 广州 510275)
以吲哚为燃料的微生物燃料电池降解和产电特性
罗 勇,张仁铎,李 婕,李明臣,张翠萍,刘广立*(中山大学环境科学与工程学院,广东 广州 510275)
以铁氰化钾为电子受体,在两极阴阳室内使用碳毛刷纤维为电极材料构建了循环式微生物燃料电池(MFC),研究了以吲哚为单一燃料和吲哚+葡萄糖为混合燃料条件下MFC的产电特性以及对吲哚和COD的去除效果.结果表明,以1000mg/L葡萄糖+250mg/L吲哚为混合燃料时,MFC的最高电压和最大功率密度分别为660mV和51.2W/m3(阳极),MFC运行10h对吲哚和COD的去除率分别为100%和89.5%;分别以 250,500mg/L吲哚为单一燃料时,MFC的平均最高电压分别为 115,118mV,最大功率密度分别为 2.1,2.3W/m3(阳极).在 MFC中,250,500mg/L吲哚被完全降解的时间分别为6,30h.MFC能够利用吲哚为燃料,在实现高效降解吲哚的同时对外产生电能,可用于处理含有毒且难降解有机物的焦化工业废水.
吲哚;微生物燃料电池;降解;产电性能
近年来,微生物燃料电池(MFC)由于可利用微生物为催化剂将废水中的有机物转化为电能,在污水处理领域受到广泛关注.目前,已报道能够被MFC利用作为燃料的有醋酸、多种单糖和食品加工废水、养猪废水和啤酒废水等[1-6].这些有机物大多易降解,而工业废水往往含有大量有毒且难降解的有机物,因此,研究 MFC处理此类有机物是决定其能否应用于实际废水处理的关键.
焦化工业废水成分复杂,含有大量的酚类化合物,含氮、硫、氧的杂环化合物,多环芳香族化合物、脂肪族化合物等有机污染物,是典型的含芳香族化合物及杂环化合物的废水[7].其中,吲哚、苯酚和吡啶是焦化废水中较为典型、有毒且难降解的含氮类杂环化合物[7-8],对人体和动物具有突变性和致癌性,对微生物活性产生一定抑制作用[9-10].尽管传统的厌氧和好氧生物法也能够降解这类物质,但能耗较高,且废水中巨大的有机能量得不到有效利用.利用MFC技术降解这类物质并产生电能是MFC处理废水的新思路[10-11].然而,吲哚能否作为燃料在MFC中实现降解和产电还尚未见报道.本研究通过构建连续式铁氰化钾阴极 MFC,研究吲哚作为单一燃料以及吲哚+葡萄糖共基质时产电和降解性能,旨在为MFC处理难降解有机物以及焦化废水提供依据.
1 材料与方法
1.1 试验装置
MFC反应器由有机玻璃制成,其形态和结构与张翠萍等[11]报道的类似.阴阳极之间采用质子交换膜(Nafion 212, Dupont Co., USA)隔开,阴极室和阳极室的体积均为 18mL.阴极采用50mmol/L铁氰化钾作为电子受体.阳极和阴极材料均为碳毛刷纤维,其长为7cm,宽为3.6cm.外电路通过导线与插入阴阳极的碳纤维相连而构成回路,外电阻为1000Ω.阳极液和阴极液可通过BT12200恒流泵 (上海琪特分析仪器有限公司)分别在阴阳室内循环流动,流速为 20mL/min. MFC输出电压由DT50数据采集卡每隔30s采集一次.MFC保持恒温(30 ± 1)℃.
1.2 MFC的接种与运行
取广州市猎德污水处理厂厌氧和好养污泥,并以1:1比例混合后,以其污泥上清液为接种液,接种液中的微生物经葡萄糖驯化2年后接种到MFC阳极中.此后,加入 1000mg/L葡萄糖作为燃料运行MFC,获得 2个稳定的电压输出周期后,采用1000mg/L 葡萄糖+250mg/L吲哚的混合基质作为MFC的燃料.再次获得2个稳定的产电周期后,使用250mg/L吲哚作为单一燃料来运行MFC.
MFC的阳极液除含有碳源(葡萄糖和吲哚)外,还包含无机盐溶液.每升无机盐包含以下成分:4.0896g Na2HPO4,2.544g NaH2PO4,0.31g NH4Cl, 0.13g KCl,12.5mL微量元素和 12.5mL维生素.每升维生素溶液由以下成分组成:2mg维生素H, 2mg维生素 B,2mg维生素 B6,0.1mg维生素B12,5mg核黄素,5mg 硫胺,5mg烟酸,5mg泛酸,5mg对氨基苯甲酸,5mg硫锌酸.当输出电压低于40mV时更换基质,通入氮气10min以保证阳极的厌氧状态,同时开始下一个周期的运行.
1.3 分析方法
每个周期内,定期采集水样测定葡萄糖、吲哚浓度和COD,测定前使用0.22μm的滤膜滤除微生物.吲哚的浓度采用Agilent 1100HPLC分析,流动相为甲醇∶水= 60∶40(体积比),流速1.0mL/min,色谱柱为 TC-C18反相柱(ODS, 250mm×4.6mm,5μm),柱温 40℃,测定波长为285nm.葡萄糖的测定采用蒽酮浓硫酸比色法[12]; COD采用标准分析方法[13].库仑效率(CE)按照式(1)计算[1]:

式中:M 为氧气的分子量,32 g/mol; ti为时间;Ui为 t时刻的电压;b为每摩尔氧气转移的电子数,4;V为反应器容积;R为外电阻;F为法拉第常数,96487C/mol;△S为COD的变化.
体积功率密度(PV, W/m3)计算如下:

式中:U为电压;I为电流;V为阳极室的有效体积,L;最大体积功率密度可通过PV= Pmax/V计算,其中Pmax为MFC可获得的最大功率(通过测定极化曲线可得到,单位为W).
扫描电镜(SEM)观察:在无菌操作台上剪下少量毛刷电极,使用磷酸盐缓冲液清洗2次后,用2.5%戊二醛固定,在 JSM-6330F扫描电镜(日本电子株式会社)下观察并拍照.
2 结果
2.1 以吲哚和葡萄糖为混合燃料时 MFC的产电特性
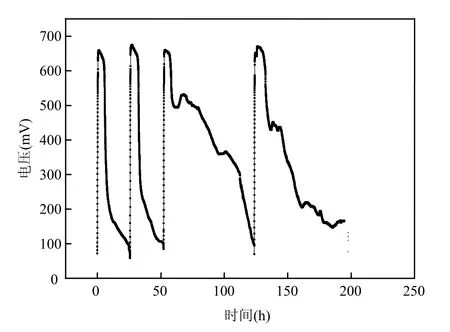
图1 以吲哚和葡萄糖为混合燃料时MFC的产电特性Fig.1 Electricity generation of the MFC using a mixture of indole + glucose as the fuel
由图1可见,以1000mg/L葡萄糖为单一燃料时,MFC的输出电压迅速升高,在3h内达到最大电压670mV,整个周期的运行时间为24h.稳定运行2个周期后,置换1000mg/L葡萄糖+250mg/L吲哚的混合燃料继续运行MFC,3h内MFC的最高电压仍然能达到660mV.这说明利用吲哚和葡萄糖共基质为燃料时,吲哚并没有抑制产电细菌的活性.而共基质时,MFC的产电周期的运行时间高达70h.
2.2 以吲哚为单一燃料时MFC的产电特性

图2 以吲哚为单一燃料时MFC的产电特性Fig.2 Electricity production of the MFC using indole as the sole fuel

图3 以吲哚为单一燃料时阳极生物膜表面扫描电镜照片Fig.3 SEM images of anode surface biofilm with indole as the sole fuel
当使用250mg/L吲哚为单一燃料运行MFC时,2个运行周期的最高电压分别为 115,117mV,运行时间分别为28,30h(图2).随后采用500mg/L吲哚来运行MFC,2个运行周期的最高电压分别为115,118mV,运行时间分别为32,28h(图2).扫描电镜分析表明(图3),此时阳极电极上覆盖了大量的微生物,主要以杆菌为主.
2.3 MFC对有机物的降解特性
由图4可以看出,MFC以吲哚和葡萄糖为混合燃料运行,第3h时,吲哚的去除率仅为20.8%,葡萄糖的去除率则高达88.4%;而第6h时吲哚的去除率为82%,而葡萄糖则已被完全消耗.周期结束时(第70h),COD的去除率可达到90.8%.

图4 利用混合燃料时MFC中有机物的降解效果Fig.4 Concentration and removal of various organic matters using a mixture of glucose and indole as the fuel in the MFC
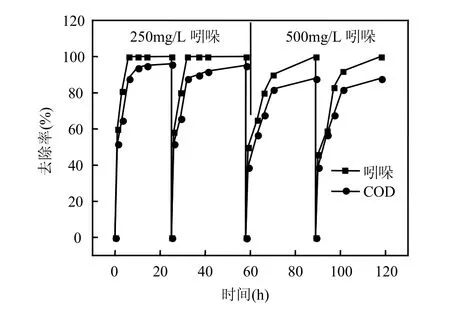
图5 以吲哚为单一燃料时MFC的降解特性Fig.5 Removal rate of indole and COD of the MFC using indole as the sole fuel
由图5可见,以250mg/L吲哚为单一燃料时,吲哚的去除率在不到 6h即达到 100%,而此时COD去除率为 88%,周期结束时(约第 22h)的COD去除率为95%.当吲哚浓度提升至500mg/L时,第6h时MFC对吲哚和COD的去除率分别为62%和57%,而第30h时,对吲哚和COD的去除率分别为100%和88%.
3 讨论
本研究中,以1000mg/L葡萄糖和1000mg/L葡萄糖+250mg/L吲哚为燃料时,MFC的最大功率密度分别为 43,51.2W/m3;而以 250mg/L吲哚为单一燃料时,MFC的最大功率密度仅为2.1W/m3.这说明单一燃料吲哚会限制产电细菌的活性,从而导致了 MFC的产电性能下降,这与Zhang等[14]关于吡啶限制产电的报道类似.
对比葡萄糖燃料和混合燃料的产电曲线(图1)可以看出,混合燃料的产电曲线出现了明显的“拖尾现象”(产电周期延长).以 250mg/L吲哚为单一燃料时,第3h吲哚的去除率为81%(图5);以1000mg/L葡萄糖和250mg/L吲哚为混合燃料时,第3h吲哚的去除率仅为20.8%,而此时葡萄糖的去除率则高达88.5%(图4).这说明产电细菌优先利用易降解的葡萄糖,待葡萄糖快耗尽时,再利用难降解的吲哚进行产电,因此产电曲线出现了明显的“拖尾现象”.
Ren等[15]利用白腐菌降解吲哚,200mg/L吲哚被完全降解需要 216h.Katapodis等[16]使用嗜热菌 Sporotrichum thermophile降解吲哚, 1000mg/L吲哚被完全降解需要 6d.本研究 250, 500mg/L吲哚被MFC完全降解分别仅需6,30h.可能有以下几方面的因素导致MFC对吲哚的快速降解,首先,本研究取自污水处理厂厌氧和好养池的混合菌种经过长达2年的驯化,具有良好的降解性能,这些菌种已被证明能高效降解难生物降解的有机物苯酚和吡啶[14,17];其次,相比于传统的碳纸电极,本研究采用的毛刷电极具有更大的比表面积,能够吸附更多的微生物,从而提升了MFC的降解性能[18-19];另外,有学者证明MFC运行(产电周期内)时的降解效率比开路状态高10%~ 20%[17].
Zhang等[14]发现,MFC阳极中降解吡啶的菌种可能是杆菌,本研究阳极电极上的菌种也以杆菌为主(图3),这说明降解吲哚的菌种也可能是杆菌.利用高效液相色谱对 MFC运行周期的阳极室的溶液成分进行分析,结果表明,吲哚降解过程中有低浓度的中间产物出现,这些中间产物也可能被微生物利用来产电,但具体的情况仍有待进一步证实.
值得注意的是,以250mg/L吲哚为单一燃料时MFC的库仑效率仅为0.7%.较低的库仑效率主要由2个原因造成:吲哚是难降解有机物,微生物代谢吲哚的速度较葡萄糖等可生化性较好的有机物慢,故电子产生和转移速度慢[20];本研究中采用的循环式MFC的连接瓶中存在着大量包括产甲烷菌在内的非产电菌,这些菌种会消耗掉大部分的COD,这也导致了库仑效率的下降.
本研究中,虽然MFC能够有效地降解高浓度的吲哚,然而从吲哚中仅能够回收有限的能源.在今后的研究中,可通过改变反应器结构和电极材料来有效地提高库仑效率和功率输出.
4 结论
4.1 MFC能够以吲哚为单一燃料以及葡萄糖+吲哚为混合燃料实现对外电路的输出.以 250, 500mg/L吲哚为单一燃料时MFC的平均最高电压分别为 115,118mV,平均周期运行时间分别为27,30h,库仑效率分别为 0.7%和 0.4%;以1000mg/L葡萄糖+250mg/L吲哚为混合燃料时,最高输出电压和最大功率密度分别为 660mV, 51.2W/m3,库仑效率为 2.9%,周期运行时间高达70h.
4.2 MFC 也可实现对吲哚的高效降解.以1000mg/L葡萄糖+250mg/L吲哚为燃料时,运行周期内第 10h时吲哚和葡萄糖的去除率均为100%;而以250mg/L吲哚和500mg/L吲哚为单一燃料时,MFC完全降解吲哚分别需要6,30h.
[1] Liu H, Logan B E. Electricity generation from an air-cathode single chamber microbial fuel cell in the presence and absence of a proton exchange membrane [J]. Environmental Science and Technology, 2004,38(14):4040-4046.
[2] Catal T, Fan Y, Li K, et al. Effects on furan derivatives and phenolic compounds on electricity generation in microbial fuel cells [J]. Journal of Power Sources, 2008,18(1):162-166.
[3] Oh S E, Logan B E. Hydrogen and electricity generation from a food processing wastewater using fermentation and microbial fuel cell technology [J]. Water Research, 2005,39(19):4673-4682.
[4] Min B, Kim J R, Oh S E, et al. Electricity generation from swine wastewater using microbial fuel cells [J]. Water Research, 2005, 39(20):4961-4968.
[5] Feng Y, Wang X, Logan B E. Brewery wastewater treatment using air-cathode microbial fuel cells [J]. Applied Microbial and Biotechnology, 2008,78(5):873-880.
[6] 孙寓姣,左剑恶,崔龙涛,等.不同废水基质条件下微生物燃料电池中细菌群落解析 [J]. 中国环境科学, 2008,28(12):1068-1073.
[7] 李咏梅,顾国雄,赵建夫.焦化废水中几种含氮杂环有机物在A1-A2-O系统中的降解特性研究 [J]. 环境科学学报, 2002, 22(1):34-39.
[8] Lu Y, Yan L, Wang Y, et al. Biodegradation of phenolic compounds from coking wastewater by immobilized white rot fungus Phanerochaete chrysosporium [J]. Journal of Hazardous Materials, 2009,165(1):1091-1097.
[9] Merabet S, Robert D, Weber J V, et al. Photocatalytic degradation of indole in UV/TiO2: optimization and modelling using the response surface methodology (RSM) [J]. Environmental Chemistry Letters, 2009,7(1):45-49.
[10] 骆海萍,刘广立,张仁铎,等.高浓度苯酚的MFC降解及产电性能[J]. 环境科学学报, 2008,28(11):2181-2185.
[11] 张翠萍,王志强,刘广立,等.降解喹啉的微生物燃料电池的产电特性研究 [J]. 环境科学学报, 2009,29(4):740-746.
[12] Raunkjaer K, Hvitved T, Neilsen P H. Measurement of pools of protein, carbohydrate and lipids in domestic wastewater [J]. Water Science and Technology, 1994,28(1):251-262.
[13] Clesceri L S, Greenberg A E, Eaton A D. Standard methods for the examination of water and wastewater, [M]. 20th ed. Washington, D C: American Public Health Association, 1998.
[14] Zhang C, Li M, Liu G, et al. Pyridine degradation in the microbial fuel cells [J]. Journal of Hazardous Materials, 2009,172(1):465-471.
[15] Ren D, Zhang D, Yan K, et al. Studies on the degradation of indole using white rot fungus [J]. Fresenius Environmental Bulletin, 2006,15(10):1238-1243.
[16] Katapodis P, Moukouli M, Christakopoulos P, et al. Biodegradation of indole at high concentration by persolvent fermentation with the thermophilic fungus Sporotrichum thermophile [J]. International Biodeterioration and Biodegradation, 2007,60(4):267-272.
[17] Luo H, Liu G, Zhang R, et al. Phenol degradation in microbial fuel cells [J]. Chemical Engineering Journal, 2009,147(2):259-265.
[18] Luo Y, Liu G, Zhang R, et al. Power generation from furfural using the microbial fuel cell [J]. Journal of Power Sources, 2010, 195(1):190-194.
[19] Logan B, Cheng S, Waston V, et al. Graphite fiber brush anodes for increased power production in air-cathode microbial fuel cells [J]. Environmental Science and Technology, 2007,41(9):3341-3346.
[20] 叶晔捷,宋天顺,徐 源.用高浓度对苯二甲酸溶液产电的微生物燃料电池 [J]. 环境科学, 2009,30(4):1221-1226.
Electricity generation from indole degradation using the microbial fuel cell.
LUO Yong, ZHANG Ren- duo, LI Jie, LI Min-chen, ZHANG Cui-ping, LIU Guang-li*(School of Environmental Science and Engineering, Sun Yat-sen University, Guangzhou 510275, China). China Environmental Science, 2010,30(6):770~774
A sequential microbial fuel cell (MFC) was constructed to investigate indole degradation and simultaneous electricity generation using indole and a mixture of indole + glucose as the fuel. When 250mg/L indole and 500mg/L indole were used as the fuels in the MFC, the maximum voltage outputs were 115,118mV, respectively, and the corresponding average removal efficiencies of indole were 100% and 62%. Moreover, 250mg /L and 500mg/L indole were removed completely in the MFC within 6, 30h. When a mixture of 1000 mg/L glucose + 250mg/L indole was used as the fuel, the maximum power density was 51.2W/m3in the MFC. Within 10 h, the averaged removal rates of indole and COD in the MFC were 100% and 89.5%, respectively. The MFC could enhance biodegradation of recalcitrant contaminants such as indole in practical applications of wastewater treatment.
indole;microbial fuel cell;degradation;electricity generation
2009-11-27
国家自然科学基金资助项目(50608070);清华大学环境模拟与污染控制国家重点联合实验室专项基金(08K02ESPCT)
* 责任作者, 副教授, liugl@mail.sysu.edu.cn
X703.5
A
1000-6923(2010)06-0770-05
罗 勇(1982-),男,江西南昌人,中山大学环境学院博士研究生,主要研究方向为微生物燃料电池和污水资源化.发表论文 4篇.
