驻极体美洛昔康贴剂对大鼠血液和肝脏组织中药物浓度的影响
2010-12-09肖永恒江键李国栋王冬涂晔马琳梁媛媛崔黎丽
肖永恒,江键,李国栋,王冬,涂晔,马琳,梁媛媛,崔黎丽
(1.第二军医大学药学院,上海 200433;2.第二军医大学基础部,上海 200433)
驻极体美洛昔康贴剂对大鼠血液和肝脏组织中药物浓度的影响
肖永恒1,江键2,李国栋1,王冬1,涂晔1,马琳2,梁媛媛2,崔黎丽1
(1.第二军医大学药学院,上海 200433;2.第二军医大学基础部,上海 200433)
利用药剂学方法和栅控恒压电晕充电技术制备驻极体美洛昔康贴剂,考察驻极体美洛昔康贴剂经皮给药24 h内,美洛昔康在SD大鼠血液和肝脏组织中浓度的变化,探讨负极性驻极体对美洛昔康的透皮促渗效果.实验结果表明经皮给药24 h内,-2 000 V驻极体对美洛昔康的透皮促渗效果不明显;-1 200 V驻极体对美洛昔康的透皮吸收有明显的促渗作用,且促渗倍数为对照组4倍.
经皮给药;驻极体;美洛昔康;血药浓度;肝脏组织
透皮给药系统是药剂学中一个新兴的领域,由于其独特的优点而一直受到许多学者的关注.它给药量相对较少,能减少副作用,而且可以实现缓控释给药[1].但是,皮肤角质层的天然屏障作用一直是药物透皮吸收的最大阻碍.药物主要是通过角化细胞周围的脂质通道穿过角质层的[2],这样就使得许多亲水性的和分子量相对较大的化合物不能通过角质层或者是透过量达不到治疗浓度.因此,寻找促进药物透过皮肤的方法已成为研发透皮给药系统的关键.
驻极体是指能够长期储存空间电荷和偶极电荷的电介质材料,驻极体技术是利用驻极体产生的持续稳定的静电场和微电流在皮肤角质层脂质双分子层间形成暂时可逆的通道及拓宽毛囊孔径来实现增加药物通透量的一种经皮给药促渗方法.本文以聚丙烯膜为驻极体制备材料,美洛昔康为模型药物,通过SD大鼠的在体透皮实验,从药物动力学方面研究负极性驻极体对药物的透皮促渗效果.
1 材料和方法
1.1 主要试剂及器材
压敏胶Eudragit E100,德国Röhm公司;美洛昔康原料药,上海康明高科技有限公司;其他试剂均为色谱纯、优级纯或分析纯;栅控电晕充电系统(大连理工大学静电与特种电研究所);EST102表面电位计(中国劳动保护研究所);氮气吹扫仪(杭州奥盛仪器有限公司);高效液相色谱仪(日本岛津公司).
1.2 材料及实验动物
聚丙烯(Po lyp ropylene,PP),日本东丽株式会社;SD大鼠,雄性,(200±10)g,第二军医大学实验动物中心提供.
1.3 驻极体美洛昔康贴剂的制备
将一定量Eudragit E100用丙酮溶解,加入柠檬酸三丁酯,溶解后加入美洛昔康,混合均匀后涂布于5 cm×6.5 cm的PP膜(背衬面)上制成美洛昔康贴剂.用栅控电晕充电系统制备-2 000 V和-1 200 V聚丙烯驻极体,将PP驻极体充电面与美洛昔康贴剂背衬层复合制成驻极体美洛昔康贴剂.
1.4 血浆和肝组织样品的处理
1.4.1 血浆样品处理
取大鼠血浆500μL置于10 m L塑料离心管中,加入吡罗西康标准溶液(20μg/m L)30μL和盐酸(2.4 mol/L)200μL,涡旋30 s,加入6 m L乙酸乙酯涡旋3 min,于6 000 r/min离心6 min,取上清液5 m L于氮气流下60℃水浴吹干,残留物用150μL流动相复溶,于12 000 r/min离心10 min后取上清液进样分析[3].
1.4.2 肝组织样品处理
精密称取大鼠肝组织,加入0.1 mo l/L氢氧化钠溶液,高速匀浆3 min,取匀浆液500μL置于10 m L塑料离心管中,同上1.4.1血浆样品处理[4].
1.5 体内透皮实验
SD大鼠108只,随机分成9个取样组(1,2,4,6,8,10,12,18,24 h).每组12只大鼠按体重大小配对,每对经麻醉、固定、剃须刀腹部去毛后分别贴上美洛昔康贴剂(对照组)和-1 200 V驻极体美洛昔康贴剂(-1 200 V实验组)及-2 000 V驻极体美洛昔康贴剂(-2 000 V实验组),然后分别于以上时间点定时取样.眼眶静脉丛取血于甘素化试管,3 000g离心10 min取上清血浆500μL;同时取肝组织2.0 g,加入氢氧化钠溶液(0.1 mo l/L)4 m L,高速匀浆3 min,取匀浆液500μL.血浆和肝组织匀浆液按“血浆样品处理”项进行相同处理.
2 结果与讨论
2.1 血浆和肝脏组织中药物含量随时间的变化
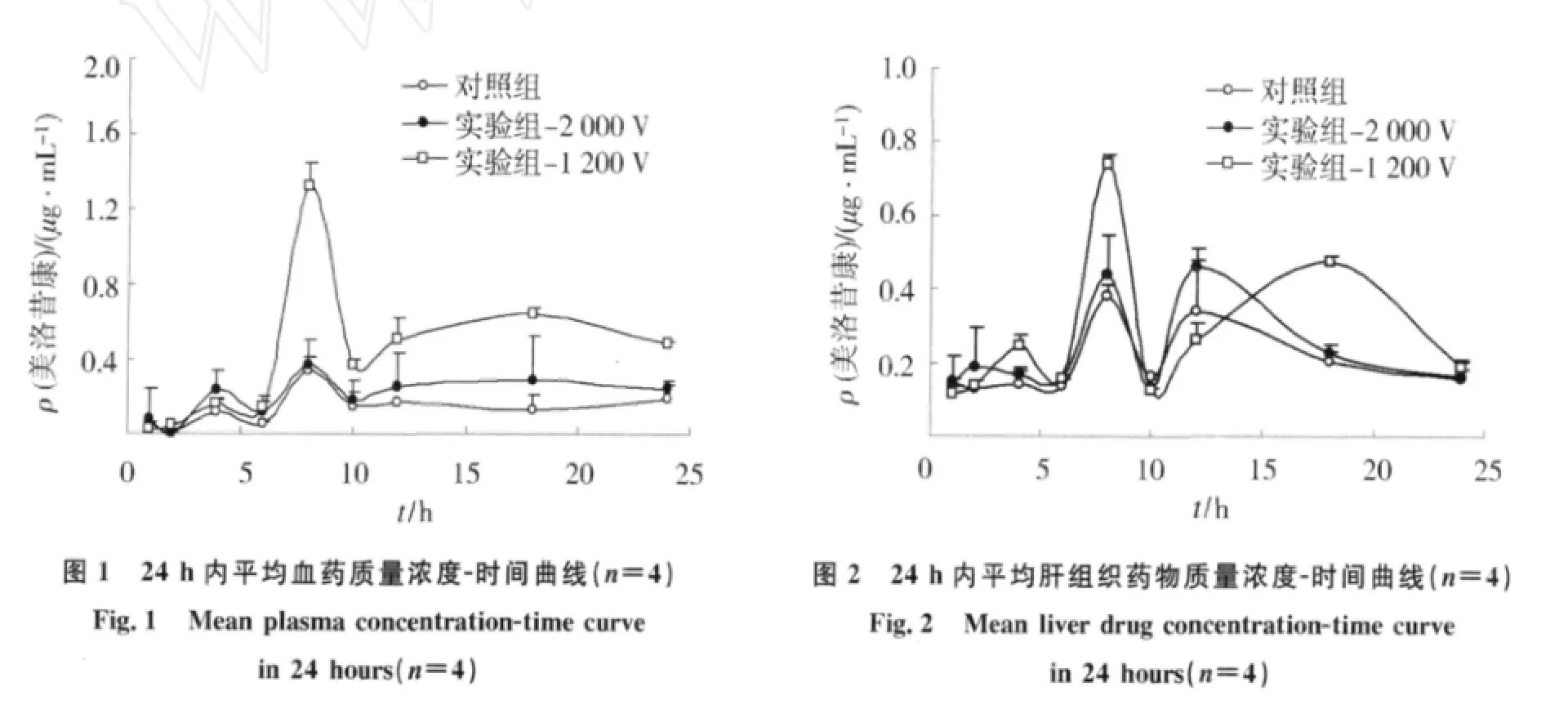
图1为对照组、-1 200 V实验组和-2 000 V实验组经皮给药24 h内美洛昔康在大鼠血浆中的浓度随时间变化的曲线.由图可见,对照组、-1 200 V实验组和-2 000 V实验组血药浓度随时间的变化规律相似,曲线分别在4 h和8 h出现2个峰值,并在8 h达到最大血药浓度,从8 h到24 h,血药浓度趋于平稳.这是因为在经皮给药的起始阶段,贴剂中药物的释放占主导地位,药物由贴剂向角质层以较快的速度扩散.随着药物扩散时间的持续,药物由角质层向下层组织扩散的速度也逐渐增加,但是药物由贴剂向角质层中的扩散速度远大于药物由角质层向下层组织的扩散速度,因此,总体效果是药物在皮肤角质层中的量增加较快,血药质量浓度增加相对较慢,且在4 h达到1个峰值.随着作用时间的延长,药物由于浓度差所造成的释放动力逐渐减小,角质层中药物的量达到极大值,此时,由于皮肤血液循环的“漏槽”效应,药物由角质层向下层组织的扩散速度远大于药物由贴剂向角质层中的扩散速度,因此,4 h后药物在角质层中的含量不断减少,血药质量浓度快速上升,并在8 h时达到最大峰值;从8 h到24 h,贴剂和角质层“储库”中药量不断减少,“漏槽”效应减弱,药物的扩散速率趋于平稳,因此血药质量浓度也趋于平稳.
图1结果还表明,-2 000 V实验组血药质量浓度略高于对照组的,但差异没有统计学意义;-1 200 V实验组血药质量浓度明显高于对照组和-2 000 V实验组的,且差异均有统计学意义.这是由于-1 200 V驻极体能够较持久地打开角质层紧密排列结构,增加其膜脂的流动性,并形成微细易于通透的流动性孔道,使得药物快速进入角质层,并通过角质层进入活性表皮及真皮层,经由毛细血管进入体循环,达到较高的血药质量浓度水平.而-2 000 V驻极体的高表面电位和高密度电荷能在短时间内更大程度地影响角质层的紧密排列,并形成孔道使大量药物扩散进入角质层,但是这种皮肤结构的改变是短暂的,随着作用时间的增加,皮肤结构趋于正常排列,药物的扩散主要由美洛昔康的扩散决定.
图2给出了对照组、-1 200 V实验组和-2 000 V实验组在经透皮给药24 h内大鼠肝脏组织中美洛昔康含量随时间的变化曲线.肝组织中药物质量浓度随着血药质量浓度的变化而变化,也表现出同样的变化趋势.这是因为美洛昔康进入体循环后,绝大部分与血浆蛋白结合,然后主要经肝脏代谢排出体外.
2.2 峰值(8 h)浓度比较
图3给出了对照组、-1 200 V实验组和-2 000 V实验组血药浓度和肝组织药物浓度分别在峰值(8 h)时的比较,概率p<0.05为显著性差异.8 h时,-1 200 V组血药浓度明显高于对照组和-2 000 V组的,且约为对照组的4倍;肝组织药物质量浓度表现出同样的统计结果.根据体外透皮实验结果[5]:1)负极性驻极体较正极性的对美洛昔康有更显著性的透皮促渗作用;2)在0至-1 200 V的电压范围内负极性驻极体对美洛昔康的促渗作用与驻极体的表面电位呈正相关性.综合体内外实验结果表明,-1 200 V较-2 000 V驻极体具有更显著的促进美洛昔康透皮吸收的作用.驻极体所产生的静电场和微电流能引起皮肤角质层超微结构的改变并形成新的可逆性的孔道,同时还能增强角质层细胞膜脂的流动性,从而增加药物的经皮通透性.而且,不同极性驻极体对药物的经皮吸收促进作用与药物的极性有着密切的关系.美洛昔康是一个弱酸性的小分子化合物,在中性和偏碱性的环境中极易失去一个质子变成一个负离子,负极性驻极体在改变大鼠皮肤角质层微结构的同时还对药物产生了一定的推动作用,这种推动作用有利于药物从贴剂基质中释放.当驻极体的表面电位较低时,负极性驻极体对美洛昔康的推动作用在促渗作用中占主导地位,这种推动作用随着表面电位的升高而增强;当驻极体的表面电位达到一定值(-1 200 V)时,可逆性的孔道和膜脂的流动性占据了主导地位,成为负极性驻极体促进美洛昔康经皮转运的主要因素.因此,-1 200 V驻极体能更好地促进美洛昔康透过皮肤角质层进入血液循环,并达到较高的血药浓度,起到良好的全身治疗作用.
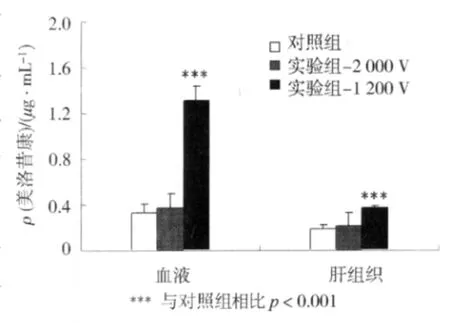
图3 峰值质量浓度比较Fig.3 Com parison of peak value
3 结论
不管从治疗水平(血药质量浓度)角度,还是从代谢(肝组织药物质量浓度)角度,-1 200 V驻极体较-2 000 V驻极体对美洛昔康的经皮渗透有更显著性的促进作用.此外,-1 200 V驻极体美洛昔康贴剂作用时,大鼠血药质量浓度和肝组织药物质量浓度变化整体都较口服制剂的平稳,药物在体内的循环时间延长,有效血药质量浓度维持时间较长,达到类似缓释制剂的作用.
[1]MARK R P,ROBERT L.Transdermal drug delivery[J].Nature Biotec,2008,26(Supp l):1261-1268.
[2]郑俊民.经皮给药新剂型[M].北京:人民卫生出版社,2006.
[3]BAEJW,KIM M J,JANGC G,et al.Determination of meloxicam in human p lasma using a HPLCmethod w ith UV detection and its app lication to a pharmacokinetic study[J].J Chromatogr B,2007,859:69-73.
[4]夏运岳,潘建新,顾振纶.美洛昔康在大鼠体内的药代动力学研究[J].中国药理学通报,2001,17(2):236-237.
[5]JIANG Jian,KONG Yuxiu,CHENGLiang,et al.Effect of electret on transdermal permeation of meloxicam from a patch fo rmulation[Z].The Proceedingsof the 6th International Conference on App lied Electrostatics,Shanghai,2008.
Effect of Electret Meloxicam Patch on the Drug Concentration in Plasma and Liver of SD Rats
XIAO Yong-heng1,JIANGJian2,LIGuo-dong1, WANGDong1,TU Ye1,MA Lin2,LIANG Yuan-yuan2,CUILi-li1
(1.Schoo l of Pharmacy,Second M ilitary M edical U niversity,Shanghai 200433,China; 2.Department of Physics and Mathematics,College of Basic Medical Sciences,Second M ilitary M edical University,Shanghai 200433,China)
PP electret meloxicam patches w ere p repared by the co rona charging and pharmaceutical method to study the concentration changes of d rug in p lasma and liver tissue w ithin 24h after transdermal administration,and to investigate the enhancement of negative electret on transdermal abso rp tion of meloxicam.The results indicated that-1 200 V electret had a remarkable enhancing effect on percutaneous abso rp tion of meloxicam w ith the enhancing ratio of 4,but-2 000 V electret showed no obvious enhancement on meloxicam transdermal abso rp tion.Therefore,-1 200 had much better enhancing effect on meloxicam transdermal abso rp tion as compared w ith-2 000 V electret.
transdermal administration;electret;meloxicam;p lasma concentration;liver tissue
O 484
A
1000-1565(2010)05-0560-04
2010-04-20
国家自然科学基金资助项目(50577066;50977089);军队"十一五"国际合作项目(06H 022)
肖永恒(1984-),男,湖北武汉人,第二军医大学在读硕士研究生.
崔黎丽(1961—),女,河北盐山人,第二军医大学教授,硕士生导师,主要从事物理药剂学方向研究.
(责任编辑:梁俊红)
