葡萄糖/天冬酰氨模拟体系丙烯酰胺形成
2010-12-05章银良白明星
章银良,白明星
(郑州轻工业学院食品与生物工程学院,河南 郑州 450002)
葡萄糖/天冬酰氨模拟体系丙烯酰胺形成
章银良,白明星
(郑州轻工业学院食品与生物工程学院,河南 郑州 450002)
采用葡萄糖与天冬酰氨的模拟体系来研究反应条件对丙烯酰胺的产生的影响。以色度、198 nm下紫外吸光度和丙烯酰胺含量为指标,考察反应温度、时间、初始pH值和摩尔配比对丙烯酰胺形成的影响。结果表明反应温度是影响丙烯酰胺形成关键因素,葡萄糖比天冬酰胺对模拟体系的丙烯酰胺形成影响要大,初始pH值在8时,丙烯酰胺形成最大。
丙烯酰胺;美拉德反应;模拟体系;天冬酰胺
热加工是食品加工最普遍和广泛作用的一种加工方法,如高温杀菌、油炸等。2002年4月,瑞典斯德哥尔摩大学Tornquist等通过检测发现,一些普通食品在经过煎、炸、烤等高温加工处理时会产生丙烯酰胺,而且其含量随加工温度的升高而升高。油炸食品中丙烯酰胺含量一般在1000 μg/kg以上,炸透的薯片达12800 μg/kg。由于丙烯酰胺在动物试验中表现出致癌活性,因此食品中存在丙烯酰胺的问题引起了全球的关注。丙烯酰胺对人和动物是一种有效累积性神经毒物[1],可通过皮肤、口腔或呼吸道而进入生物体内,一旦进入人体内,它可以快速分布全身的组织中,环氧丙酰胺和环氧化合物是其代谢产物,它们与DNA加合形成加合物[2]。丙烯酰胺和蛋白质的巯基结合形成N-2甲氨酰乙基加合物,从而产生其毒性和危害性[3]。一些试验已经发现丙烯酰胺会导致哺乳动物细胞基因变异和染色体异常。1994年国际癌研究协会(IARC)将丙烯酰胺归为可能使人致癌[4]。
目前,通过研究,对富含淀粉类的食品在油炸过程中产生丙烯酰胺的机理有了初步的了解。英国与瑞士雀巢研究中心的研究小组首次在〈Nature〉上发表了丙烯酰胺产生机理的文章,初步揭示了丙烯酰胺产生的机理[5]。美拉德反应在丙烯酰胺的形成方面起关键作用。美拉德反应是由还原糖和氨基酸或蛋白质中的自由氨基在高温条件下所发生的一系列复杂的化学反应,是热加工食品中风味和色泽产生的重要途径之一。在参与美拉德反应的各种氨基酸中,天冬酰胺是食品中产生丙烯酰胺的重要途径之一,还原糖和氨基酸—天冬酰胺提供了丙烯酰胺的分子骨架[6-8]。
采用葡萄糖与天冬酰氨的模拟体系来研究反应条件对丙烯酰胺的产生的影响,为热加工食品减少丙烯酰胺形成和食用安全提供技术基础。
1 材料、方法和设备
1.1 试剂
柠檬酸、葡萄糖、丙烯酰胺(含量>99%):天津科密欧化学试剂有限公司。L-天冬酰胺(生化试剂、纯度>98.5%)、以上未标明试剂均为分析纯(AR)。
1.2 设备
HH-1智能型数显恒温油浴槽:金坛市正基仪器有限公司;WSC-S测色色差计:上海精密科学仪器有限公司;UV-2102pc紫外可见分光光度计:尤尼柯(上海)仪器有限公司;电子天平JA1203:上海越平科学仪器有限公司;GC-MS 6850-6793:安捷伦公司。
1.3 方法
1.3.1 不同反应温度对模拟体系的影响
准确称取葡萄糖0.1200 g和天冬酰胺0.1000 g(物质的量比1∶1),加入20 mL蒸馏水,放入密封试管中, 再置于油浴锅中,分别于温度 100、120、140、160、180℃下反应30 min,确定不同反应温度对模拟体系中丙烯酰胺产生及各相关指标的影响,每个重复3次。
1.3.2 不同反应时间对模拟体系的影响
准确称取葡萄糖0.1200 g和天冬酰胺0.1000 g(物质的量比1∶1),加入20 mL蒸馏水,放入密封试管中,置于160℃油浴锅中反应,分别反应10min、20min、30 min、1 h、1.5 h,确定不同反应时间对模拟体系中丙烯酰胺产生及各相关指标的影响,每个重复3次。
1.3.3 不同物质的量比对模拟体系的影响
准确称取葡萄糖 0.3600、0.2400、0.1200、0.0600、0.0400 g和天冬酰胺0.1000 g使葡萄糖:天冬酰胺的物质的量比分别为 3∶1、2∶1、1∶1、1∶2∶1∶3,分别加入20 mL蒸馏水,放入密封试管中,再置于160℃油浴锅中反应30 min,确定不同的物质的量比对丙烯酰胺形成及相关指标的影响,每个重复3次。
1.3.4 pH对模拟体系的影响
准确称取葡萄糖0.1200g和天冬酰胺0.1000g(物质的量比1∶1),加入20mL蒸馏水,调整pH值,使其pH分别为 4.0、5.0、6.0、7.0、8.0、9.0 然后放入密封试管中,置于160℃油浴锅中反应30min,确定pH时间对模拟体系中丙烯酰胺产生及各相关指标的影响,每个重复3次。
1.3.5 反应物色度的测定
对每次的反应物取其中5 mL,然后测其L*、a*、b*值,重复3次,取其平均值。
1.3.6 反应产物中丙烯酰胺含量的检测
食品中丙烯酰胺含量的测定方法气相色谱-质谱(GC-MS)法(GB/T 5009.204-2005)[9]。
2 结果与讨论
2.1 反应温度对葡萄糖/天冬酰胺模拟体系的影响
反应温度对模拟体系的色泽和紫外吸收的影响见表1,反应温度对丙烯酰胺形成的影响见图1。

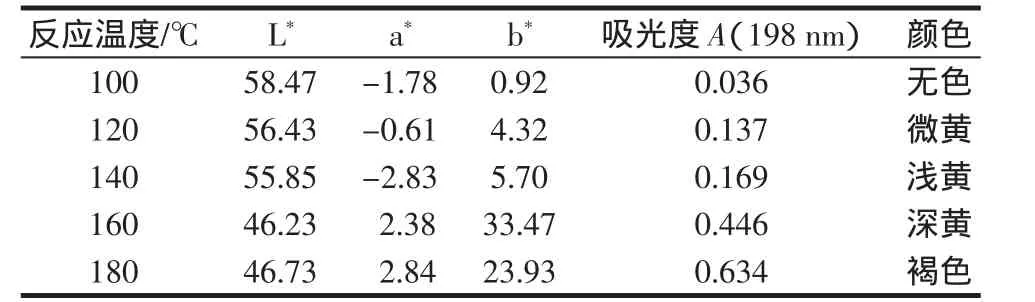
表1 反应温度对模拟体系色泽和紫外吸收的影响Table1 Effects of temperature on the color and UV absorption of model system
本文采用L*a*b*色空间表示模拟体系的颜色变化。在L*a*b*空间中,L*是溶液颜色的亮度,a*、b*是色方向,其中a*为红色方向、-a*为绿色方向、b*为黄色方向、-b*为蓝色方向。从表1可以看出,随着反应温度的升高,溶液颜色的亮度越来越小,a*值由绿色转变为红色方向,b*值向黄色方向发展,所以总体颜色是从无色慢慢变成为180℃时深褐色,表明了美拉德反应速度由低向高发展。从198 nm紫外吸收可以看出,吸光度越来越大,表明丙烯酰胺生成与温度成正相关性[10]。从图1可以看出,随着模拟体系反应温度的提高,丙烯酰胺含量从100℃的0含量慢慢升高,从140℃开始快速升高到180℃已经达到了3.6 mg/kg,说明反应温度是丙烯酰胺生成的关键因素。
2.2 反应时间对葡萄糖/天冬酰胺模拟体系的影响
反应时间对模拟体系的色泽和紫外吸收的影响见表2,反应时间对丙烯酰胺形成的影响见图2。

表2 不同反应时间对模拟体系色泽和紫外吸收的影响Table2 Effects of reaction time on the color and UV absorption of model system
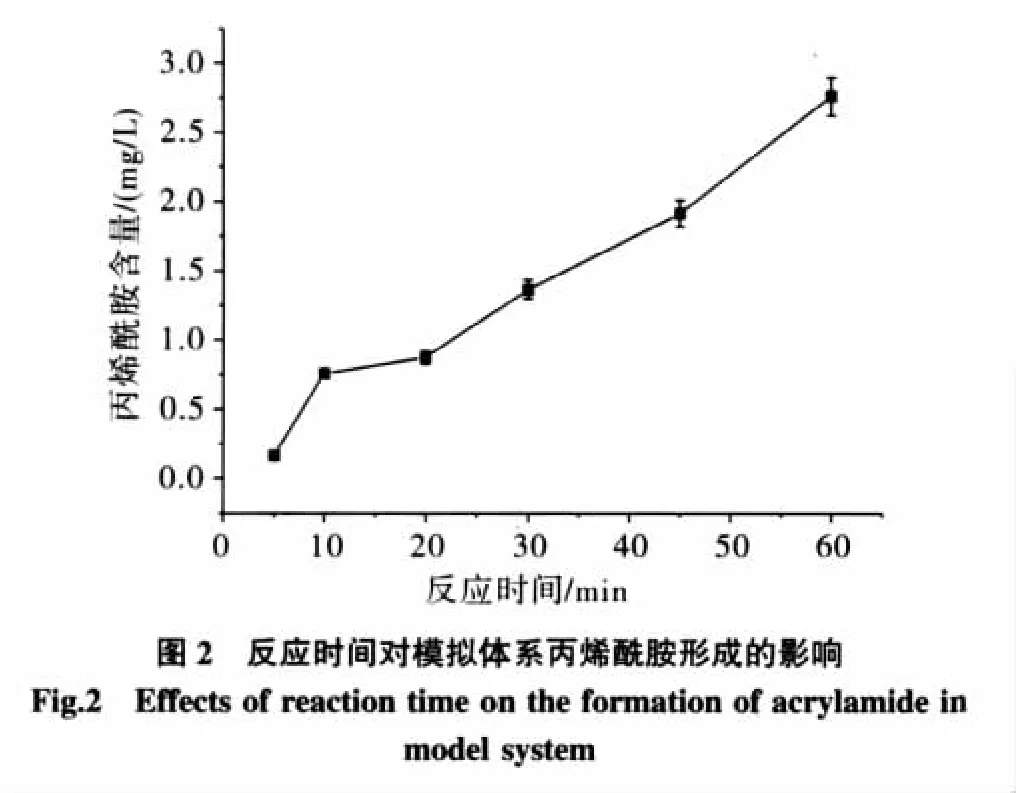
从表2可知,随着反应时间的延长,溶液颜色的亮度越来越小,a*值由绿色转变为红色方向,b*值向黄色方向发展,所以总体颜色是从无色逐渐变成浅黄、橙黄、褐色、深褐色,表明了美拉德反应速度随着时间延长由慢向快发展。从198 nm紫外吸收可以看出,吸光度越来越大,表明丙烯酰胺生成与时间成正相关性。从图2可以看出,在160℃下模拟体系发生美拉德反应,随着时间的延长,丙烯酰胺含量几乎与时间成线性相关,时间越长,丙烯酰胺含量越高,所以在模拟体系中,当温度在140℃以上时,反应时间也是比较重要影响因素。
2.3 初始pH值对葡萄糖/天冬酰胺模拟体系的影响
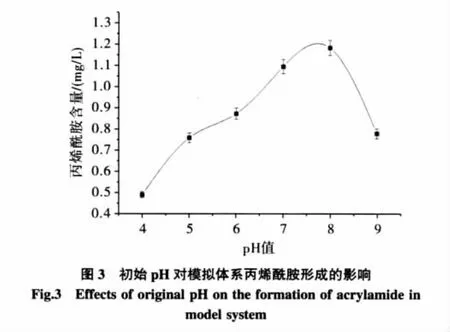
初始pH值对模拟体系的色泽和紫外吸收的影响见表3,初始pH值对丙烯酰胺形成的影响见图3。
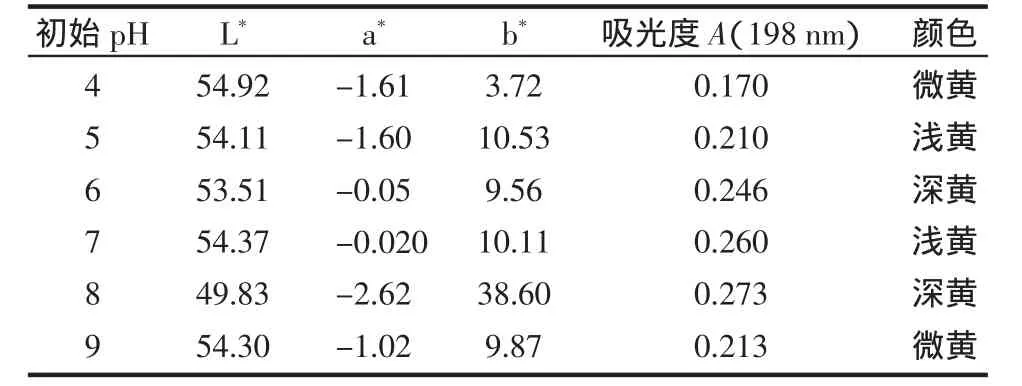
表3 反应pH值对模拟体系色泽和紫外吸收的影响Table3 Effects of reaction pH on the color of UV absorption of model system
从表3可以看出,随着pH升高,溶液颜色的亮度变化先是下降,到pH值8时,亮度最小,此时的a*值也最小,b*值为最大,紫外吸收也达到最大,溶液颜色达到最深呈深黄色,因此可以说明在160℃下,反应30 min,模拟体系的初始pH值为8时,美拉德反应速度最快,这与文献报道的一致[11]。
从图3可以看出,在160℃下模拟体系发生美拉德反应30 min,随着pH值的升高,丙烯酰胺含量慢慢升高,当pH值达到8时丙烯酰胺含量达到最大值,继续升高pH值,丙烯酰胺含量开始下降,这与美拉德反应程度呈高度一致性,同时也验证了丙烯酰胺形成机理主要来自美拉德反应这个阐述[6]。
2.4 摩尔比对葡萄糖/天冬酰胺模拟体系的影响
葡萄糖/天冬酰胺的摩尔比对模拟体系的色泽和紫外吸收的影响见表4,葡萄糖/天冬酰胺的摩尔比对丙烯酰胺形成的影响见图4。
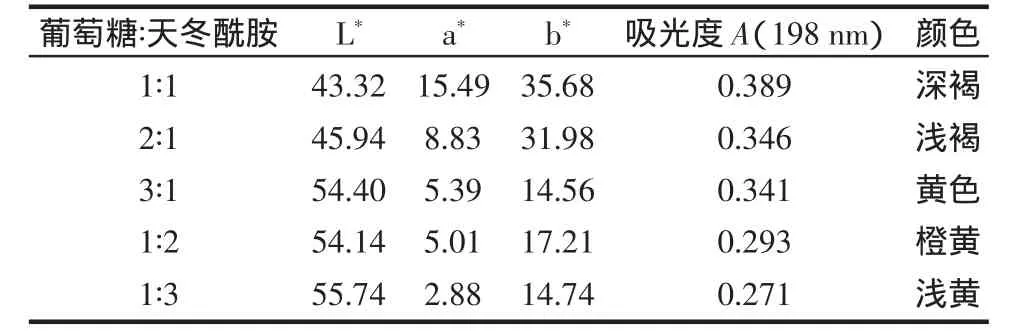
表4 反应物质的量比对模拟体系的影响Table4 Effects of ratio of glucose to asparagine on model system
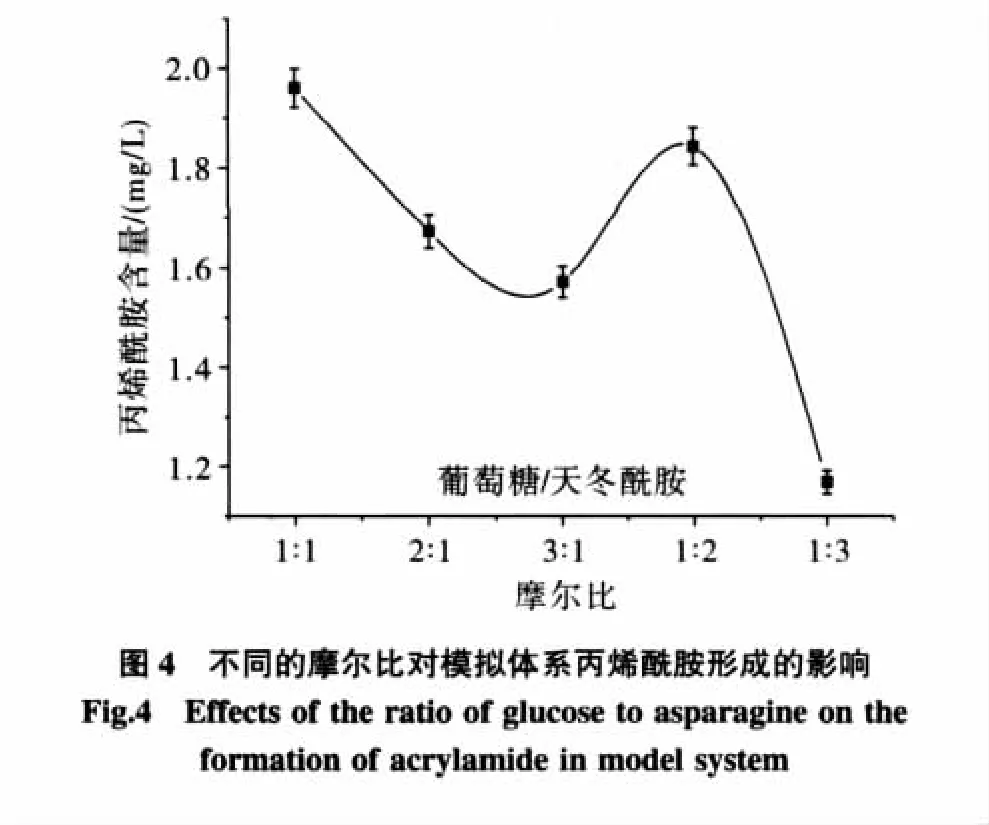
从表4可以看出,随着葡萄糖/天冬酰胺的摩尔比变化,溶液颜色的亮度发生不规律的变化,在此模拟体系中,葡萄糖含量增加,亮度升高,a*值下降,b*值也下降,紫外吸收也相应下降,总体颜色从深褐色到黄色。同时,在此模拟体系中,天冬酰胺含量增加,亮度升高,a*值下降,b*值也下降,紫外吸收也相应下降,总体颜色从深褐色到浅黄色。表明了美拉德反应速度随着反应体系中的还原糖与氨基酸配比而影响,配比相当时速度最快,丙烯酰胺形成的量也就越大。天冬酰胺过量引起的对形成丙烯酰胺的影响要小于葡萄糖过量引起的影响。
3 结论
1)葡萄糖/天冬酰胺模拟体系的反应温度是影响丙烯酰胺形成的关键因素,天冬酰胺含量对丙烯酰胺形成的影响小于葡萄糖对其的影响。
2)葡萄糖/天冬酰胺模拟体系随着初始pH值增加丙烯酰胺含量随着增加,当pH值达到8时达到最大,同样随着反应时间延长,丙烯酰胺含量增加。
[1]LeQuesne P M.Acrylamide.In:Spencer PS,Schaumburg HH(eds)Experimental and clinical neurotoxicology[M].Williams and Wilkins,Baltimore,1980:309-325
[2]Sagerback D,Calleman C J,Schroeder J L,et al.Formation of N-7(2-carbamoyl-2hydroxyethyl)guanine in DNA of the mouse and the rat dollowing intraperitoneal administration of[14C]acrylamide[J].Carcinogenesis 1995,16(5):1161-1165
[3]Bergmark E,Calleman C J,He F,et al.Determination of hemoglobin adducts in humans occupationally exposed to acrylamide[J].Toxicol.Appl.Pharmacol.,1993,120(1):45-54
[4]IRAC monographs on the evaluation of carcinogenic risks to humans[C].vol 60.International Agency for Research on Cancer,Lyon,1994:389
[5]Mottram D S,Wedzicha B I,Dodson A T.Acrylamide is formed in the Maillard reaction[J].Nature,2002,419:448-449
[6]Zyzak D V,Sanders R A,Stojanovic M,et al.Acrylamide formation mechanism in heated foods[J].Journal of Agricultural and Food Chemistry,2003,51(16):4782-4787
[7]Becalski A,Lau B P Y,Lewis D,et al.Acrylamide in food:occurrence,sources and modeling[J].Journal of Agricultural and Food Chemistry,2003,51(3):802-808
[8]Friedman M.Chemistry,Biochemistry,and Safety of Acrylamide.A Review[J].Journal of Agricultural and Food Chemistry,2003,51(16):4504-4526
[9]中华人民共和国国家质量监督检验检疫总局.中华人民共和国国家标准GB/T5009.204-2005食品中丙烯酰胺含量的测定方法气相色谱-质谱(GC-MS)法[M].北京:中国标准出版社,2006:26-28
[10]杨玉生,张彭湃,马武生,等.紫外分光光度法分析测定微量丙烯酰胺的研究[J].食品科技,2005,31(1):81-83
[11]刘邻渭.食品化学[M].北京:中国农业出版社,2000:35-36
The Formation Study of Acrylamide in the Model System of Glucose/Asparagine
ZHANG Yin-liang,BAI Ming-xing
(School of Food and Biology Engineering,Zhengzhou University of Light Industry,Zhengzhou 450002,Henan,China)
The model system of glucose and Asparagine was carried out to study the effect of reaction condition on acrylamide formation.The effect of reaction temperature,reaction time,original pH value and molar ration on acrylamide formation have been studied in terms of colority,UV absorbency at 198 nm and the content of acrylamide.The results demonstrate that reaction temperature is a key factor for acrylamide formation,glucose is much more important for acrylamide formation than asparagine.And the content of acrylamide is maximum at original pH 8.
acrylamide;Maillard reaction;model system;Asparagine
郑州轻工业学院博士基金项目(2007BSJJ007)
章银良(1963—),男(汉),教授,博士,主要从事食品科学方向的研究与教学工作。
2009-07-29
