盐酸法制备低氟含量饲料级磷酸氢钙的工艺研究
2010-10-23段利中颜家保范宝安
段利中,颜家保,范宝安
(武汉科技大学湖北省煤转化与新型炭材料重点实验室,湖北武汉430081)
盐酸法制备低氟含量饲料级磷酸氢钙的工艺研究
段利中,颜家保,范宝安
(武汉科技大学湖北省煤转化与新型炭材料重点实验室,湖北武汉430081)
在不添加任何除氟剂的条件下,用盐酸浸取磷矿,通过调整工艺参数和采用特殊的试验条件,制备了低氟含量饲料级磷酸氢钙;着重探讨了盐酸浓度、反应时间、静置时间、温度、鼓气速率等因素对磷酸氢钙中氟含量的影响.结果表明,在盐酸溶解过程中减少氟的溶出,有利于在反应中同步降低氟含量;得到的磷酸经简单的过滤、中和,可用于制备氟含量低达0.1%(低于国家标准0.18%)的饲料级磷酸氢钙.
盐酸法;低氟含量;饲料级磷酸氢钙;制备;工艺
我国磷矿资源丰富,磷矿储量仅次于摩洛哥,居世界第二位.但是,大多数属于中低品位矿,矿石反应活性低,杂质含量高,为典型的难选低活性磷矿种类[1].湖北省磷矿资源比较丰富,但绝大部分为中低品位且难选[2].对于我们这个人口众多资源相对缺乏的国家来说,低品位氟含量高的磷矿的开发利用显得尤为重要,磷矿是生产饲料级磷酸氢钙的原料,但在酸溶过程中,磷矿中的氟元素容易溶解在液相中,很难再分离出来[3],导致所产磷酸氢钙中的氟含量偏高,而氟含量过高对家禽,家畜的身体造成毒害,进而对人体产生伤害,有些低品位的磷矿氟含量高达18%,本研究所采用的来自湖北孝感某地的磷矿氟含量高达18%,因此除氟至关重要.
饲料级磷酸氢钙(以下简称饲钙)生产工艺有多种,目前国内主要为湿法磷酸法,采用该法产量占国内生产总量的80%以上[4].湿法磷酸的除氟方法主要有溶剂萃取法[5]、浓缩法[6]和化学沉淀法.国外的研究起步较早,上世纪60年代初,以色列矿业工程公司(I.M.I)开发了著名的IMI法,首次实现了盐酸法生产磷酸的工业化[7].1987年,荷兰的Sietse van der Sluis,Yulia Meszaros和Wim GJ Marchee[8]等人用磷酸处理磷矿;1992年,巴西的Marcato和 Giulietti[9]用硝酸处理磷矿;虽然国内外的研究都取得一定的进展,但都需要添加除氟剂和其他溶剂,增加了生产成本和设备投资,也加大了处理副产物的难度.
本研究是在实验室条件下进行的,用盐酸溶解磷矿,在不添加除氟剂的情况下,通过调整工艺参数和采用特殊的试验条件,在磷矿浸取阶段采用单因素法进行试验,寻找抑制氟以离子或络合离子形式向液相转移的主要影响因素,为低氟含量的高品质饲料级磷酸氢钙的生产打下一定的基础.
1 实验部分
1.1 主要试剂和仪器
HCl(36%);磷矿(120目过筛);柠檬酸钠溶液(0.75 mol/L);乙酸钠溶液(3 mol/L);高氯酸(优级纯);NaF(分析纯);乙酸(1 mol/L);丙酮(分析纯);Ca(OH)2(分析纯);氨水(分析纯).
p HS-25型p H计(上海精密科学仪器有限公司);pF-1Q9型氟离子选择性电极(上海罗素科技有限公司);AL204型电子天平(梅特勒-托利多仪器(上海)有限公司);JJ-1A型精密定时搅拌器(江苏省金坛市荣华仪器制造有限公司),流量计.
1.2 实验步骤
实验前,把恒温水浴锅调到实验所需的温度;待温度稳定后,向三口烧瓶中加入称量好的10 g磷矿和一定量的蒸馏水,用移液管移取一定量的盐酸,加入三口烧瓶,开启搅拌器,记下加酸的起始时间;反应一定时间后,关闭搅拌器,把烧瓶拿下,室温静置一段时间,将反应后的溶液抽滤,得到的滤液用氨水中和至p H=5.4(中和时用磁力搅拌器搅拌),过滤,母液回收处理,滤饼用丙酮过滤后得到产品磷酸氢钙.将产品自然风干,最后根据国家标准 GB/T 22549—2008[10]采用氟离子选择性电极测定饲料级磷酸氢钙中的氟含量.
1.3 实验原理
磷矿的主要成分是氟磷灰石(Ca5F(PO4)3),矿石中还含有少量的碳酸镁、SiO2、Na+、K+、Ca2+以及铁、铝、锰氧化物.
反应阶段的主要反应如下:


中和反应控制不好会严重影响产品质量.用氨水中和磷酸时,当p H>2.5时,液相开始有少量沉淀析出;随着p H值的升高,磷酸氢钙析出量逐步增加,当p H≥5.0时磷酸氢钙几乎完全析出;当p H>6.0后,有磷酸三钙生成,同时由于铁、锰等有色金属离子的析出而略带淡黄色,影响产品外观.中和过程应控制在p H值为5.0附近为宜[3].因此本研究的反应终点的p H值为5.4.
磷酸与氨水的反应:
2 结果与讨论
2.1 盐酸浓度的影响
反应条件:矿石用量10 g,反应温度为室温,反应时间为1 h,静置1 h,用氨水中和,反应终点的p H为5.4.
由图1可见,随着盐酸浓度的增加,所产磷酸氢钙中的氟含量随之下降,在盐酸浓度为5.3 mol/L时达到最低2.22%,继续增加盐酸浓度,氟含量急剧上升.当盐酸浓度由4.8 mol/L增加到5.3 mol/L时,溶液中的酸度增加,H+的浓度增加,使得HF的电离平衡HF=H++F-向左进行,溶液中的氟主要以HF气体的形式逸出,有效地降低了氟含量;当盐酸浓度超过5.3 mol/L后,由于加入盐酸浓度过大,反应剧烈,产生大量的泡沫,使得 HF气体在液面的停留时间增加,导致氟含量增加.因此,确定较佳盐酸浓度为5.3 mol/L.
2.2 反应时间对氟含量的影响
反应条件:矿石用量10 g,反应温度为40℃,盐酸浓度为5.3 mol/L,静置1 h,用氨水中和,反应终点的p H为5.4.

图1 盐酸浓度对氟含量的影响Fig.1 The effect of hydrochloric acid concentration on fluorine content

图2 反应时间对氟含量的影响Fig.2 The effect of reaction time on fluorine content
由图2可见,反应时间对磷酸氢钙中的氟含量影响较大,随着反应时间的延长,氟含量逐渐降低.由于随着反应时间的延长,磷矿被盐酸充分溶解,从磷矿中浸出的Ca2+增加,而此时溶液的酸度也有利于CaF2的形成;另外,Fe和 Al在酸的含量减小时,它们可以反应形成不溶的化合物[11](如 Ca4SO4AlSiF13·10 H2O[12]),使得氟含量明显降低,反应2 h时,氟含量达到最低2.62%.反应时间超过2 h后,氟含量开始增大,后略有下降并趋向于稳定.由于反应时间过长溶液中的酸度下降,H+的浓度明显减小,HF的电离平衡 HF=H++F-向右进行,此时,驻留在反应器中的SiF4气体也进入液相,氟含量随之增大;4 h后反应体系达到稳定,氟含量基本保持不变.因此,确定较佳反应时间为2 h.
2.3 静置时间对氟含量的影响
反应条件:矿石用量10 g,反应温度为40℃,盐酸浓度为5.3 mol/L,反应时间为2 h,用氨水中和,反应终点的p H为5.4.
由图3可见,静置的时间越长,生产的磷酸氢钙中的氟含量越低,静置0.5 h~1.5 h时,氟含量基本不变且较高,由于在静置的过程中封闭在液面上方的 HF气体溶于冷凝在三口烧瓶上方的水蒸气中,同时溶液中的F–与Fe3+,Al3+络合,导致氟含量较高,静置时长超过1.5 h后,随着磷矿中的酸度降低,F–与Ca2+,Al3+形成CaF2,Ca4SO4AlSiF13·10H2O沉淀,由于静置的时间越长,沉淀越完全,氟含量也越低.因此,考虑到生产效率确定较佳的静置时长为2.5 h,此时氟含量为1.5%.
2.4 鼓气速率对氟含量的影响
反应条件:矿石用量10 g,盐酸浓度为5.3 mol/L,反应时间为2 h,静置2.5 h,用氨水中和,反应终点的p H为5.4.
由图4可见,鼓气速率从500 mL/min增加到700 mL/min时,磷酸氢钙中的氟含量逐渐降低,当鼓气速率为700 mL/min达到最低0.1%,这是由于鼓气速率过低时,鼓入的气体太少,HF气体被气提的就少,相应的液相中氟含量就高;当鼓气速率超过700 mL/min时,氟含量增加,这是由于鼓气速率过快时,液面上层会产生大量泡沫,使含 HF气体停留时间增加,氟含量反而略有上升.因此,确定较佳的鼓气速率为700 mL/min.

图3 静置时间对氟含量的影响Fig.3 The effect of retention time on fluorine content

图4 鼓气速率对氟含量的影响Fig.4 The effect of foaming on fluorine content
2.5 鼓气存在时温度对氟含量的影响
反应条件:矿石用量10 g,盐酸浓度为5.3 mol/L,鼓气速率700 mL/min,反应时间为2 h,静置2.5 h,用氨水中和,反应终点的p H为5.4.
由图5可见,温度升高磷酸氢钙中的氟含量略有升高,由于温度较低时,磷矿的溶解缓慢,HF气体的溶解度较大,HF的逸出速率相对较小,但鼓气的存在可以有效地把所产生的HF气体气提出来,达到有效除氟的目的.温度升高,略有上升,根据阿伦尼乌斯方程:k=Aexp(–Eα/R T),k为速率常数,R为摩尔气体常量,T为热力学温度,Eα为表观活化能,A为指前因子(也称频率因子).因为温度升高,矿石溶解加快,产生的 HF泡沫多,HF极易溶于水,而溶解的 HF与矿石中的SiO2存在平衡反应:4HF+SiO2=SiF4+2H2O,温度升高SiF4的水解速率 SiF4+2H2O=2H2SiF6+H2SiO3增加[13],进入液相的氟增多,氟含量升高.温度超过50℃时,由于鼓气能有效的包裹 HF使其减小与液相接触的机会,从而使氟含量降低.温度为65℃时,达到最低0.12%.当温度超过65℃时,反应速率增加,产生大量的泡沫使得氟含量上升.因此,确定较佳的反应温度为65℃.
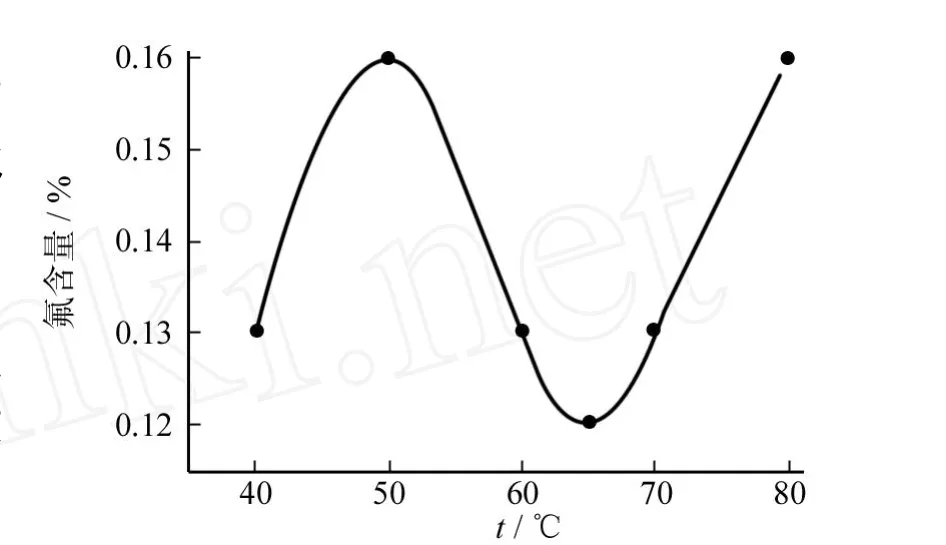
图5 温度对氟含量的影响Fig.5 The effect of temperature on fluorine content
3 结论
(1)本研究的优化工艺条件为:反应时间为2 h,静置时长2.5 h,反应温度为65℃,盐酸的浓度为5.3 mol/L,鼓气速率为700 mL/min.在该条件下,产品磷酸氢钙中的氟含量最低可达0.1%,低于饲料级磷酸氢钙的国家标准(<0.18%)的要求.
(2)当鼓气存在时,所产磷酸氢钙中的氟含量最低可达0.1%,明显低于普通条件下的最低氟含量1.5%.
(3)鼓气在适当的条件下有利于除氟.当鼓气速率过慢时,由于鼓入的气体太少,HF气体被气提的就少,相应的液相中氟含量就高.鼓气速率如果过快时,导致液面上层形成大量的泡沫聚集,反而使 HF气体的停留时间增长不利于除氟.
[1]毛常明,刘晶晶,尹进华,等.湿法磷酸的工艺研究进展[J].河北化工,2005,(4):14-16.
[2]刘乃富.湖北省中低品位磷矿合理利用的分析与建议[J].化工矿物与加工,2005,(11):1-4.
[3]范保安,王广建,陈学玺.盐酸浸取磷矿制酸的无除氟清洁工艺[J].青岛化工学院学报,2002,23(3):23-26.
[4]杜丽梅,曹极飞,魏忠雄.饲料级磷酸氢钙发展现状及市场前景[J].云南化工,2002,29(4):36-38.
[5]王军民.湿法磷酸的净化脱氟新工艺研究[J].无机盐工业,2001,33(1):6.
[6]励生,胡文成.湿法磷酸浓缩特性及脱氟速率的研究 [J].磷肥与复肥,1995,10(4):5-7.
[7]Slack A V.Phosphoric Acid.VolⅠ,PartⅡ[M].New York:Marcel Dekker Inc,1968.
[8]Sietse van der S,Yulia M,Wim GJ.The digestion of phosphate ore in phosphoric acid[J].Ind Eng Chem Res,1987,26:2501-2505.
[9]Marcato R,Giulietti M.Production of dicalcium phosphate by treatment of phosphate rock with concentrate nitric acid[J].Fertil Res,1993,34:203-207.
[10]中华人民共和国国家标准 [S].GB/T 22549—2008.
[11]Zafar Z I,Anwar M M,Pritchard D W.Beneficial route of low-grade phosphate rocks for fertilizer production[J].Ind Eng Chem Res,1995,34:4501-4507.
[12]Frazier A W,Lehr J R,Dillard E F.Chemical behavior of fluorine in production of wet-process phosphoric acid[J].Environm Sci Technol,1977,11(10):1007-1014.
[13]崔波,陈学玺,杨 兰,等.磷矿除氟工艺研究 [J].化工矿物与加工,2006,(12):8-9.
Technology for Preparing Feed-Grade Dicalcium Phosphate with Low Content of Fluorine via Hydrochloric Acid Route
Through adjusting process parameters and adopting special experimental conditions,feed-grade dicalcium phosphate with low content of fluorine was preparedvialeaching phosphate ore with hydrochloric acid in the absence of any defluorinating agents.The effects of concentration of HCl,reaction time,retention time,temperature and foaming on the content of fluorine in dicalcium phosphate were investigated.Results indicate that inhibiting dissolution of F during leaching of phosphate ore in HCl contributes to simultaneously decrease F content in title product.Phosphoric acid obtained along with leaching in HCl,after simple filtration and neutralization,can be well used to prepare feed-grade dicalcium phosphate with low F content of 0.1%(lower than corresponding national standard 0.18%).
hydrochloric acid route;low F content;feed-grade dicalcium phosphate;preparation;technology
O 611.65
A
1008-1011(2010)05-0021-04
2010-04-18.
武汉科技大学绿色制造与节能减排科技研究中心开放基金(B0915).
段利中(1985-),男,工学硕士,从事磷化工与化工环境污染治理的研究.
