猪脂肪控制氧化及挥发性氧化产物研究
2010-10-19徐永霞张若洁徐竞一陈清婵王可兴潘思轶
徐永霞,张若洁,徐竞一,陈清婵,王可兴,潘思轶*
(华中农业大学食品科学技术学院,湖北 武汉 430070)
猪脂肪控制氧化及挥发性氧化产物研究
徐永霞,张若洁,徐竞一,陈清婵,王可兴,潘思轶*
(华中农业大学食品科学技术学院,湖北 武汉 430070)
通过单因素试验和正交试验研究以热反应制备肉味香精前体物为目的的猪脂肪控制氧化工艺条件。以过氧化值(POV)、硫代巴比妥酸值(TBA)和酸值(AV)表征油脂的氧化状态。结果表明,猪脂肪控制氧化的较佳工艺条件为:反应温度120℃、反应时间2h、氧气流速0.025m3/h。采用固相微萃取-气质联用技术对猪脂肪控制氧化产物中的挥发性成分进行分析,共鉴定出32种化合物,其中醛类化合物占52.52%,为猪脂肪控制氧化产物中的主要挥发性成分。
猪脂肪;控制氧化;肉味香精;工艺;挥发性成分
Abstract:The process conditions for the controlled oxidation of lard before the production of pork flavor via thermal reaction were optimized using orthogonal array design based on single factor and experiments. Peroxide value (POV), thiobarbituric acid (TBA) and acid value (AV) were used to evaluate oxidation status. The optimal controlled oxidation conditions of lard were found to be:reaction temperature, 120 ℃; reaction duration, 2 h; and oxygen flow rate, 0.025 m3/h. The volatile oxidation products obtained under these optimal conditions were analyzed by headspace solid phase micro-extraction (HS-SPME)combined with GC-MS. A total of 32 compounds were identified in oxidized lard. Aldehydes were the most abundant volatile components, which accounted for 52.52% of the total volatile oxidation compounds.
Key words:lard;controlled -oxidation;meat flavor;process;volatile components
肉味香精作为一种重要的食品添加剂已广泛应用于方便食品、肉制品和膨化食品等众多食品中,主要用于产品的调香、呈味[1]。以脂类为原料,用氧化脂肪参与热反应制备的肉味香精,是获得良好肉香风味的较好途径[2],也是近年来逐渐兴起的一种方法。采用脂肪控制氧化技术制备的肉味香精,不仅肉味浓郁、和谐,而且各种肉的特征性香味突出。
研究表明[3],不同种类的肉的特征香味来自于动物脂肪部分。如果从各种肉类(如牛、猪、鸡肉等)组织中除去脂肪部分,经加热后具有类似的香味,难以区别出各种肉的特征香气。在空气中加热牛和猪的脂肪时,一开始就会产生肉的特征香味,而在氮气中加热时,则不能生成肉的加热香味。这说明某种程度的脂肪氧化在香味生成上具有很重要的作用[4]。脂质对肉香味的贡献主要从以下两个方面来实现:脂质降解生成肉香味挥发性组分;脂质和Maillard 反应间的相互作用[5]。动物脂肪在高温下发生氧化反应,脂肪酸断裂形成很多挥发性物质,其中对风味作用比较大的是较低香气阈值的脂肪族醛、酮、醇和内酯化合物等,具有肉香味,它们在特征肉香味形成中起重要作用[6]。
研究发现[7],脂肪氧化产生的不饱和醛、酮等含羰基化合物与氨基酸、肽等含氨基化合物反应,脂肪通过降低含硫化合物的含量以及提供挥发性化合物而改善肉的香味。成坚等[8]、谢建春等[9]分别研究了鸡脂肪氧化和美拉德反应制备鸡肉香精。龚钢明等[10]进行了氧化牛油Maillard反应制备牛肉香精的研究。不同的动物油脂组分和氧化程度的不同,对经美拉德反应形成特定肉风味物质起着重要的作用。本实验通过单因素和正交试验来研究猪脂控制氧化规律和以制备肉味香精为目的的较优化工艺条件,并对猪脂肪控制氧化的挥发性产物进行分析。实验结果对以动物脂肪为原料制备肉味香精的技术开发提供参考。
1 材料与方法
1.1 材料与设备
猪板油购自当地超市;C8~C20正构烷烃标准品德国FluKa化学公司。
Agilent 6890 N/5975气质联用(GC-MS)仪 美国Agilent公司;固相微萃取装置、20mL顶空钳口样品瓶美国Supelco公司;DVB/CAR/PDMS 50/30μm(二乙烯基苯/碳分子筛/聚二甲基硅氧烷);LZB-4玻璃转子流量计。
1.2 方法
1.2.1 猪脂肪氧化指标的测定
过氧化值(POV)、硫代巴比妥酸值(TBA)和酸值(AV)的测定方法、试剂的配制及标定方法等参照文献[11-12]进行。
1.2.2 猪脂肪控制氧化实验
在装有直形回流冷凝管、水银温度计及通气管的500mL三口烧瓶中加入50g猪脂,置于恒温磁力搅拌器中进行油浴加热。当反应瓶温度上升到指定温度时开始通入一定流量的氧气并计时,到达指定时间停止反应,取样分析。
1.2.3 固相微萃取法制备样品
取适量在70℃水浴中融化均匀的猪脂肪样品于螺口样品瓶中,加入磁转子,用聚四氟乙烯隔垫密封,于磁力搅拌器上加热平衡10min。用已活化好的DVB/CAR/PDMS 50/30μm萃取头(270℃活化30min)顶空吸附20min后,将萃取头插入GC进样口,解析5min。
1.2.4 气相色谱-质谱分析
Agilent公司6890-5973N气相色谱-质谱仪。
气相色谱条件:HP-5毛细管柱(30m×320μm,0.25μm);进样口温度:250℃,不分流进样;升温程序:起始温度40℃,以3℃/min升至120℃,保持2min,再以5℃/min升至240℃。
质谱条件:色谱-质谱接口温度280℃,离子源温度230℃,四极杆温度150℃;离子化方式:EI,电子能量70eV,质量扫描范围35~350u。
2 结果与分析
2.1 不同反应条件对氧化猪脂肪效果的影响
在参考相关文献及大量预备实验的基础上,对反应时间、反应温度及氧气流速3个因素对POV、TBA和AV值的影响趋势分别进行单因素试验,从而筛选出POV、TBA适当高、AV尽可能低的氧化产物,找出较佳工艺条件组合,为热反应制备猪肉香精提供较好的前体物质。
2.1.1 反应温度对猪脂肪控制氧化的影响
在固定猪脂用量50g、反应时间2h、氧气流速0.025m3/h的条件下,对猪脂肪进行氧化,平行实验2次。测定氧化猪脂肪的POV、AV和TBA,取各项指标的平均值,考察不同反应温度对各指标的影响,如图1所示。

图1 温度对AV、POV和TBA的影响Fig.1 Effect of oxidation temperature on AV, POV and TBA
由图1可以看出,AV随着温度的升高而逐渐增大。在100~120℃之间AV增加较缓慢,在120℃之后AV增幅明显变大。从AV考虑,氧化温度不宜超过120℃。AV可反映油脂氧化形成脂肪酸的含量,通常也被用于表示油脂酸败的程度,油脂酸败产生的低级脂肪酸具有臭味,AV越高酸败和焦臭味就越严重。在100~130℃之间,POV随着温度的升高而增大,从100℃到110℃时,POV明显上升,之后增加变缓,在130℃时POV达最大值。当温度大于130℃时,POV又呈下降趋势。POV的高低反映出油脂氧化形成氢过氧化物(ROOH)的含量,虽然ROOH不能提供香气,但它的分解和热解可提供肉香味物质或肉香味前体物,仅从制备肉香味物质或肉香味前体物考虑,高POV有利于肉香味物质的形成。油脂氧化初期,POV随氧化程度加深而增大,而当油脂深度氧化时,ROOH的分解速度超过其生成速度,从而导致POV下降。
油脂氧化过程中,不饱和脂肪酸进一步分解产生醛、酮和低分子有机酸类等化合物,丙二醛是动物油脂变质过程中的中间产物。TBA反映了油脂氧化酸败的程度。TBA越大说明油脂被氧化的程度越甚。当脂肪严重酸败后,测得的结果反而会显著降低。可能由于脂肪氧化成醛后,进一步氧化成酸类物质而使原醛类物质含量降低。温度对TBA的影响较小,温度从100℃增至120℃,TBA增加缓慢,在120℃时达最大值,之后又开始下降。
因此,综合考虑氧化温度对AV、POV和TBA的影响,猪脂肪氧化温度取120℃比较适合。此时既可以得到较高的POV和TBA,这对香气物质的产生有利,同时又可使AV处于相对低的范围,以防止产生焦臭味等不良气味。
2.1.2 反应时间对猪脂肪控制氧化的影响
在固定猪脂肪用量50g、反应温度120℃、氧气流速0.025m3/h的条件下,对猪脂肪进行氧化,平行实验2次。测定氧化猪脂肪的POV、AV和TBA,取各项指标的平均值,考察不同反应时间对各指标的影响,如图2所示。

图2 时间对AV、POV和TBA的影响Fig.2 Effect of oxidation time on AV, POV and TBA
由图2可以看出,AV随着时间的延长而逐渐增加。在1~3h内AV增加较缓慢,在3h之后增幅明显增大。从AV考虑,氧化时间不宜超过3h。POV在反应1h后迅速上升,之后增加幅度较缓,在反应4h后有下降的趋势。时间对TBA值的影响较小,在1~2h之间,TBA有所增加,当反应超过2h后,TBA又逐渐下降。因此,综合考虑反应时间对AV、POV和TBA的影响,要获得较高的POV和TBA,控制较低的AV,较佳的反应时间应为2~3h。
2.1.3 氧气流速对猪脂肪控制氧化的影响
在固定猪脂肪用量50g、反应温度120℃、反应时间2h的条件下,对猪脂肪进行氧化,平行实验2次。测定氧化猪脂肪的POV、AV和TBA,取各项指标的平均值,考察不同氧气流速对各指标的影响,如图3所示。
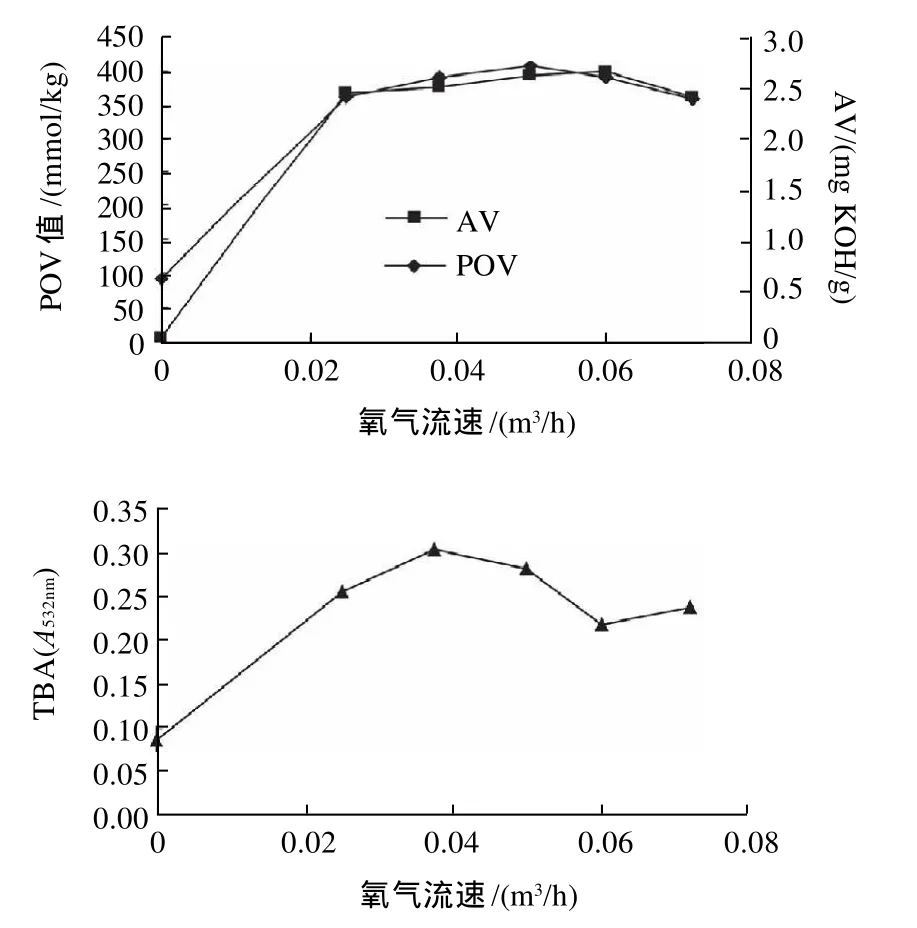
图3 氧气流速对AV、POV和TBA的影响Fig.3 Effect of oxygen flow rate on AV, POV and TBA
由图3可以看出,当通氧气时会明显提高猪脂肪的POV、AV和TBA。AV和POV在氧气流速0.025~0.0375m3/h之间基本保持不变,当大于0.06m3/h时有下降趋势,总体变化趋势都较平缓,表明氧气流速的变化对AV和POV的影响较小。TBA随氧气流速增大而增加,在氧气流速为0.0375m3/h时达最大,之后又开始降低。因此,要获得较高的POV、TBA和尽可能低的AV值,氧气流速选取0.0375m3/h比较适合。
2.2 猪脂肪控制氧化的正交试验
2.2.1 各因素对氧化猪脂肪AV的影响
由表1可知,各因素对AV的影响顺序是:氧化时间>氧化温度>氧气流速。温度和时间通常是两个有相互作用的因素。在脂类氧化过程中,当温度选择较低时,则时间会略长一点,而当温度选择较高时,则时间会比较短[13]。氧化时间延长,AV上升,在2h后,AV上升幅度明显。其他因素的影响规律是:氧化温度升高,AV上升,从120℃到130℃,AV上升幅度较大,在130℃时AV最高;氧气流速对AV影响较小。

表1 正交试验结果及分析Table 1 Orthogonal array design arrangement and experimental results
2.2.2 各因素对氧化猪脂肪POV的影响
由表1可知,各因素对POV的影响顺序是:氧化时间>氧化温度>氧气流速。时间是最重要的因素。时间越长,POV越大。其他因素的影响规律是:氧化温度升高,POV增加,但从120℃到130℃,POV增加不明显;氧气流速对POV影响较小。
2.2.3 各因素对氧化猪脂肪TBA的影响
由表1可知,各因素对TBA的影响顺序是:氧气流速>氧化时间>氧化温度。时间和氧气流速对TBA的影响大小无明显差别。TBA随氧气流速的增大而增加。随时间的延长,TBA增加。TBA受氧化温度的影响不明显。
2.2.4 猪脂肪控制氧化的较优工艺
据以上分析,要获得较高的POV和TBA以及较低的AV,猪脂肪控制氧化的较佳工艺条件为:氧化温度120℃、氧化时间2h、氧气流速0.025m3/h。
2.3 猪脂肪控制氧化挥发性成分分析
以较佳工艺下获得的氧化猪脂肪为研究对象,采用SPME-GC-MS法分离鉴定出的挥发性氧化产物及其相对质量分数见表2。
用固相微萃取-气质联用技术对控制氧化猪脂肪的挥发性成分进行提取分离,通过计算机谱库(N IST/WILEY)进行检索及RI值,再结合相关文献进行人工谱图解析。由表2可知,在猪脂肪中共检测出32种挥发性氧化产物,其中有12 种醛类化合物,总相对质量分数为52.52%,为猪脂控制氧化产物中的主要挥发性成分;5种酸类化合物,总相对质量分数为10.18%;5种醇类化合物,总相对质量分数为3.95%;呋喃类化合物1种,相对质量分数为3.19%;3种酯类化合物,总相对质量分数为0.93%;3种酮类化合物,相对质量分数为0.53%;3种烃类化合物,总相对质量分数为0.47%。其中相对质量分数较高的是己醛(1.96%)、庚醛(1.63%)、(E)-2-庚烯醛(3.03%)、辛醛(3.57%)、(E)-2-辛烯醛(7.26%)、壬醛(3.78%)、(E)-2-壬烯醛(2.55%)、2,4-壬二烯醛(1.26%)、(E)-2-癸烯醛(11.13%)、(E,E)-2,4-癸二烯醛(6.18%)、2-十一烯醛(9.19%)、己酸(5.73%)、壬酸(2.41%)、1-辛烯 -3-醇(1.32%)、1-辛醇(2.29%)、2-戊基呋喃(3.19%)。
猪脂肪控制氧化的主要挥发性成分是醛类化合物,一般认为不同种类的肉的特征香味来自于动物脂肪部分,那么,醛类作为脂肪氧化降解的主要成分,其中很可能含有某种特征香味物质[3,5]。大部分研究表明[14-15],醛类物质是脂类氧化的主要挥发性成分,与本实验结果一致。(E,E)-2,4-癸二烯醛是猪脂氧化的重要醛类化合物,具有油腻的脂肪味,油炸鸡香味,醛香、土豆、青香,它是深度油炸食品中最重要的香味物质之一[13]。其他醛类化合物如2-十一烯醛、(E)-2-癸烯醛、2,4-壬二烯醛、(E)-2-辛烯醛、壬醛、庚醛等具有多种香味特征,如脂肪香、油炸香味、坚果味、金属味、黄瓜味和水果味等。
此外,检测到的醇类、酯类和酮类化合物对猪脂氧化产生的猪脂香味有贡献。1-辛烯-3-醇是亚油酸自动氧化的产物,具有蘑菇香、青香、蔬菜香以及油腻的气息。γ-内酯则会产生愉悦的油炸香味[13]。其他的挥发物,包括呋喃、脂肪酸、碳氢化合物对猪脂香味也有贡献。其中2-戊基呋喃是亚油酸自动氧化的产物,可能是含脂食品中的重要的香味物质[16]。
3 结 论
研究了以热反应制备猪肉香精为目的的猪脂肪控制氧化反应工艺条件,并以POV、AV及TBA值作为猪脂肪氧化状态的控制指标。通过单因素及正交试验确定了猪脂肪控制氧化的相对优化工艺条件为:反应温度120℃、反应时间2h、氧气流速0.025m3/h。猪脂肪氧化程度不需太高,因为氧化程度越高,挥发性氧化产物中增加香气的化合物会增加,但产生异味的化合物也会增加,这将对猪脂肪风味产生不利影响。
采用顶空固相微萃取-气质联用技术对猪脂肪控制氧化的挥发性成分进行分析,共鉴定出32种化合物,其中醛类化合物占52.52%,为猪脂肪控制氧化产物中的主要挥发性成分,它们将是参与麦拉德反应,形成猪肉香味的主要组分。此外还鉴定出5种酸类化合物(10.18%),5种醇类化合物(3.95%),1种呋喃类化合物(3.19%),3种酯类化合物(0.93%)等对猪肉香味有贡献的挥发性成分。
[1] 肖作兵, 杨斌, 王婷婷. 脂肪控制氧化制备鸡肉香精前体物的工艺研究[J]. 食品工业, 2008(1):41-43.
[2] 孙宝国. 肉味香精技术进展[J].食品科学, 2004, 25(10):339-342.
[3] FARMER L J, PATTERSON R I S. Compounds contributing to meat flavor[J]. Food Chem, 1991, 40:201-205.
[4] 彭秋菊, 孙宝国, 梁梦兰, 等. 牛脂氧化制备肉味香精的研究进展[J].食品科学, 2005, 26(2):245-249.
[5] MOTTRAM D S. Flavour formation in meat and meat products:a review[J]. Food Chem, 1998, 62(4):415-424.
[6] 孙寒潮, 刘通讯. 脂肪对美拉德反应产物挥发性香气成分的影响研究[J].食品工业科技, 2007, 28(9):87-91.
[7] 杨红菊, 乔发东, 马长伟. 脂肪氧化和美拉德反应与肉品风味质量的关系[J].肉类研究, 2004(1):25-28.
[8] 成坚, 刘小艳. 氧化鸡油通过Maillard反应生成鸡肉风味物质的研究[J].食品与发酵工业, 2005(6):40-43.
[9] 谢建春, 孙宝国, 汤渤. 鸡脂控制氧化-热反应制各鸡肉香精[J].精细化工, 2006(2):141-144.
[10] 龚钢明, 肖作兵, 荣绍丰, 等. 氧化牛油Maillard反应制备牛肉香精研究[J]. 中国调味品, 2008(6):79-83.
[11] 韩雅珊. 食品化学实验指导[M]. 北京:中国农业大学出版社, 1992:39-41.
[12] 杨书珍, 宁正祥, 张友胜. 油溶性二氢杨梅素对油脂的抗氧化作用[J]. 中国油脂, 2003, 28(1):44-46.
[13] 文志勇, 孙宝国, 梁梦兰, 等. 脂质氧化产生香味物质[J].中国油脂,2004(9):41-44.
[14] YASUHARA A, SHIBAMOTO T. Headspace volatiles from heated pork fat[J]. Food Chem, 1990, 37:13-20.
[15] ZHU X D, WANG K X, ZHU J L, et al. Analysis of cooking oil fumes by ultraviolet spectrometry and gas chromatography-mass spectrometry[J]. J Agric Food Chem, 2001, 49:4790-4794.
[16] SAXBY M J. Food taints and off-flavours[M]. Glasgow:Blackie Academic and Professional, 1993:150-201.
Optimization of Conditions for Controlled Oxidation of Lard and Analysis of Volatile Oxidation Products
XU Yong-xia,ZHANG Ruo-jie,XU Jing-yi,CHEN Qing-chan,WANG Ke-xing,PAN Si-yi*
(College of Food Science and Technology, Huazhong Agricultural University, Wuhan 430070, China)
TS225.2
A
1002-6630(2010)21-0076-05
2010-08-31
湖北省农业科技创新团队项目(2007620)
徐永霞(1983—),女,博士研究生,研究方向为香精香料。E-mail:xuyx1009@webmail.hzau.edu.cn
*通信作者:潘思轶(1956—),男,教授,博士,研究方向为农产品加工化学。E-mail:pansiyi@mail.hzau.edu.cn
