甘油氢解Cu/Cr催化剂制备方法对性能的影响
2010-10-19欧建雄兰支利尹笃林杨春华欧兰英
欧建雄,兰支利,尹笃林,杨春华,欧兰英
(湖南师范大学精细催化合成研究所,湖南 长沙410081)
研究开发
甘油氢解Cu/Cr催化剂制备方法对性能的影响
欧建雄,兰支利,尹笃林,杨春华,欧兰英
(湖南师范大学精细催化合成研究所,湖南 长沙410081)
Cu/Cr催化剂由于Cu对C—C键氢解活性很低,对C—O键氢解活性很高而成为甘油氢解制1,2-丙二醇效果最好的固体催化剂。采用5种方法制备了Cu/Cr催化剂,并用于甘油的催化氢解反应,发现Cu/Cr催化剂的制备方式极大地影响着其对甘油的催化氢解性能。以5种方法制备的Cu/Cr催化剂中,对甘油的催化氢解性能依次是:铜氨络合沉淀法>Adkins法>碳酸钠沉淀法>硅藻土浸渍法>干混法。运用XRD、TG、BET、FTIR、TPR等表征手段对制备的催化剂结构进行了表征,详细分析了不同方式制备的催化剂的结构差异,将催化剂的结构表征结果与催化反应性能进行关联分析和讨论,并从理论上解释了催化剂结构差异和催化氢解性能的关系。关键词:催化氢解;Cu/Cr催化剂;制备方式;甘油
1,2-丙二醇(1,2-PDO)是一种重要的化工原料,广泛用于食品、医药和化妆品工业中。现有生产方法普遍采用环氧丙烷水合法,存在较大的环境污染;同时由于丙烯等石化原料价格的不断上涨和石化资源的不可再生性,迫切需要开发新的原料来源和合成路线。以生物质甘油为原料,通过催化氢解来生产丙二醇,是最有可能的替代路线。生物柴油生产过程中副产大量甘油,大约每生产1 t生物柴油可产生100 kg甘油。同时作为生物质碳资源之一的甘油,来源于生物质,是可再生资源,已被美国能源部(DOE)定义为未来的12个最基本的化工原料之一[1]。以甘油为原料来生产丙二醇既解决了甘油的生产过剩,又符合绿色化学发展的要求。
近年来,关于甘油催化氢解的研究,国外已有较多报道,并呈日益增加的趋势。甘油催化氢解的研究背景、机理及其应用,国内也有许多文献进行过详细介绍[2-4]。甘油的氢解反应中,催化剂的研发是关键,一般使用Ⅷ族等具有高加氢活性的金属与酸性载体配合的催化剂。Werpy等[5]采用Ni、Re/C催化剂催化甘油氢解制1,2-丙二醇,选择性高达88%;Perosa等[6]报道了Raney Ni 作催化剂的甘油催化氢解;Dasari等[7]报道了Cu/Cr催化甘油的氢解反应。在已研究的各种催化剂中,甘油催化氢解生成1,2-丙二醇效果最好的是含Cu催化剂,这与Montassier等早期研究成果一致。原因是Cu对C—C键氢解活性很低,而对C—O键的氢解却表现出良好的反应活性[8]。在以Cu/Cr为催化剂进行的甘油氢解反应中,本文作者课题组的前期工作及前人的研究表明,Cu/Cr催化剂的制备方式对甘油的氢解反应活性有很大的影响,但缺少对不同制备方法制得催化剂的结构的深入认识,本研究利用XRD、BET、TPR、TG、FTIR等对催化剂结构差异进行对比表征研究,并将催化剂的结构表征结果与催化反应性能进行关联分析和讨论;以期深层次地探讨Cu/Cr催化剂的催化活性组分及影响因素。
1 实验部分
1.1 催化剂的制备
采用5种方法制备Cu/Cr催化剂,Cu/Cr原子比为1∶1。
(1)Adkins法[9](A法) 将(NH4)2Cr2O7和氨水的混合液搅拌下滴入80 ℃的Cu(NO3)2水溶液中。沉淀过滤,洗涤,75~80 ℃干燥12 h,研细,在电炉上搅拌分解。10%的乙酸精制,110~115 ℃干燥12 h,300 ℃下焙烧3 h,还原。
(2)铜氨络合沉淀法[10]B法) 将Cu(NO3)2和氨水常温下配成深蓝色溶液,调pH值为11,搅拌下缓慢加入一半(NH4)2Cr2O7溶液,1∶1稀释的浓HNO3调pH值约为6,再加另一半(NH4)2Cr2O7溶液,50 ℃老化4 h,抽滤、洗涤,余下步骤同A法。
(3)Na2CO3沉淀法[11](C法) 将铜和铬的硝酸盐混合溶液,搅拌升温至45 ℃,缓慢加入1 mol/L的Na2CO3溶液,控制时间约30 min,调pH值至9,45 ℃老化2 h,静置、过滤,洗涤,余下步骤同A法。
(4)硅藻土浸渍法(D法) 将铜和铬的混合硝酸盐溶液加入等体积充分干燥好的硅藻土,连续均匀搅拌下浸渍12 h,90 ℃下将水全部烘干,余下步骤同A法。
(5)干混法(E法) 将称量的Cu(NO3)2和(NH4)2Cr2O7固体粉碎研磨,120 ℃下干燥15 h,研磨,300 ℃下焙烧3 h,冷却、研磨、还原。
1.2 催化剂表征
催化剂程序升温还原(TPR)采用天津鹏翔科技有限公司生产的TP5000型多用吸附仪。将200 mg的催化剂样品置于不锈钢的管式反应器中,N2吹扫30 min,升温至100 ℃后切换V(H2)∶V(N2)为1∶4的混合气(H2流量为10 mL/min),以5 ℃/min的升温速率从100 ℃升温至400 ℃。热重(TG)采用德国耐驰STA409PC热重分析仪,升温速率10 ℃/min,样品用量11~15 mg,N2气氛,温度50~800 ℃。采用N2吸附-脱附法,–196 ℃,TriStar3000全自动比表面积与孔隙率分析仪测定样品BET比表面积。测前样品于80 ℃、10-6mmHg(1 mmHg=133.3 Pa)压力下脱气12 h。红外光谱采用美国热电尼高力370FTIR红外光谱仪。催化剂晶相XRD分析采用丹东Y-2000型X射线衍射仪,Cu Kα辐射、石墨单色器,管电压30 kV,管电流20 mA,扫描速度6˚/min,扫描范围2θ= 10˚~80˚。
1.3 甘油氢解反应中催化剂的性能评价
甘油催化氢解反应活性评价在带有机械搅拌装置的100 mL间歇高压反应釜中进行。以水为溶剂,甘油含量50%,氢气压力7 MPa,温度230 ℃,搅拌速度600 r/min,连续反应5 h后迅速冷却。产物用Agilent 6890N型气相色谱仪(FID检测器、HP-5毛细管柱)进行检测,并以正丁醇为内标物采用内标法进行定量分析。
2 结果与讨论
2.1 甘油氢解反应及其催化剂活性评价
研究表明[7],在酸性或中性条件下,甘油的催化氢解按图1所示机理进行。首先,甘油在催化剂的作用下通过分子内脱水生成中间产物烯醇及其酮(醛)式互变异构体,羟基丙酮进一步发生加氢反应生成1,2-丙二醇[3]。
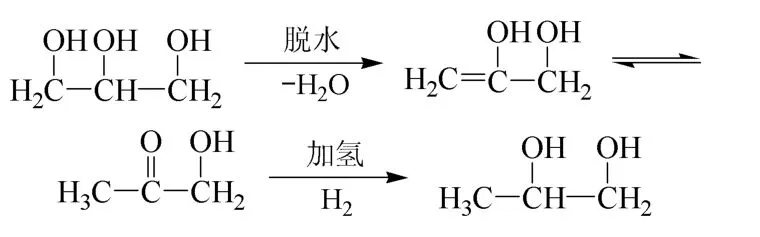
图1 甘油氢解的脱水-加氢机理
表1是不同制备方法得到的催化剂对甘油催化氢解后的转化率、1,2-丙二醇的产率和选择性结果。从表1可看出,不同的制备方式对催化剂的活性有很大的影响,其活性顺序是B法>A法>C法>D法>E法。B法制备的催化剂的活性和选择性最好,分别达到了58.4%和90.6%;而E法制备的催化剂活性虽最差,为25.1%,但选择性较好,达到84.4%;C法、D法制备的催化剂的活性和选择性都较差。显然,在5种制备方法中,用铜氨络合沉淀法制备的催化剂有着明显的优势,在转化率和选择性方面均比其它催化剂要好。
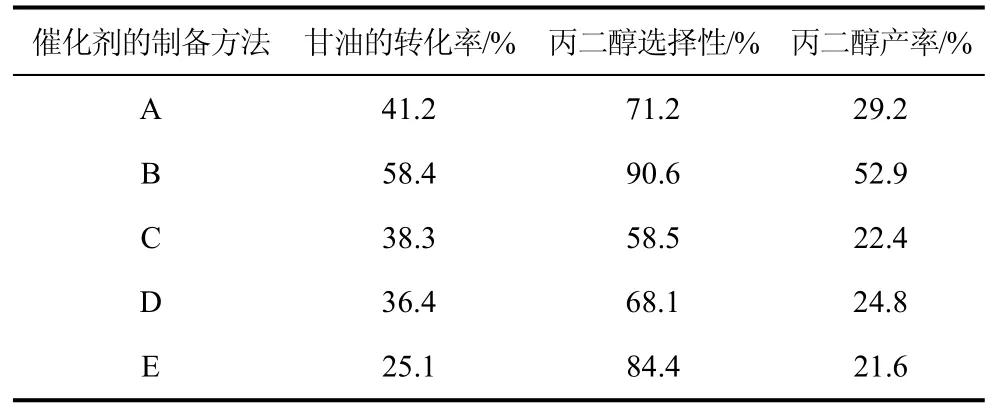
表1 Cu/Cr催化剂的催化氢解反应活性
2.2 催化剂的XRD测试
图2给出5种制备方式还原前的催化剂XRD图。从图5中可发现:由于A法、B法采用相同原料和相似的络合沉淀法,曲线形状大致相同,其催化剂的氧化态(未还原的状态)均存在CuCr2O4、Cr2O3的尖晶石相及其无定形相。CuCr2O4结构和Cr2O3相近,两者可以共生,它们的XRD衍射峰部分重叠较难分辨。仔细分析可发现不同方法制得的催化剂的XRD图也存在细微不同,它们制得的CuCr2O4峰形不同,A法的峰形发生宽化,可能是晶体存在大量缺陷和晶粒太大的缘故;B法峰形较尖,其生成的粒子晶形完整;C法、D法、E法制备的催化剂,其氧化态的XRD峰形平缓,没有突出的特征吸收峰,这表明经高温焙烧分解的氧化态主要是以无定形态存在,催化剂中主要以无定形的铜铬氧化物的形态存在。陈文凯等[12]认为Cu/Cr催化剂中铜的价态会因为制备方法以及使用等因素而有所不同。催化剂的活性与铜的价态以及组分间的互溶程度有关,不同制备方式的催化剂由于其前体不同,经焙烧后的组分及其组分间的互溶度和相互作用不同,进而造成催化剂活性的差异。
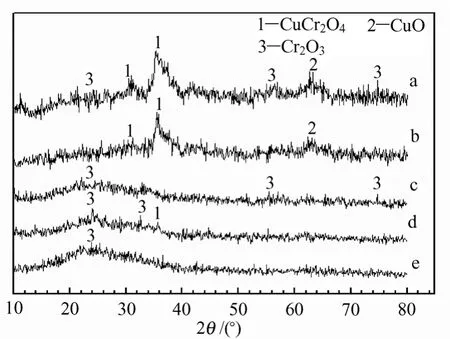
图2 还原前的铜铬催化剂XRD图

图3 还原后的铜铬催化剂XRD图
图3是经氢气还原后催化剂XRD图,还原后的催化剂均出现明显的铜晶体衍射峰,亚铬酸铜晶体峰变小,甚至消失,说明在氢气气氛下催化剂被还原。有人认为这种催化剂在氢气气氛下Cu2+被还原为Cu,少量的Cr2O3被还原为Cr并溶于Cu中,调变了Cu的空d轨道数,使Cu产生了加氢活性[13]。对比不同方法铜的衍射峰,可以看到以A法、B法制备的铜晶体衍射峰较低,这说明还原过程中部分还原为铜晶体,Cu粒径极小或以高分散的形式存在;其原因是由于这两种络合沉淀法焙烧后主要以CuCr2O4形式存在,较其它方法制备的更难被完全还原,形成的Cu能更好地分散到铜铬氧化物中,同时也说明了Cu与Cr2O3之间存在一定的相互作用。C法、E法均出现尖细的衍射峰,峰面积较大,铜主要以铜晶相形式存在。说明在氢气还原气氛下晶粒不断熔合而长大,而晶粒的计算也证实了这点。随着晶粒的增大,Cu的比表面积不断减少;另外,Cu含量的增加和粒径的增大,会造成Cu与Cr相分离,使二者紧密接触部分减少。戎晶芳等[14]、李德经等[15]认为:由于Cr2O3对氢具有很强的亲和力,一定条件下CuO与CuCr2O4或CuO与Cr2O3紧密接触才有很好的加氢活性。郭宪吉等[16]提出催化剂的活性顺序和催化剂中各个组分的晶粒大小、组分间的互溶程度密切相关,组分间互溶较好、晶粒度较小的催化剂具有较高的活性,通过对比不同制备方法得到的催化剂的XRD图谱,再结合其活性,可知铜氨络合沉淀法制备的催化剂活性最佳。
2.3 催化剂热重分析
图4为不同制备方式的催化剂的热重曲线。由图4可知B法、A法制备的催化剂的热重曲线相似,在200~300 ℃都有一个失重峰,其质量分数分别为23.00%、22.25%。失重量存在着细微的差别,其原因可能是由于其形成络合沉淀的环境不同,沉淀在结构和组成上存在细微的差异,这种差异可能与催化剂的组成和价态变化有关。A法在410~700 ℃还有一个平缓的失重峰,为5.90%,此阶段的失重和失重量的大小将直接影响催化剂的性能,催化剂的性能评价结果也印证了这点。C法、D法、E法制备的催化剂由于其形成催化剂的前体不同,热重曲线上的失重峰的失重温度范围和失重量也不同,Na2CO3沉淀法在100~400 ℃失重33.51%,系碱式碳酸铜失重,而650~750 ℃为铬的碳酸盐和亚铬酸铜的分解,这表明Na2CO3沉淀法有少量的亚铬酸铜生成,而XRD测试的结果也证实了亚铬酸铜的存在。干混法在140~260 ℃和480~540 ℃分别为两种组成成分Cu(NO3)2和(NH4)2Cr2O7的失重。从TG分析可知,B法制备的催化剂失重量较A法、C法、D法、E法都要小,其催化剂的活性最好,这表明催化剂的制备方式的不同导致催化剂的前体存在差异,而这种差异直接影响着催化剂的组成以及催化活性。
2.4 催化剂的酸性测试
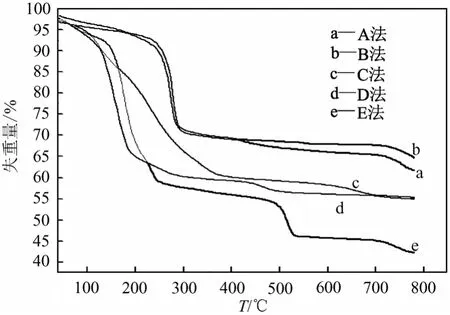
图4 5种制备方式的催化剂的TG谱图
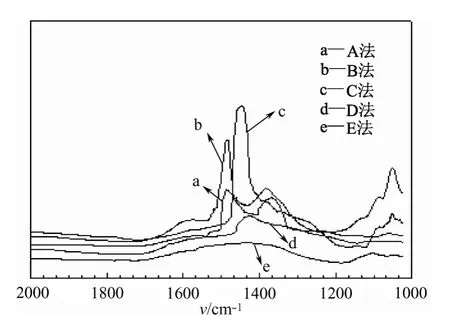
图5 催化剂吸附吡啶的红外光谱图
图5为用A法、B法、C法、D法及E法制备的固体催化剂在高真空干燥后,一定温度和压力下吸附吡啶的红外光谱图。c谱为C法制备的催化剂吸附吡啶的红外光谱图,其在1440~1460 cm-1处有很强的吸收光谱带。这是由于吡啶在催化剂表面上吸附,与L酸络合而成的特征光谱带,表明C法制备的催化剂存在L酸部位,也反映了催化剂中Cu与Cr之间产生了某种相互作用。b谱为B法的吡啶吸附红外光谱图,其最强吸收位于1485~1500 cm-1处,为吡啶与B酸形成的吡啶铵离子的特征吸收谱带。由于催化剂的制备方法和原料相似,以A法制备的催化剂的吡啶吸附的红外光谱图与B法相似,表明这两种络合沉淀法制备的催化剂存在B酸部位。根据Thomas规则,当金属氧化物中加入价数不同或配位数不同的其它氧化物时,由于同晶取代的结果而产生酸性中心。D法催化剂在1378~1484 cm-1存在一个弱的吸收谱带;E法制备的催化剂在1400~1550 cm-1处都不存在特别的吸收谱带,说明这2种方法制备的催化剂没有典型的B酸和L酸位。对比几种催化剂吸附吡啶的红外谱图,其特征吸收谱带和面积存在明显差异,以B法、C法制备的峰面积较大,说明含酸中心数量较多,但D法制备的由于催化剂铜铬的互溶度较差,协同作用不强,加上比表面积较小,晶粒过大,虽然含有较多酸中心,但其催化活性不强。结合实验结果可发现,酸性催化剂能促进甘油的催化氢解,而含有B酸位的催化剂催化活性更高。
2.5 催化剂的BET、孔容和粒度
表2中列出了几种不同制法得Cu/Cr催化剂的比表面积、孔容和粒度数据。从表2中可知制备方法对催化剂的比表面积影响很大,比表面积和催化剂活性从大到小基本一致,为B法>A法>C法>D法>E法,用粒度分析仪测定的各分散粒子的粒度大小也与比表面积的大小完全一致。B法、A法所用的试剂相同,但由于温度、加料方式以及溶液pH值的不同,使得形成沉淀时环境存在差异,温度越高,其老化时越容易引起粒子的聚集;微粒增大,比表面积变小。一定的酸性环境和pH值有利于铜离子与氨形成铜氨络合物沉淀,减少铜离子溶于溶液而流失活性组分,增加催化剂的活性中心。Na2CO3沉淀法形成碱性条件下的碱式碳酸盐沉淀,粒子较络合沉淀时更易聚集,分散不够均匀,比表面积变小。浸渍法虽能有效地保留化学组分,但组分间的溶合和相互作用显然没有形成沉淀强。而干混法只是简单的机械混合,其粒子的粉碎、分散程度没有在溶液中形成沉淀分散得均匀。
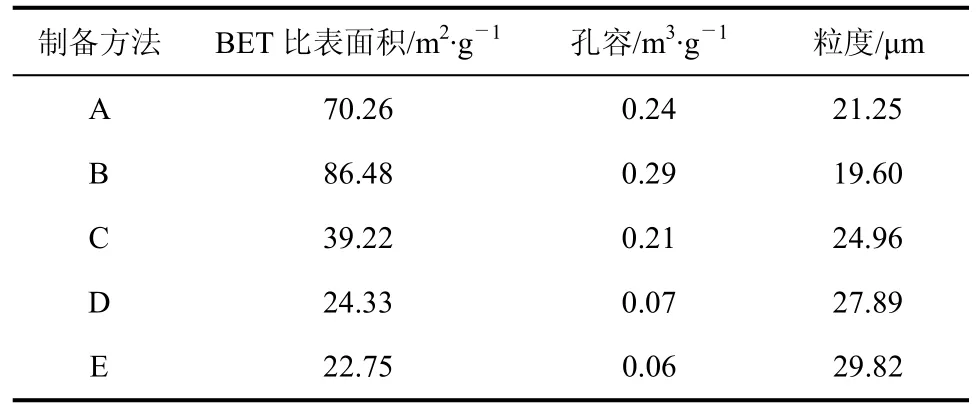
表2 Cu/Cr催化剂的比表面、孔容和粒度
催化剂的活性与反应可利用的比表面积和活性中心数量密切相关,大的比表面积可增加活性组分负载量,从而增加活性中心数目。表2中还可发现催化剂的活性与BET比表面积呈正比。大的比表面积能提高催化剂的有效因子和增大单位面积上活性位浓度以及催化剂与反应物的接触面积。孔容的增大有利于加快扩散速率,提高催化剂的内表面利用率,从而提高催化剂的活性。比较可以看出,制备方式的差异显著影响着催化剂的比表面积和氢解活性,比表面积较大、分散更均匀的B法制备的催化剂活性最好。
2.6 催化剂的TPR表征
图6为不同制备方式催化剂的TPR图。由图6可知,不同制备方法得到的催化剂的还原温度及其还原性能有明显的差异,其中B法还原温度最低,为209℃,A法224℃、C法262℃、D法244℃、E法251℃。戎晶芳等[14]对铜铬氧化物催化剂的TPR表征结果表明,CuCr2O4和CuO 的还原温度约500 K,Cu2+→Cu+的还原温度约为471 K,而Cu+→Cu的还原温度约为536 K。A法、B法催化剂的前体都是铜氨络合铬酸盐沉淀,他们焙烧后易形成复合氧化物而使得还原温度前移,同时以共沉淀法制备得到的催化剂晶粒最小,焙烧过程中铜的氧化物组分已熔进Cr2O3晶格中,铜铬之间溶合调变,协同作用增强。当然这两种方法制备的催化剂,由于沉淀的条件和环境的细微差异,造成它们的最佳还原温度(209 ℃、224 ℃)和还原峰面积的不同,催化活性也有所差异。C法、D法、E法制备的催化剂由于其形成条件和催化剂的前体不同,它们之间形成了较大晶粒的铜铬氧化物,较前两种相比,其还原温度相对升高,加上含铜组分在催化剂表面分布不够均匀,局部地区形成堆积,使得铜铬组分之间不能有效互溶,催化剂的活性自然也就降低。金属氧化物的还原温度取决于金属本身的性质及其周围的环境,反映了催化剂中氧化物的脱氧能力和催化剂的催化性能。文献[17]认为催化剂的还原峰越高,峰面积越大,其催化剂的活性越高。比较5种制备方式发现,B法制备的催化剂还原温度较低,峰面积较大,同时铜铬之间能很好地溶合调变,产生协同作用,因此催化活性最佳。
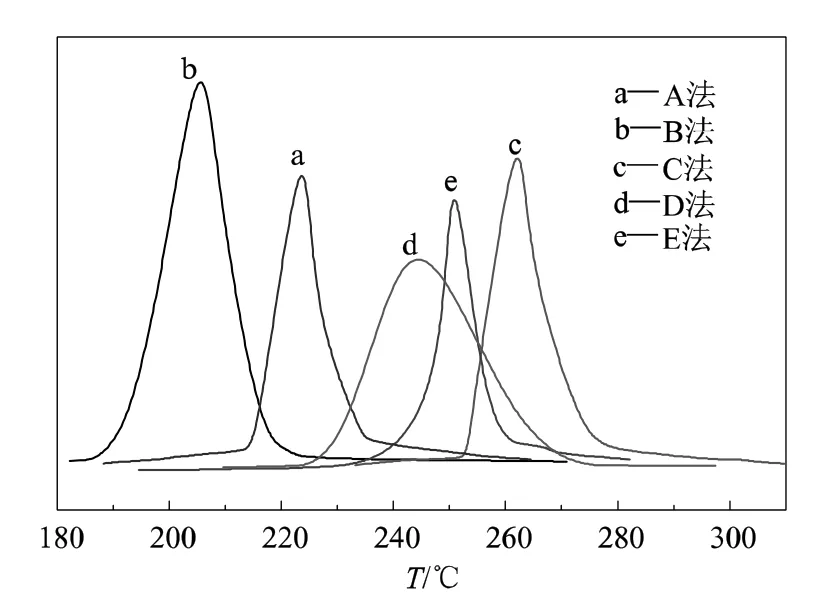
图6 5种制备方式的Cu/Cr催化剂的TPR图
3 结 论
铜铬催化剂制备方式不同,极大地影响着其对甘油的催化氢解反应。在所用的5种催化剂中,以铜氨络合沉淀法制备的催化剂,因能更好地提高催化剂的比表面积,降低铜原子自身的结晶度,降低催化剂的TPR还原温度以及促进铜铬氧化物晶相的有效溶合调变而具有更好的加氢活性和氢解性能。Adkins法、Na2CO3沉淀法制备的催化剂,由于沉淀环境和催化剂前体不同,BET比表面积降低、催化剂活性组分减少和晶粒增大,TPR还原温度升高而氢解效果次之;硅藻土浸渍法的催化剂由于活性组分含量较低,活性物种进入载体,外表面上活性物种减少,氢解性能较沉淀法也有所减弱;而干混法制备的催化剂,只是简单的物理混合和高温焙烧,铜铬氧化物不能很好地溶合调变,互溶度降低,协同作用减弱,活性最低。
[1] Werpy T,Petersen G. Top value added chemicals from biomass,1,Results of screening for potential candidates from sugars and synthesis gas[R].US DOE Report.2004.
[2] 冯建,袁茂林,陈华,等.甘油催化氢解的研究和应用[J].化学进展,2007,19(5):651-658.
[3] 赵洵,许张乔,曹发海.生物质甘油制备1,3-丙二醇的研究进展[J].合成技术及应用,2007,22(1):29-32.
[4] 许赟珍,欧先金,郭妮妮,等.生物柴油副产物甘油的高附加值利用[J].过程工程学报,2008,8(4):695-702.
[5] Werpy T A, Frye J G,Zacher A H,et al.Hydrogenolysis of 6-carbon sugars and other organic compounds:US,6841085B2[P]. 2005-01-11.
[6] Perosa A, Tundo P.Selective hydrogenolysis of glycerol with Raney nickel[J].Ind.Eng.Chem.Res.,2005,44:8535-8537.
[7] Dasari M A,Kiatsimkul P P,Sutterlin W R,Suppes G J. Low-pressure hydrogenolysis of glycerol to propylene glyceroll [J].Appl. Catal. A:General,2005,281:225-231.
[8] Runeberg J,Baiker A,Kijenski J.Copper catalyzed amination of ethylene glycerol[J].Appl. Catal.,1985,17(2):309-319.
[9] Adkins H,Connor R.The catalytic hydrogenation of organic compounds over copper chromitej[J].J. Am. Chem. Soc.,1931,53:1091-1095.
[10] 吴玉塘, 陈文凯,刘兴泉,等.铜铬催化剂的制备方法:中国,1136979A[P].1995-05-30.
[11] 丁建飞,李秋小,李永胜. Cu - Cr催化N,N-二甲基十二烷基酰胺加氢[J].石油化工, 2006,35(6):557-560.
[12] 陈文凯,杨迎春,刘兴泉,等.低温液相合成甲醇铜基催化剂的表征[J].分子催化,2002,16(4):289-291.
[13] 金松寿. 量子化学基础及其应用[M].上海:科学技术出版社,1980.
[14] 戎晶芳,黄维,陆文云,等.铜铬氧化五催化剂的结构与性能研究[J].化学物理学报,1994,7(3):254-262.
[15] 李德经,刘红涛,谭丕亨,等.铜铬氧化物催化剂在苯乙酮加氢中的活性组成研究[J].催化学报,1998,8(1):87-92.
[16] 郭宪吉,齐化多,徐三魁,等.铜基甲醇合成催化剂的表征及铜、锌组分间的相互作用[J].天然气化工,2000,25(5):36-39.
[17] Long Y,Chu W,Ye Y H,et al.Hydrogenolysis of methyl formate to methanol on novel copper-based catalysts[J].Studies in Surface Science and Catalysis,2004,147:613-688.
Influence of preparation methods of Cu/Cr catalyst for hydrogenolysis of glycerol
OU Jianxiong,LAN Zhili,YIN Dulin,YANG Chunhua,OU Lanying
(Institute of Fine Catalysis and Synthesis,Hunan Normal University,Changsha 410081,Hunan ,China)
Cu/Cr catalyst exhibits superior catalytic hydrogenolysis activity in glycerol hydrogenolysis to 1,2-propanediol for its efficient hydrogenolytic activity towards C—O bond and poor activity towards C—C bond. Cu/Cr catalysts were prepared by different methods and examined for the glycerol hydrogenolysis reaction. Experimental results indicated that preparation methods have large effects on the glycerol hydrogenolysis. Among five catalysts prepared,the catalytic hydrogenolysis activity was found in the order of copper ammonia complexation method > Adkins method > sodium carbonate method > diatomite impregnation method > dry-mixed method. XRD,TG,BET,FT-IR and TPR were used to measure and analyse the structural differences of catalysts prepared by different methods. The correlation and structural effect with catalytic performance were also analysed and discussed.
catalytic hydrogenolysis;copper-chromium catalyst;preparation methods;glycerol
O643
A
1000–6613(2010)04–0659–06
2009-09-16;修改稿日期:2009-12-10。
湖南省自然科学基金资助项目(05JJ30024)。
欧建雄(1977—),男,硕士研究生。联系人:兰支利,教授。电话 0731-88872576;E-mail lanzl@hunnu.edu.cn。
