SNAI1在85例结直肠癌患者组织中表达的研究
2010-09-20赵海燕吴共发王雅娟韩慧霞
赵海燕 吴共发 王雅娟 韩慧霞
1.南方医科大学附属南方医院病理科,广东 广州 510515;2.南方医科大学基础医学院病理学系,广东 广州 510515
结直肠癌是最常见的恶性肿瘤之一 ,在美国已经成为肿瘤死亡的首因;在上海也逐渐超过胃癌成为第二常见的恶性肿瘤[1]。以往研究发现上皮-间质转化(epithelial-mesenchymal transition,EMT)参与了恶性肿瘤的侵袭和转移, SNAI1通过抑制E-钙黏蛋白(E-cadherin)的表达触发EMT的发生,导致癌细胞丧失上皮特性,富于侵袭和转移特性,是恶性肿瘤所必需的[2]。关于SNAI1的研究已经多见报道,但是尚无采用配对方法比较结直肠癌组织和淋巴结转移组织中SNAI1表达的研究。在本研究中,我们通过免疫组织化学法检测85例结直肠癌患者的癌旁正常黏膜组织、结直肠癌组织和淋巴结转移癌组织中SNAI1的表达情况,采取多种分组和多种统计方法对数据进行详细分析比较,探讨SNAI1在结直肠癌中的意义。
1 资料和方法
1.1 标本来源 收集南方医科大学附属南方医院病理科2007年1月1日—2008年3月1日存档的85例结直肠癌患者(高分化腺癌26例、中分化腺癌23例、低分化腺癌36例;Dukes A+B 45例,Dukes C+D 40例)的137个蜡块,癌旁正常黏膜组织22例(距癌灶15 cm以上)和淋巴结转移癌组织30例均来自于85例结直肠癌患者。患者年龄23~85岁(平均57.2岁),术前均未接受化疗、放疗。所有组织4%甲醛固定,常规石蜡包埋,3 μm厚切片,采用免疫组织化学二步法进行检测。
1.2 试剂 SP法检测试剂盒和DAB显色试剂盒均购自北京中杉公司;SNAI1兔抗人多克隆抗体购自美国Bioworld公司。
1.3 SP法检测SNAI1的表达 免疫组织化学方法按试剂盒说明书操作。SNAI1抗体的工作浓度为1∶200,0.01 mol/L柠檬酸盐缓冲液抗原修复,SP法检测试剂盒,DAB显色,苏木精复染,中性树胶封固。PBS取代一抗作阴性对照。
1.4 结果判断标准 胞核出现棕黄色颗粒为阳性,⑴强度分数标准:无色为0分,淡黄色为1分,棕黄色为2分,棕褐色为3分。⑵随机选择10个高倍视野,每个视野计算100个肿瘤细胞,共计数1 000个肿瘤细胞,计算阳性细胞百分率:1%~<25%为1分,25%~<50%为2分,50%~<75%为3分,≥75%为4分。两项得分相乘,4~7分为“+”,8~11分为“++”,满12分为“+++”,“+~+++”为阳性表达。
1.5 统计处理 采用SPSS 13.0统计软件进行处理,多组比较采用Kruskal-Wallis检验,两两比较采用Mann-Whitney U 检验,双变量相关分析采用Spearman和Kendall’s tau-b检验,双侧检验,P<0.05为差异具有统计学意义。
2 结 果
2.1 SNAI1在正常结直肠组织、癌组织和淋巴结转移灶组织中的表达 免疫组化结果显示,SNAI1表达主要定位在细胞核内(图1)。多组比较显示,SNAI1在正常结直肠黏膜组织、原发癌灶及淋巴结转移癌组织中的表达明显不同,差异具有统计学意义(χ2=50.496,P=0.000),以淋巴结转移癌中的表达最强。两两比较发现,SNAI1在原发性结直肠癌组织中的表达显著高于正常结直肠黏膜组织中的表达(Z=-6.018,P=0.000);低分化癌组织的表达显著高于高中分化癌组织(Z=-2.467,P=0.014),SNAI1在Dukes A+B与Dukes C+D分期中的表达差异无统计学意义(Z=-0.975,P=0.330)。双变量相关分析显示组织类别(即正常结直肠黏膜组织、高分化癌组织、中分化癌组织、低分化癌组织和淋巴结转移癌组织)与SNAI1的表达呈显著正相关(Kendall’s tau-b相关系数r=0.532>0.5,P=0.000;Spearman’s 相关系数r=0.595>0.5,P=0.000,表1)。
2.2 SNAI1在高、中、低分化癌与其淋巴结转移癌的对比表达 淋巴结转移灶癌组织的表达显著高于原发性结直肠癌组织(Z=-3.446,P=0.001,表1),但剔除无淋巴结转移的原发性结直肠癌后,发现原发性结直肠癌组织与其淋巴结转移癌组织的表达差异并无统计学意义(χ2=4.785,P=0.188,表2)。
2.3 SNAI1表达与淋巴结转移的相关分析 双变量相关分析显示淋巴结转移与SNAI1的表达呈显相关(Kendall’s tau-b 相关系数r=0.209<0.5,P=0.01;Spearman’s 相关系数r=0.221<0.5,P=0.009)。

图1 SNAI1在不同组织中的表达Fig.1 Expression of SNAI in different tissues(SP, ×200)
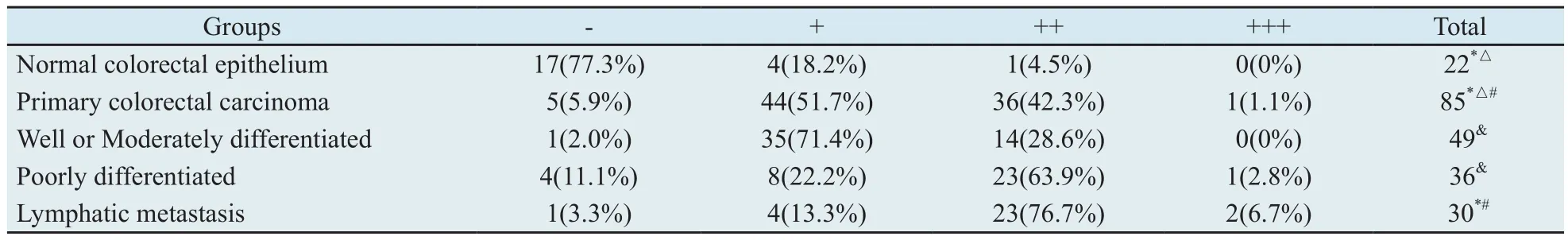
表1 SNAI1在正常结直肠组织、结直肠癌组织和淋巴结转移组织中的表达情况Tab.1 Expression of SNAI in normal colorectal epithelium, colorectal carcinoma and lymph node metastases
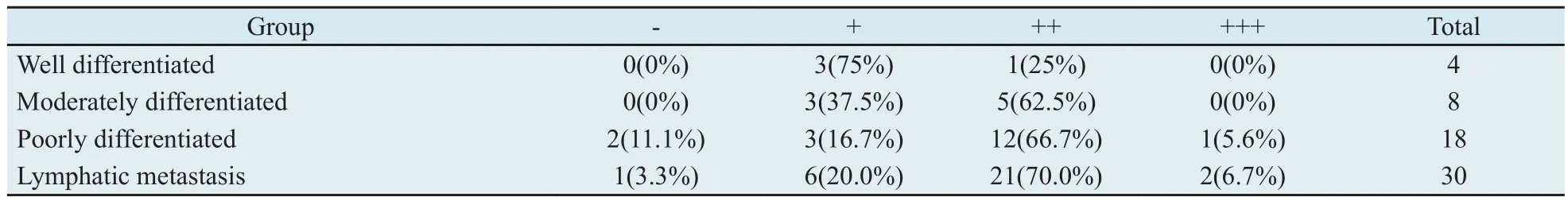
表2 SNAI1在高、中、低分化癌与其淋巴结转移癌的对比表达情况Tab.2 Comparison of SNAI1 in well, moderately, poorly differentiated carcinoma and paired lymphatic metastasis
3 讨 论
SNAI1是锌指转录因子家族成员之一,这个家族成员还有E12/E47、ZEBl、SIPl和Slug等,其家族具有相似的结构,由一个高度保守的羧基末端及一个高度可变的氨基末端构成,其家族成员结构上的差异主要表现在中间P-S富集区域[3]。SNAI1是一个能诱导EMT的锌指转录因子[4],可以促进癌细胞在早期发生侵袭和转移[5]。SNAI1在上皮细胞的表达能促进在基因表达层面的成纤维表型的出现,这种表型具有侵袭和迁移的潜能和特性[6]。 最重要的是,SNAI1能够直接抑制E-cadherin的表达,而E-cadherin是负责细胞上皮表型如细胞极性、细胞和基质的黏附能力的主要成分[7]。SNAI1通过与E-cadherin启动子区域的E-box结合,直接抑制E-cadherin表达,破坏上皮细胞之间的连接,使癌细胞松散,易于发生迁移,促进EMT的发生,与肿瘤的浸润、转移、复发密切相关[8]。Larue等[9]描述,在中胚层与神经嵴的前体中,SNAI1通过下调E-cadherin而触发上皮细胞向间充质细胞的转变。E-cadherin表达丢失被认为是EMT最显著的特征[10-11]。EMT是细胞丧失上皮特征例如细胞极性,细胞连接和获得间质特性如增加运动性的一种形态学过程[12]。它最初在胚胎发育过程中如原肠胚形成阶段,肾器官发育及神经嵴形成中被描述[13],大量的研究表明EMT被认为是肿瘤演进及转移的基本过程,是良性肿瘤向高侵袭性肿瘤转换所必需的过程[14]。由此可以看出,SNAI1确实是肿瘤恶性的标志。在本研究中,免疫组化结果显示,SNAI1在正常结直肠黏膜、原发癌灶及淋巴结转移癌组织中的表达明显不同,差异具有统计学意义(P<0.05),以淋巴结转移癌的表达最强。两两比较发现,SNAI1在原发性结直肠癌组织中的表达显著高于正常结直肠组织中的表达(P<0.05);低分化癌组织的表达显著高于高中分化癌组织(P<0.05),SNAI1在Dukes A+B与Dukes C+D分期中的表达差异无统计学意义 (P>0.05),且双变量相关分析显示组织类别与SNAI1的表达呈显著正相关(相关系数r>0.5,P<0.05),相关关系非常密切。据此推断,SNAI1可以作为结直肠癌恶性程度的评估指标。
淋巴结转移灶癌组织的表达显著高于原发性结直肠癌组织 (P<0.05),这个结果与高维哲等[15]的研究结果一致。但剔除无淋巴结转移的原发性结直肠癌病例后,发现原发性结直肠癌组织与其淋巴结转移癌组织的表达差异并无统计学意义(P>0.05)。我们认为,这种将来自同一个患者的原发癌灶和淋巴结转移癌进行比较的方法更具可比性和严谨性。我们由此推测,在结直肠癌中,淋巴结转移癌的癌细胞恶性程度并不比原发癌灶的强,但这需要进一步的分子生物学方面的研究。
我们将淋巴结转移和SNAI1这两个变量进行双变量相关分析,发现两者显著正相关(P<0.05),即SNAI1表达水平越高则淋巴结转移概率也越大。根据以往研究[15],在结直肠癌中,SNAI1表达弱者转移的发生率低,表达强者其转移发生率高。出现这种联系的原因应该是SNAI1通过直接抑制E-cadherin的表达,促进EMT,使癌细胞具有转移能力[8]。综上所述,我们认为在临床中,通过检测结直肠癌的SNAI1水平,可能可以作为患者是否有淋巴结转移风险的预测指标。
SNAI1 在结直肠癌中表达与EMT及转移等关系的分子生物学机制已经有报道[8,16-17]。另外,有研究指出拮抗SNAI1作用逆转调控EMT及肿瘤的体外转移潜能[18]。在此基础上有望寻找出一种结直肠癌防治的新方法。
[1] 廉朋,蔡国响,徐烨,等.PRL-3基因在结直肠癌原发灶中的表达及其临床意义[J].中国癌症杂志,2006,16(10):823-827.
[2] Olmeda D, Moreno-Bueno G, Flores JM, et al.SNAI1 is required for tumor growth and lymph node metastasis of human breast carcinoma MDA-MB-231 cells [J].Cancer Res,2007,67(24):11721-11731.
[3] Ikenouchi J, Matsuda M, Furuse M, et al.Regulation of tight junctions during the epithelium-mesenchyme transition: direct repression of the gene expression of claudins/occludin by Snail[J].J Cell Sci,2003,116(Pt 10):1959-1967.
[4] Nieto MA.The snail superfamily of zinc-finger transcription factors [J].Nat Rev Mol Cell Biol,2002,3(3):155-166.
[5] Peinado H, Olmeda D, Cano A.Snail, Zeb and bHLH factors in tumour progression: an alliance against the epithelial phenotype? [J].Nat Rev Cancer,2007,7(6):415-428.
[6] Guaita S, Puig I, Franci C, et al.Snail induction of epithelial to mesenchymal transition in tumor cells is accompanied by MUC1 repression and ZEB1 expression [J].J Biol Chem,2002,277(42):39209-39216.
[7] Perez-Moreno M, Jamora C, Fuchs E.Sticky business:orchestrating cellular signals at adherens junctions [J].Cell,2003,112(4):535-548.
[8] Cano A, Pérez-Moreno MA, Rodrigo I, et al.The transcription factor snail controls epithelial-mesenchymal transitions by repressing E-cadherin expression [J].Nat Cell Biol,2000,2(2):76-83.
[9] Larue L, Bellcosa A.Epithelial-mesenchymal transition in development and cancer: role of phosphatidylinositol 3’kinase/AKT pathways [J].Oncogene,2005,24(50):7443-7454.
[10] Thiery JP.Epithelial-mesenchymal transitions in tumour progression [J].Nat Rev Cancer,2002,2(6):442-454.
[11] Kang Y, Massagué J.Epithelial-mesenchymal transitions: twist in development and metastasis [J].Cell,2004,118(3):277-279.
[12] Berx G, Raspe E, Christofori G, et al.Pre-EMTing metastasis?Recapitulation of morphogenetic processes in cancer [J].Clin Exp Metastasis,2007,24(8):587-597.
[13] Shook D, Keller R.Mechanisms, mechanics and function of epithelial-mesenchymal transitions in early development[J].Mech Dev,2003,120(11):1351-1383.
[14] Duband JL, Monier F, Delannet M, et al.Epitheliummesenchyme transition during neural crest development[J].Acta Anat(Basel),1995,154(1):63-78.
[15] 高维哲,李建明,杨发达,等.锌指转录因子Snail在结直肠癌中的表达及其意义[J].南方医科大学学报,2008,28(2):162-165.
[16] 杨发达,李建明,周军,等.人大肠癌细胞PRL-3基因启动子Snai1结合位点的初步研究[J].南方医科大学校报,2007,27(4):401-405.
[17] Peña C, García JM, Larriba MJ, et al.SNAI1 expression in colon cancer related with CDH1 and VDR downregulation in normal adjacent tissue [J].Oncogene,2009,28(49):4375-4385.
[18] 张阿丽,王全胜,钟亚华,等.转录因子Snai1调控上皮-间质转型及对肿瘤转移的逆转作用[J].癌症,2005,24(11):1301-1305.
