盐巴戟天炮制工艺的优化
2010-09-19马雪松佟连琨姜永粮
邹 兵 马雪松 佟连琨 姜永粮*
1 辽宁省鞍山市食品药品检验所(114006)
2 辽宁中医药大学附属医院(110032)
3 辽宁中医药大学(116600)
巴戟天为茜草科植物巴戟天(Morinda officinalis How.)的干燥根,味甘辛,性微温,有补肾阳、强筋骨、祛风湿之功效[1]。巴戟天始载于《神农本草经》,列为上品,历代本草均有记载。是我国著名的“四大南药”之一,用于阳痿遗精,宫冷不孕,月经不调,少腹冷痛,风湿痹痛,筋骨痿软等症。巴戟天中含有蒽醌、多糖、寡糖、脂类、有机酸等11类化合物及24种无机元素[2]。巴戟天的化学成分及其药理作用已有部分研究[3,4],陈小娟等[5]探讨了巴戟多糖的免疫作用,认为其能增加幼年小鼠的胸腺的重量,提高小鼠巨噬细胞吞噬百分率和小鼠脾脏免疫特异玫瑰花结形成细胞的形成;巴戟天多糖可以提高果蝇性活力,并显著提高果蝇新生幼虫的羽化率,认为巴戟天多糖具有明显的补肾壮阳作用[6]。巴戟天寡糖具有明显的补肾壮阳作用,属于巴戟天补肾壮阳作用的有效成分之一[7]。临床上一般用盐巴戟天,炮制后寡糖变化如何?尚无人考察,因此我们测定了巴戟天中补肾壮阳的主要成分耐斯糖和多糖的含量,并以此为指标确定了盐巴戟天的炮制工艺。
1 仪器与试药
1.1 仪器
岛津LC-20AB液相色谱仪;LC-Solution色谱数据工作站;电雾式检测器(美国惠泽公司);UV-3010紫外分光光度计;METTLER AE240型十万分之一分析天平(瑞士METTLER)。
1.2 试药
生品巴戟天药材购自广东德庆种植基地,经辽宁中医药大学中药鉴定教研室翟延君教授鉴定为茜草科植物巴戟天(Morinda officinalis How.)的干燥根;盐(市售);耐斯糖对照品(购自sigma公司,纯度>98%);D-无水葡萄糖对照品(购自中国药品生物制品检定所,批号:110833-200503)。
2 方法与结果
2.1 耐斯糖含量测定
2.1.1 对照品溶液的制备
取耐斯糖对照品适量,精密称定,置50mL量瓶中,加流动相,甲醇-水 (3∶97),制成每1mL含0.2148mg的溶液,即得。
2.1.2 盐巴戟天样品的制备
取净巴戟天,加盐水拌匀,置适宜的容器内,加热蒸透或至规定的程度时,趁热除去木心,切段,干燥[8]。
2.1.3 供试品溶液的制备
取本品粉末(过三号筛)0.5g,精密称定,置具塞锥形瓶中,精密加入流动相50mL,密塞,称定重量,加热回流30min,放冷,再称定重量,用流动相补足减失的重量,摇匀,静置,取上清液用微孔滤膜(0.45μm)滤过,取续滤液即得[9]。
2.1.4 测定条件
色谱柱:Diamonsil C18(5 μm,250mm×4.6mm);流动相∶甲醇-水 (3∶97);柱温:30℃;流速:0.8mL/min;进样量10 μL。
在上述色谱条件下,该分析条件良好,符合定量分析要求。耐斯糖对照品、生品巴戟天及盐巴戟天HPLC色谱图分别见图1。
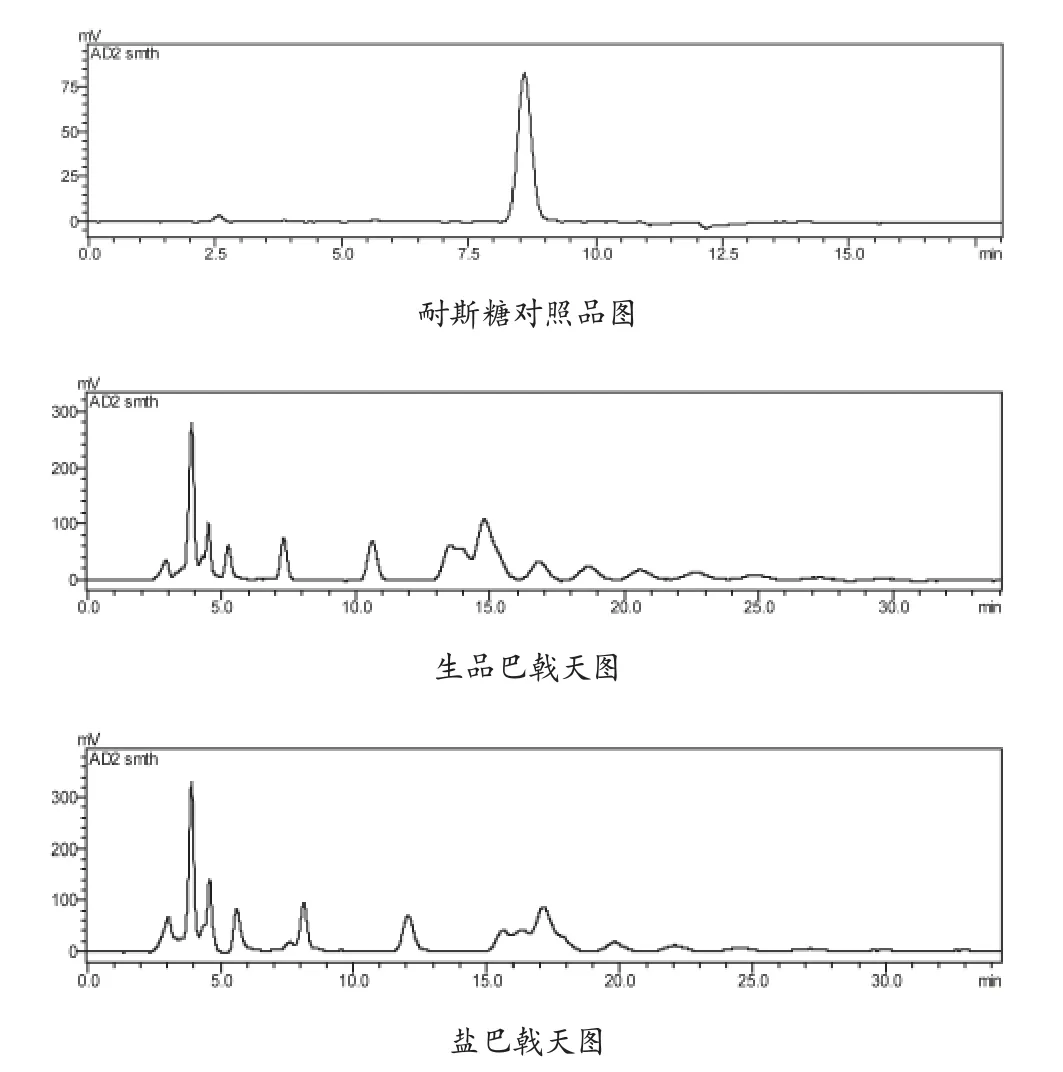
图1 巴戟天HPLC图
2.1.5 线性范围考察
取耐斯糖对照品适量,精密称定,置50mL量瓶中,加流动相,甲醇-水 (3∶97),制成每1mL含0.2148mg的溶液,即得。
精密吸取浓度为0.2148mg的耐斯糖对照品溶液10、20、30、40、50μL,进样分析,测定色谱峰面积分别为830474、1536942、2163688、2832726、3462176。以耐斯糖对照品进样量(μg)为横坐标,耐斯糖色谱峰面积积分值为纵坐标,得耐斯糖线性回归方程为:Y=305363X-197445,相关系数r=0.9998。表明耐斯糖的进样量在2.148~10.740μg范围内与峰面积呈良好的线性关系。
2.1.6 精密度试验
精密吸取上述配制的耐斯糖对照品溶液,连续进样6次,每次20μL,按上述色谱条件,测定色谱峰面积,RSD为1.4%,测定结果表明,本实验精密度符合有关规定。
2.1.7 稳定性试验
按2.1.3,2.1.4项下制备供试品溶液,精密吸取同一供试品溶液各10μL,分别在0时、4时、8时、12时、16时、24时,进样分析,测定色谱峰面积,RSD为1.6%,实验结果表明,供试品制备后24h内化学性质稳定。
2.1.8 重复性试验
取巴戟天样品粉末6份,按2.1.3、2.1.4项下制备供试品溶液,连续进样6次,每次10μL,结果RSD为1.8%测定结果表明,本实验重现性良好。
2.1.9 加样回收率试验
取已知耐斯糖含量的盐巴戟天样品6份,每份约0.25g精密称定,分别精密加入耐斯糖对照品适量,按2.1.3、2.1.4项下制成供试品溶液,测定结果表明,耐斯糖平均回收率为100.73%,RSD为1.3%。测定结果符合有关规定。
2.2 巴戟天中多糖的含量测定
2.2.1 巴戟天多糖的精制
称巴戟天(三号筛)50g,加80%乙醇200mL浸渍24 h,85℃回流提取2次,每次1.5 h,过滤,药渣加蒸馏水500mL浸泡1 h;90℃温浸50min,抽滤,滤渣加120mL蒸馏水浸泡过夜,过滤,合并滤液;在电子万用炉上加热,浓缩至70mL,每30mL浓缩液加10mL氯仿萃取,萃出液呈棕色黏稠液;合并浓缩液约70mL加入0.75g活性炭脱色,加热90℃抽滤,滤液浓缩至60mL,加95%乙醇250mL摇匀,静置于冰箱;过滤,以95%乙醇多次洗涤,无水乙醇,乙醚,丙酮每次10mL 3次洗涤,60℃烘干,备用[10]。
2.2.2 对照品溶液的制备
精密量取10.0mg D-无水葡萄糖于250mL量瓶中,加蒸馏水溶解并稀释至刻度,制成浓度为0.1mg/mL储备液。
2.2.3 测定条件
按制备方法项下操作制备对照液、供试液和空白液,在400~800nm波长范围内进行光谱扫描,均在484nm处均有最大吸收值,故选定484nm作为含量测定的最大波长。
2.2.4 标准曲线的绘制
精密量取葡萄糖标准液(100mg/L)0.10、0.20、0.40、0.60、0.80、1.00、1.20mL于25mL具塞比色管中,加蒸馏水至2.00mL,再各加5%苯酚溶液1.60mL摇匀,迅速加入浓H2S04溶液7.50mL,振摇5min,放置10min,置沸水浴中加热20min,取出冷却至室温;于484nm,以试剂空白为参比测定吸光度。以葡萄糖浓度(C)为横坐标,吸光度(A)为纵坐标,得回归方程:Y=11.79X+0.0155,r=0.9997,结果表明,D-无水葡萄糖溶液浓度在0.005~0.06mg/mL的范围内与与吸收值有良好的线性关系。
2.2.5 换算因子的测定
精密称取已制备巴戟天多糖5.0mg,加蒸馏水溶解,转移至25mL容量瓶中,并稀释至刻度,摇匀制得巴戟天多糖储备液;吸取多糖储备液2.0mL,置于10mL容量瓶中,加水定容;吸取上述溶液2.0mL加5%苯酚溶液1.60mL摇匀,迅速加入浓H2S04溶液7.50mL,振摇5min,放置10min,置沸水浴中加热20min,取出冷却至室温;于484nm,以2.0mL水作空白对照,测定吸光度,由回归方程求出此巴戟天多糖储备液中葡萄糖的浓度,按如下公式求换算因子:f=m/(C×D×V),式中m为巴戟天多糖的质量(mg),C为巴戟天多糖储备液中葡萄糖浓度(mg/L),D为巴戟天多糖的稀释倍数,V为体积(mL)[10](表1)。

表1 换算因子的测定
由表可得,换算因子平均值为1.2361,RSD=0.12%,表明精密度良好。
2.2.6 供试品溶液的制备
取盐巴戟天样品适量,粉碎,取过三号筛约0.2000g,于圆底烧瓶内,加150mL 80%的乙醇,于90℃水浴回流1h,过滤,滤渣中加150mL蒸馏水,90℃水浴1h,过滤,残渣用热水洗4次,每次10mL,合并滤液,转入250mL容量瓶中,定容。吸取2mL用蒸馏水定容至10mL,即得供试品溶液。
2.2.7 样品的测定
吸取供试品溶液2.0mL,按2.2.4项下的操作,依据回归方程求供试品液的浓度,并且转换成百分含量。多糖质量分数 W% = (C×D×f/m )×100%,式中: C为葡萄糖的浓度,D为多糖稀释因素,f为换算因子,m为样品质量。
2.2.8 精密度试验
取一定浓度的标准品溶液,按上述条件,连续6次测定吸光度,测定RSD 为1.0%,结果表明,本实验精密度符合有关规定。
2.2.9 稳定性试验
取供试品溶液2.0mL,按照2.2.4项下方法显色后,室温下放置,在上述光谱条件下于0、2、4、6、8、10、12h时间间隔,分别测定样品吸光度,测定RSD为1.7%,实验结果表明,供试品组分化学性质稳定。
2.2.10 重复性试验
取巴戟天样品粉末六份,按2.2.6项下制备供试品溶液,连续进行测定六次,计算总多糖含量,测定RSD为0.8%,结果表明本实验重现性良好。
2.2.11 加样回收率试验
取已知多糖含量的巴戟天样品6份,每份约0.1g,分别加入D-无水葡萄糖对照品适量,按2.2.6、2.2.7项下操作,测定样品吸光度,葡萄糖平均回收率为99.92%,RSD为1.3%,结果符合有关要求。
3 盐巴戟天工艺优选
3.1 盐巴戟天样品的制备
取药材每份50g,于煤气炉上密闭按盐蒸要求用蒸锅蒸制。
3.2 样品溶液的制备及测定
按2.1.3、2.2.6项下要求制备各供试品溶液。并分别于2.1.4、2.2.3及2.2.4项下条件测定耐斯糖及巴戟天中多糖的含量,进行分析。
3.3 单因素考察
3.3.1 盐溶液用量考察
取生品巴戟天5份,每份50g,置密闭容器内,分别加入已配好的2%盐溶液30、40、50、60、70mL,拌匀闷润,待盐水被吸尽后,蒸30min后出锅,烘干,粉碎,过60目筛,备用。取各样品,按上述供试品溶液的制备方法和色谱条件进行测定,结果见表2。
由表2可以看出在加盐水量为每50g药材用盐水50mL时,指标性成分含量的综合评分最高,因此选择50mL盐水为最佳,进行下一组单因素考察。

表2 溶液用量考察结果(n=3)
3.3.2 盐用量考察
取5份生品,每份50g,置蒸锅内,分别加入用不同盐量配制的溶液50mL,闷润,待盐水吸尽后,蒸30min后出锅,烘干,粉碎,过60目筛,备用。
取各炮制品粉末,按上述实验方法中指标性成分含量测定项下的供试品溶液的制备方法和条件进行含量测定,结果见表3

表3 盐用量(%)考察结果(n=3)
由表3可知,盐用量是影响巴戟天指标性成分的因素,加盐量2%的巴戟天炮制品为最佳,故选盐量为2%进行下一组单因素考察。
3.3.3 闷润时间考察
取5份生品,每份50g,置蒸锅内,加入2%盐溶液50mL,闷润不同时间,待盐水吸尽后,蒸30min后出锅,烘干,粉碎,过60目筛,备用。
取各炮制品粉末,按上述实验方法中指标性成分含量测定项下的供试品溶液的制备方法和条件进行含量测定,结果见表4。
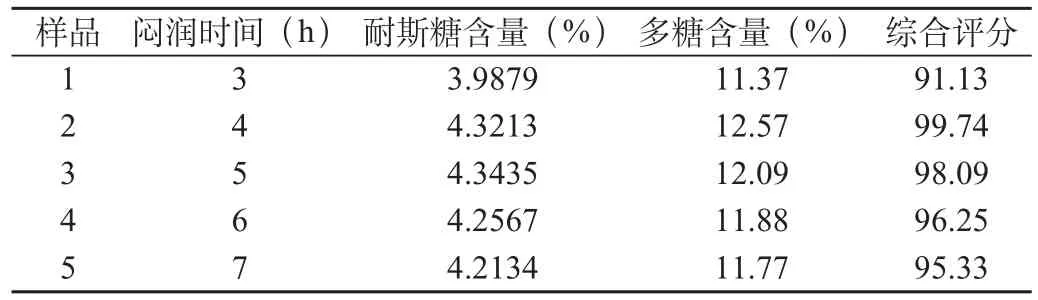
表4 闷润时间考察结果(n=3)
由表4可知,闷润时间是影响巴戟天指标性成分的因素,闷润4h为最佳,故选闷润4h进行下一组单因素考察。
3.3.4 蒸制时间考察
取5份生品,每份50g,置蒸锅内,加入2%盐溶液50mL,闷润4h,待盐水被吸尽后,蒸制不同时间后出锅,烘干,粉碎,过60目筛,备用。
取各样品粉末,由上述实验方法的制备方法和条件进行含量测定,结果见表5。
由表5可知,蒸制时间是影响巴戟天指标性成分的因素,结果为蒸制时间60min的巴戟天综合评分最高。
4 正交实验
由单因素实验结果可知,盐水用量、加盐量、闷润时间和蒸制时间均对巴戟天有效成分均有影响,故以加盐量、闷润时间和蒸制时间为考察因素,以耐斯糖和巴戟天中多糖的含量为指标,进行正交实验,因素水平表见表6,正交试验设计表见表7,方差分析表见表8。

表5 蒸制时间考察结果(n=3)

表6 因素水平表
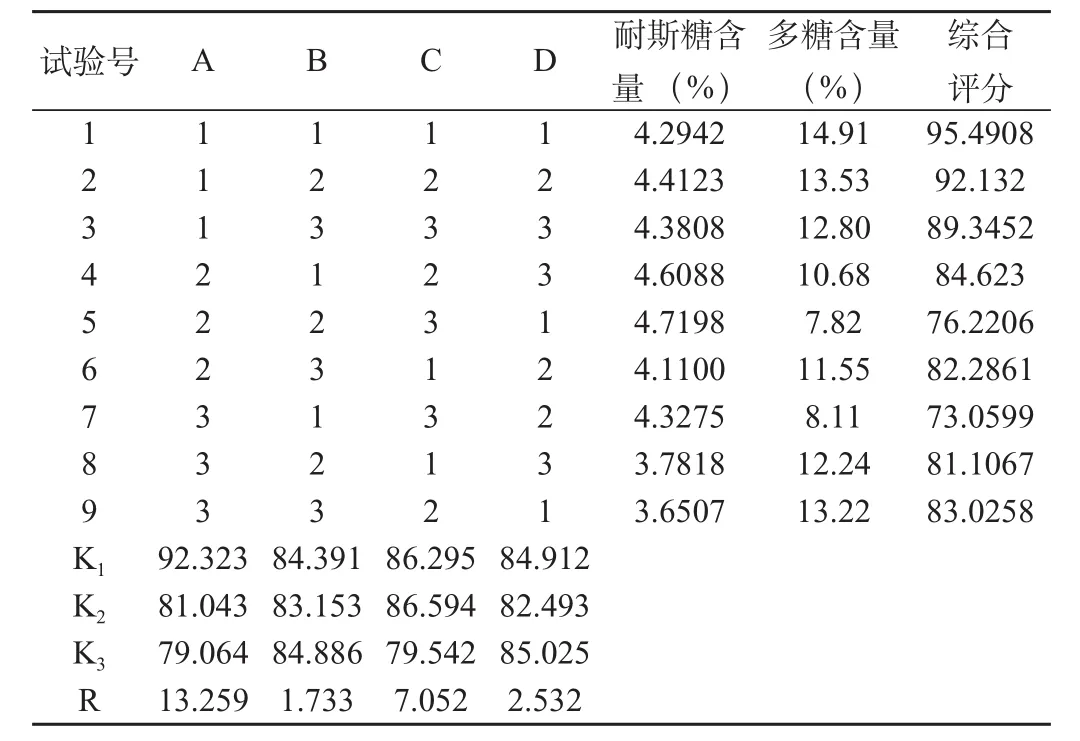
表7 正交实验设计表

表8 方差分析表
由正交实验方差分析结果可知,盐巴戟天的影响因素主次顺序为:A >C>B ,即加盐量>蒸制时间>闷润时间;且 A、C因素为显著因素,即加盐量和蒸制时间对耐斯糖和多糖的含量变化有显著影响。而因素B 对耐斯糖和多糖的含量变化无显著影响。所以,确定盐巴戟天炮制工艺为A1B3C2,即50g药材加入50mL 2%的盐水拌匀闷润5h,加热蒸制60min,趁热除去木心,切段,干燥。
5 验证实验
按优选的最佳炮制工艺制备3份样品,按上述实验制备方法和条件进行含量测定,结果见表9。由表9可见,样品1、2和3的耐斯糖和多糖含量均较高,与正交试验结果相符,说明盐巴戟天炮制工艺稳定可行。

表9 验证实验结果
6 讨论与结论
6.1 2005年版中国药典收载的巴戟天炮制品为巴戟天、巴戟肉、盐巴戟天和甘草制巴戟天4种[8],且以巴戟肉、盐巴戟天和甘草制巴戟天为主流饮片规格[11]。巴戟天的炮制特点是借助所用辅料固有的作用,以增强其壮阳、补益功能,并获得满意疗效,用盐取其下行入肾,增强补肾助阳、强筋健骨的作用[12]。盐制巴戟功专入肾,温而不燥,增强了补肾壮阳、强筋健骨作用[11]。
6.2 巴戟天低聚糖类物质具有显著的抗抑郁活性和补肾助阳的作用,但由于糖类检测的局限性,对这类成分炮制后变化的分析一直未见报道。本文采用新型的通用型检测器-电雾式检测器(CAD),用HPLC法分析巴戟天中低聚糖耐斯糖,结果表明巴戟天中耐斯糖炮制后含量增加,这和文献资料记载盐制品增强补肾阳功能较为吻合。
6.3 巴戟天中多糖为活性成分,所含的多糖有增强免疫和补肾助阳的作用,炮制过程有利于多糖的溶出,起到增效作用,但蒸制时间过长多糖会散失,故蒸制时间应严格控制。本实验用一定浓度的食盐水闷润巴戟天至一定时间后蒸制,工艺简便、易于操作、工艺参数可控,并能保证炮制品的质量。蒸制时间对多糖有较显著的影响,生品经蒸制多糖含量升高,至30min达到最高,但随时间延长,多糖含量则呈下降趋势,60min后下降明显,说明巴戟天的蒸制时间应控制在60min内,以保证有效成分的含量。
[1]陈忠,刘琳玲,何猛雄等.南药巴戟天多糖提取方法的比较研究[J].科技通报,2004,20(6):546-548.
[2]王卫平.巴戟天化学成分和药理作用研究概况[J].时珍国医国药,2000,11(7):665-666.
[3]陈忠,方代南.南药巴戟天化学成分和药理作用的研究进展[J].中草药,2001,32(S):217-218.
[4]陈忠,方代南.南药巴戟天汤液对大鼠免疫功能影响的研究[J].科技通报.2003,19(3):244-246.
[5]陈小娟,李爱华,陈再智.巴戟多糖免疫药理[J].实用医学杂志,1995,11(5):348-349.
[6]林励,徐鸿华,邓沛峰.巴戟天多糖对果蝇性活力及羽化率的影响[A].广州中医药大学中药资源研究室.中药资源开发利用研究论文集[C].广州:广东科技出版社,1996:65.
[7]肖凤霞,林励.巴戟天补肾壮阳作用的初步研究[J].食品与药品,2006,8(5):45-46.
[8]国家药典委员会.中华人民共和国药典[S].一部.北京:化学工业出版社,2005:260-261.
[9]李咏华,黄裕,杨中铎等.高效液相色谱法测定巴戟天中低聚糖含量[J].药物分析杂质,2007,27(11):1797-1799.
[10]郭素华,王和鸣,黄涛等.南靖巴戟天多糖的含量测定[J].福建中医学院学,2006 ,16(1):32-33.
[11]王作明,孙立立,王琦.有关巴戟天炮制的古文献分析[ J ].时珍国医国药,2001,12 (10) : 1131-1132.
[12]王晓奇,刘立维.巴戟天炮制的历史沿革[J].中成药,1994,16 (4): 26.
