钙铝层状双氢氧化物的改性及表征
2010-09-15施惠生章钱光人阮秀秀
施惠生章 萍,钱光人阮秀秀
(1同济大学先进土木工程材料教育部重点实验室,上海 200092)
(2上海大学环化学院,上海 200444)
钙铝层状双氢氧化物的改性及表征
施惠生1章 萍1,2钱光人*,2阮秀秀2
(1同济大学先进土木工程材料教育部重点实验室,上海 200092)
(2上海大学环化学院,上海 200444)
采用离子交换法,将铝酸三钙(C3A)投加至十二烷基硫酸钠(sodium dodecyl sulfate,SDS)溶液中,通过调节pH值和反应温度,制备出插入SDS阴离子的钙铝层状双氢氧化物(CaAl-SDS-layered double hydroxide,CaAl-SDS-LDH)。通过X射线衍射、红外光谱、透投射电镜及热重-差热分析等手段对样品分析表征。结果表明,在SDS浓度为0.2 mol·L-1,pH值11,合成温度25℃为最佳合成工艺条件,所得CaAl-SDS-LDH层间距为2.79 nm,SDS阴离子在层间以双分子层的形式垂直于层板形成交错有序的排布;CaAl-SDS-LDH中有机物质量分数为40%。经SDS改性后的CaAl-SDS-LDH具有层状结构,晶粒尺寸较小,粒径分布集中,晶粒有序度较高。
钙铝层状双氢氧化物;SDS;改性;C3A
以水滑石为代表的阴离子型层状双羟基氢氧化物水滑石类矿物 (Layered Double Hydroxides,简称LDHs),是由相互平行且带有正电荷的层板组成,层间由平衡层板正电荷的阴离子及水分子组成,其基本结构式为:[M1-x2+Mx3+(OH)2x+(An-)x/n·mH2O其中 M2+二价金属离子,包括 Ca2+、Mg2+、Zn2+、Co2+、Cu2+、Mn2+、Ni2+等,M3+代表三价金属离子,包括 A13+、Fe3+、Cr3+等,An-代表阴离子,包括 Cl-、NO3-、PO43-、OH-、CO32-等[1]。因其具有层间阴离子可交换性、结构坍塌记忆效应、主层板可自组装性等特点,已广泛用于高分子复合材料、催化材料、环境治理等领域[2-4]。但由于LDHs层间表面羟基的亲水特性,可用十二烷基硫酸钠(SDS)等阴离子表面活性剂对其进行改性,可将LDHs层间表面亲水性转化为憎水性,使其可制备出对非离子性有机污染物具有高效吸附性能的有机LDHs材料[5-6],如SDS改性后的MgAl-LDH可有效地去除水体中三氯乙烯、四氯乙烯等[7]。
水泥矿物之一铝酸三钙(C3A)在水化过程中,可形成具有层状结构的 4CaO·Al2O3·19H2O(C4AH19),4CaO·Al2O3·13H2O(C4AH13)或者 2CaO·Al2O3·8H2O(C2AH8)化合物,它们是由带正电荷的钙铝[Ca2Al(OH)6]+主层板,存在于夹层空间里的OH-阴离子和水分子组成的CaAl-OH-LDHs[8]。CaAl-OH-LDHs主层板 Ca、Al是以 2∶1 组合,Ca2+的离子半径(0.10 nm)高于Mg2+(0.072 nm),使其表面效应较Mg-Al-LDH高,更有利于提高改性剂交换速率,增大其交换容量。而层间的OH-较CO32-、Cl-更容易被其他阴离子交换[9]。同时CaAl-OH-LDHs合成简便,通过控制C3A水化条件可形成。目前已有文献报道在一定条件下高聚物PC与C3A发生水化反应而形成具有层状结构的有机CaAl-PCn-LDH[10]。
本工作利用C3A化合物直接与SDS溶液水化,通过对起始SDS溶液pH值以及水化过程中温度的研究,确定制备出高有机含量的CaAl-SDS-LDH材料的最佳合成条件。同时通过XRD、FTIR、TGDTA及TEM等表征测试手段,研究了有机CaAl-SDS-LDHs材料的结构、形貌,为其后续作用于吸附环境中非离子型有机污染物的治理上提供了参考。
1 实验部分
1.1 C3A制备
将氧化钙(分析纯 A.R.)和氢氧化铝 (分析纯A.R.)按物质的量之比 3∶2 均匀混合后压片,于 1350℃保温4~5 h。成品研磨混匀再压片继续在1350℃保温4~5 h,该过程重复数次,直至产物颜色变淡绿色,经甘油-乙醇法测产物游离氧化钙含量低于0.5%,即制得 C3A[11]。
1.2 CaAl-SDS-LDH制备
配制 0.2 mol·L-1的 SDS溶液,调节溶液 pH值。称取一定量的C3A化合物分别投加至起始pH值为 8,9,10,11,12的SDS 溶液中,在氮气氛围下密封,分别在25和65℃水浴中振荡12 h后,65℃下陈化24 h,用除CO2去离子水洗涤、抽滤,重复数次清除其表面残留SDS,样品65℃烘干研磨过筛后备用,待XRD,FTIR,TG-DTA及TEM表征。
1.3 CaAl-SDS-LDH表征
采用D/max-rB X射线衍射仪,铜靶,使用铜Kα辐射,经过滤波后经Kα2剥离处理,波长为0.15406 nm,靶电压 40 kV,靶电流 100 mA,X-射线强度由闪烁计数器测量,计数方式为counts·s-1,测角转速器的转速为1°·min-1,所得图利用PCPDWIN软件所有的卡片数据库对XRD图主要衍射峰查找分析。采用AVATAR 370傅里叶红外光谱仪,测试范围为 4000~400 cm-1,KBr压片,32 次扫描,分辨率为4 cm-1。采用STA 449C-QMS 403C热重-质谱联用仪,升温范围 40~1000℃,升温速率 10℃·min-1,N2气氛。采用透射电镜(TEM,H-800,Hitachi Company)在200 kV的条件下对SDS改性前C3A及改性后的CaAl-SDS的形貌进行表征。
2 结果与讨论
2.1 CaAl-SDS-LDH的制备
2.1.1 SDS 溶液初始 pH 值的影响
图1为C3A在SDS溶液不同起始pH值条件下经水化后形成的产物的XRD图。从图1可以明显看出,C3A在SDS溶液中发生水化后,所有产物均在较小的2θ处出现较强的衍射峰,且起始pH值越大,相应的产物出现衍射峰的位置越往小角度偏移。C3A在pH值为11下,其水化的产物在2θ为3.15°、6.86°、13.45°和 33.14°分别出现的层状结构所特有的(002)、(004)、(006)和(110)等晶面特征衍射峰[12],而且从表1样品d值和2θ 2个参数的数据可以看出,(002)晶面衍射峰及其2个高级衍射峰(004)和(006)的d值之间存在良好的倍数关系,表明产物具有良好的层状结构。且(110)晶面衍射峰强且尖锐,说明形成的产物晶体有序度较高,且该产物经SDS改性后的XRD结果,与层状结构的CaAl-LDH与SDS发生离子交换后形成产物一致[13],说明该产物同样具有主体层板[Ca2Al(OH)6]+的结构和组成,进一步说明立方晶体C3A在pH值为11的SDS溶液中水化可形成具有层状结构的CaAl-SDS-LDH。此外,从该产物的XRD图中还可以看出,产物中除了CaAl-SDS-LDH 产物的特征衍射峰外,2θ在 31.01°,33.11°,47.61°,59.17°出现了 C3A 的特征衍射峰 (见图1标 “○”者),说明产物中还含有少量没有发生水化反应的C3A化合物,这主要可能由于C3A化合物在水化过程中其表面快速形成具有层状结构的C4AH19和C2AH8晶体与SDS发生反应而阻碍其内部C3A发生水化反应。从试验中也可观察到反应后的产物坚硬程度高,因此,为使C3A化合物在水化过程中充分水化进而与SDS发生反应,在对其进行改性时,必须使其颗粒均匀分散于SDS溶液中。
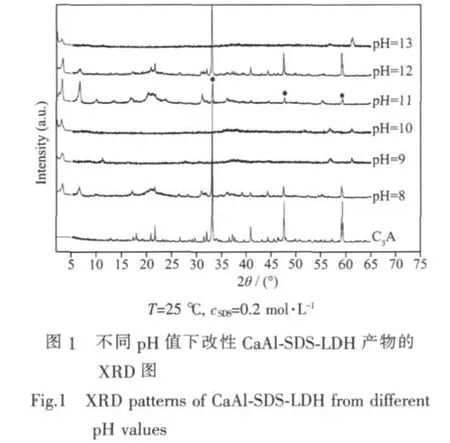
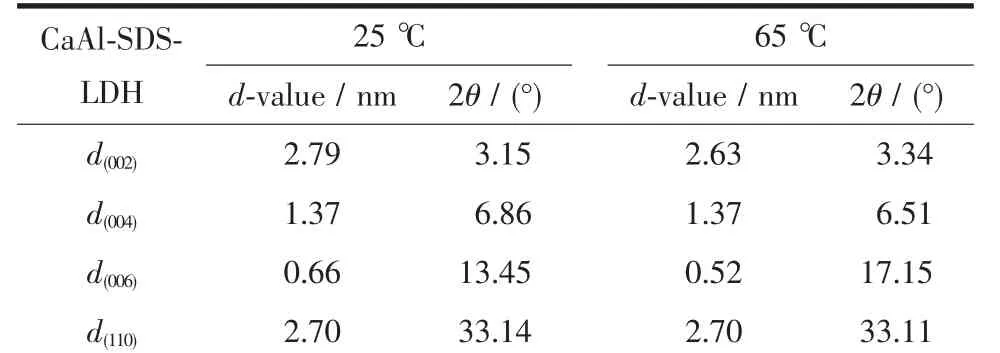
表1 不同温度下合成产物CaAl-SDS-LDH的d值和 2θ值Table 1 d-value and 2θ for CaAl-SDS-LDH with different temperatures
2.1.2 反应温度的影响
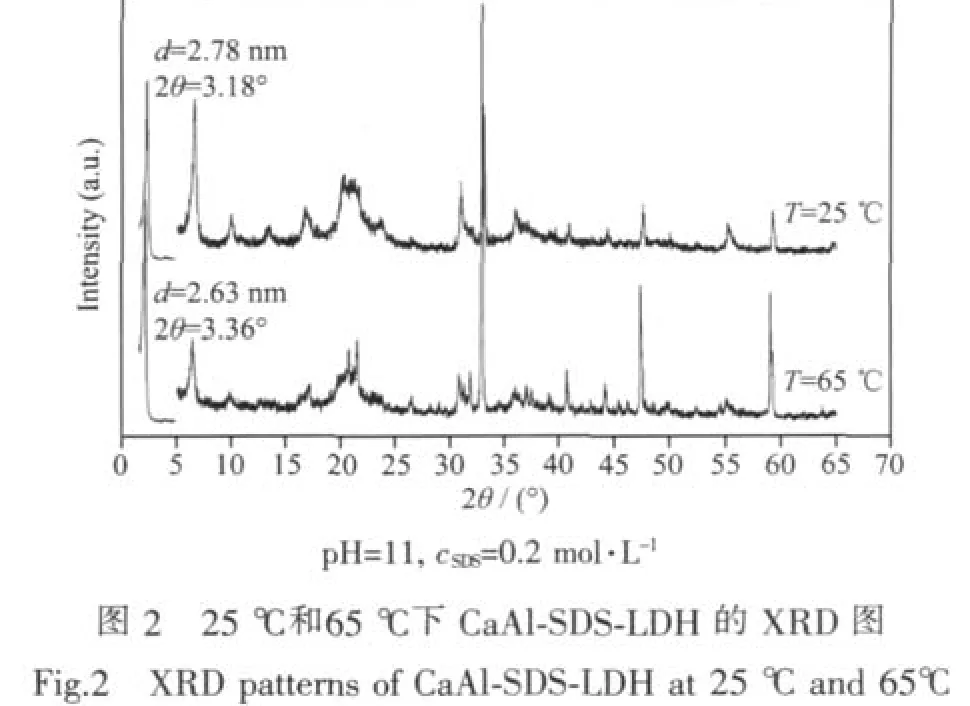
图2为C3A分别在25和65℃下,与pH为11浓度为0.2 mol·L-1的SDS溶液发生水化反应后形成的产物的XRD图。从图2中可以看出,C3A在65℃下也出现了代表层状结构的 (002)、(004)、(006)和(110)等晶面特征衍射峰,但从表1中可以看出该产物的层状结构没有C3A在25℃下形成的CaAl-SDS-LDH结构理想,且比较两者代表产物层间距的衍射峰对称性及尖锐程度,25℃下制备的CaAl-SDS-LDH(002)晶面衍射峰偏移至 2θ角为 3.15°,层间距为 2.78 nm;而在65℃下形成的 CaAl-SDSLDH,其层间距为2.63 nm,明显低于前者产物的层间距。即温度升高,SDS对C3A化合物的插层效果减低。这是因为C3A在水化过程中,升高温度将会加速具有层状结构的水化产物C4AH19和C2AH8向稳定态C3AH6产物转化[14]。而C3AH6是立方晶体,不能与SDS发生插层反应。因此升高水化温度将不利于SDS溶液对C3A化合物的有机改性。
因此,在合成制备CaAl-SDS-LDH时,为保证C3A化合物在水化过程中,充分形成具有层状结构的水化产物,进而与SDS阴离子发生插层反应,其最佳制备条件为SDS溶液pH值11,水化温度25℃。
2.2 CaAl-SDS-LDH的结构表征
2.2.1 FTIR分析
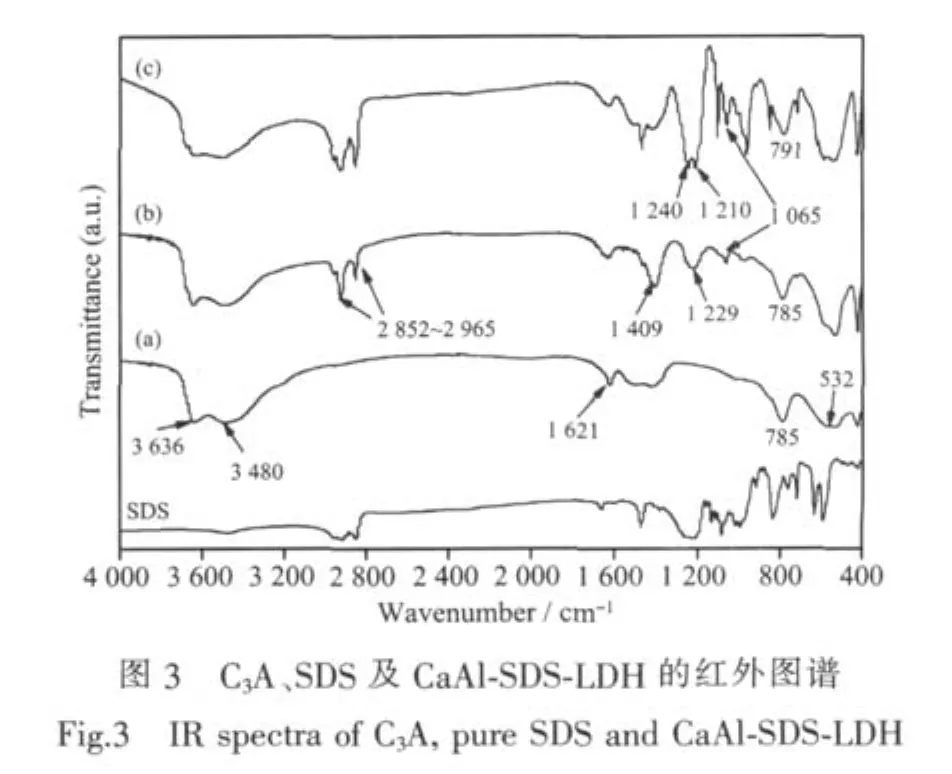
图3为C3A化合物经SDS改性前后的红外光谱。与C3A化合物红外光谱图比较,CaAl-SDS-LDH的红外图谱上分别出现了:2 920 cm-1的C-H反对称伸缩振动吸收峰,2 851 cm-1的C-H对称伸缩振动吸收峰,1470 cm-1处的C-H弯曲振动吸收峰。且从CaAl-SDS-LDH图谱上发现,在1 245 cm-1处出现了S=O较强的特征吸收峰,表明了SDS的存在。同时CaAl-SDS-LDH的红外图谱上出现Al-OH特征吸收峰(783和520 cm-1),说明改性后的产物出现[Ca2Al(OH)6]+结构。另外,对照SDS的红外谱图,有机阴离子插层后,反映-SO3-基团的特征吸收峰均向低波数发生不同程度的位移,这说明层间阴离子与层板之间存在着相互作用,这种作用可能来自于氢键作用[15]。
根据XRD结果,CaAl-SDS-LDH的晶面间距d(002)值为2.78 nm,而根据SDS的构型计算出其链长为 1.78 nm[15],以及 LDHs主层板厚度 0.48 nm,因此通过晶面间距扣除主层板厚度后,层内通道高度可达到2.3 nm,该高度介于单个和2个有机阴离子链长之间,因而计算结果可以推测出SDS阴离子在层间并非以单分子简单垂直有序地排列于上下层板之间,而是以双分子层的形式垂直于层板形成交错有序的排布结构模式[16]。此时,层间SDS阴离子可以通过基团-SO3-与带正电荷层板[Ca2Al(OH)6]+上的羟基形成氢键。此插层过程示意如图4。这个高度看出SDS主要是以插层的形式进入了C3A水化后形成的层状化合物的层间,形成CaAl-SDS-LDH。

2.2.2 TG-DTA 分析
图5(a)和(b)分别为 C3A化合物和 CaAl-SDSLDH的TG-DTA曲线。比较图5(a)和5(b)TG曲线可以看出,CaAl-SDS-LDH在100~300℃间质量的损失以水为主,300℃以上发生有机物的分解燃烧,其在300~1 000℃之间的质量损失约为20%,该损失即为CaAl-SDS-LDH中SDS的含量。从其DTA曲线可见:在135、220℃附近出现的吸热峰为CaAl-SDSLDH层间水、结构水的脱出,在约为430℃左右的放热峰应归因于有机物燃烧放热,在970℃左右存在SDS中-SO3-基团的分解[16]。与未改性前的C3A化合物相比,CaAl-SDS-LDH化合物中明显含有吸附水及层间水,且脱吸附水温度低于C3A化合物。C3A是氧化钙和氢氧化铝在高温条件下经过固相反应形成的化合物,当SDS阴离子进入C3A水化形成的C4AH19或C2AH8的层板中,增强了其表面疏水性,进而使其层板对水分子的吸附固定能力减弱[12]。

2.2.3 TEM 分析
图6是C3A化合物和CaAl-SDS-LDH的TEM照片。从图中可以看出,改性后的CaAl-SDS-LDH样品呈现出片状颗粒,粒子分布集中,尺寸较小,较好地体现出改性后CaAl-SDS-LDH化合物层片状结构特征。同时SDS作为表面活性剂,有效地抑止了晶粒的团聚,尺寸较小。

3 结 论
综合上述结果可得出以下结论:
(1)制备具有层状结构的CaAl-SDS-LDH时,SDS溶液起始pH为11,合成温度为25℃时为最佳工艺条件。
(2)SDS插层C3A水化产物后,形成的CaAl-SDS-LDH化合物,其层间距为2.78 nm。经SDS改性后,晶粒尺寸较小,粒径均一,晶粒有序度较高。
(3)通过TG-DTA结果分析,经SDS改性后的CaAl-SDS-LDH化合物,有机物含量在约为20%,表面憎水性有所增强,有利于后续对非离子型有机物的吸附应用。
[1]Palmer S J,Frost R L,Nguyen T.Coordin.Chem.Rev.,2009,253(1/2):250-267
[2]Hsueh H B,Chen C Y.Polymer,2003,44(4):1151-1161
[3]MA Yin(马 莺),CHEN Yu-Ping(陈玉萍),XU Lin(徐 林),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(4):551-559
[4]Legrouri A,Lakraimi M,Barroug A,et al.Water Res.,2005,39(15):3441-3448
[5]Zhang X,Xu Y.Chem.Mater.,2007,19(6):1452-1458
[6]Shi Z,Sigman M,Ghosh M M,et al.Environ.Sci.Technol.,1997,31(12):3581-3587
[7]Zhao H,Nagy K.J.Colloid Interface Sci.,2004,274(2):613-624
[8]Meredith P,Donald A M,Meller N,et al.J.Mater.Sci.,2004,39(3):997-1005
[9]Park J,Park J Y,Byun H J,et al.Chemosphere.,2008,70(8):1429-1437
[10]Plank J,Dai Z,Zouaoui N.J.Phys.Chem.Solids,2008,69(5/6):1048-1051
[11]Stephan D,Wistuba S.Cement Concrete Res.,2006,36(11):2011-2020
[12]Zhang H,Wen X,Wang Y.J.Solid State Chem.,2007,180(5):1636-1647
[13]SHIHui-Sheng(施惠生),ZHANG Ping(章 萍),QIAN Guang-Ren(钱光人),et al.Chinese J.Ceram Soc.(Guisuanyan Xuebao),2010,38(4):659-693
[14]Birnin-Yauri U,Glasser F.Cement Concrete Res.,1998,28(12):713-1723
[15]Pavan P,Crepaldi E,Valim J.J.Colloid Interface Sci.,2000,229(2):346-352
[16]Qian T,Yuan J,Frost R L,et al.Appl.Clay Sci.,2009,45(4):262-269
Hybrid CaAl-SDS-LDH:Preparation,Structure and Intercalation by Sodium Dodecyl Sulfate into Tricalcium Aluminate(C3A)
SHI Hui-Sheng1ZHANG Ping1,2QIAN Guang-Ren*,2RUAN Xiu-Xiu2
(1Key Laboratory of Advanced Civil Engineering Materials(Tongji University),Ministry of Education,Shanghai 200092)
(2College of Environmental and Chemical Engineering,Shanghai University,Shanghai 200072)
Modified CaAl-layered double hydroxide (CaAl-SDS-LDH)was prepared by introducing sodium dodecyl sulfate (SDS)into tricalcium aluminate (C3A)through an ion-exchange method under various pH values and reaction temperatures.The product was characterized by using X-ray diffraction (XRD),Fourier transform infrared(FTIR),transmission electron microscopy(TEM)and thermogravimetric-differential thermal analysis(TGDTA).The optimized process conditions are the initial SDS concentration of 0.2 mol·L-1,pH value of 11 and reaction temperature of 25℃.The organic content on organo-CaAl-LDH is about 40% (mass fraction).And the layer structure is not destroyed with the interlayer spacing value of 2.79 nm,and the intercalated surfactants are more likely to adopt a bilayer arrangement model,and the crystalline structure is more integrity.
CaAl-LDH;SDS;modification;C3A
O614.23+1;O614.3+1;TQ172
A
1001-4861(2010)09-1544-05
2010-05-10。收修改稿日期:2010-07-01。
国家自然科学基金(No.20907029)和(No.20677037)资助项目。
*通讯联系人。E-mail:grqian@shu.edu.cn
施惠生,男,57岁,博士,教授,博士生导师;研究方向:生态环境材料。
