聚乳酸/羟基磷灰石微球的合成与性能
2010-09-06陆荣张峰丁翠翠李苏亚
陆荣,张峰,丁翠翠,李苏亚
(盐城工学院材料工程学院,江苏 盐城 224051)
聚乳酸/羟基磷灰石微球的合成与性能
陆荣,张峰,丁翠翠,李苏亚1
(盐城工学院材料工程学院,江苏 盐城 224051)
以生物可降解高分子材料聚乳酸(PLA)为载体,羟基磷灰石(HA)为核心材料,采用溶剂蒸发法制备了聚乳酸/羟基磷灰石(PLA/HA)微球。在可确定因素固定下来后,在保证成球质量的基础上,分别通过调节乳化剂浓度和其它因素在一定范围内控制微球的平均粒径。通过正交实验摸索出制得粒径大小为200µm左右PLA/HA微球的最佳工艺方案:搅拌速度为500r·min-1,PLA浓度为0.08g·mL-1,PVA浓度为0.006g·mL-1,HA添加量为0.10g。扫描电镜(SEM)表明微球外观基本光滑圆整,但表面有少许小孔和凹槽;观察了PLA/HA微球在生理盐水中的降解行为,发现其降解速率低于纯聚乳酸;通过对微球释药率的研究发现其具有良好的缓释性能。
PLA/HA微球;合成;性能;正交设计
聚乳酸(PLA)是一种无毒、无刺激性,具有良好生物相容性的新型高分子聚合物,是以乳酸为单体经缩聚反应合成的生物可降解高分子材料。它在生物体内经过酶分解,最终形成二氧化碳和水,因其在骨组织工程的一些实验研究中表现出良好的骨修复作用,所以在医用领域被认为是最有前途的可降解高分子材料。PLA在骨组织工程的一些实验研究中表现出良好的骨修复作用,但同时也反映出一些不足,如强度不足,降解后的材料不利于骨细胞生长等[1]。羟基磷灰石(HA)是自然骨的主要成分,约占人体骨重量的60%左右,一直被公认是材料在硬或软体组织连接中起关键作用的物质,其晶体的结构式为Ca10(PO4)6(OH)2[2]。合成HA在组成成分和结构上与自然骨组织的钙盐一致,在生物学特性方面,它具有极好的生物活性,骨传导性,能为新骨的形成提供生理支架作用,与骨组织形成直接的骨性结合;但它在张力方面表现出脆性,没有足够的强度和疲劳承受力,易断裂,加工性能差,不适合单独作为骨折内固定材料使用,限制了羟基磷灰石的应用发展[3]。研究表明,PLA/HA复合材料能很好地把两组分各自所具有的生物可降解性和骨传导性能有机地结合起来,组分中的羟基磷灰石还可为骨缺损部分提供优质钙、磷来源。HA呈碱性,可抑制聚乳酸的酸催化降解,并有可能减轻或消除聚乳酸降解产生过量的酸性产物可能引起的非感染性炎症。另外,对于有机/无机复合材料来说,可降解的无机组分还可影响到有机组分的降解速率,其溶解重沉积过程能够阻碍或抑制材料内部输水孔洞的形成,从而使材料的整体降解速率下降,减缓了材料的机械强度随降解过程的衰减[4~5]。本课题组曾以聚乳酸为原料,选择聚乙烯醇为乳化剂,采用O/W乳化-溶剂挥发法制得形态较好的聚乳酸空白微球[6]。微球又称微球囊或者微囊,是利用天然的或者合成的高分子材料将固体或液体药物包裹成直径1~500µm的微小胶球,微球外面一般呈球状实体或呈平滑的球状膜壳形、葡萄串形及表面平滑或折叠的不规则的结构等各种形状,其外形取决于微球材料的性质和材料凝聚的方式[7]。近年来,聚乳酸载药微球也成为医药材料的研究热点[8~13]。因PLA/HA复合材料以其良好的骨传导性、骨诱导性、生物降解性能、较高的机械性能成为研究的热点,所以本课题组受到启发,在合成空白微球的基础上,以PLA为载体,合成出PLA/HA载药微球,研究了微球的最佳合成工艺并且做了体外性能研究,为进一步用于生物医用高分子材料的研究提供理论支持。
1 实验部分
1.1 主要试剂和仪器
聚乳酸(PLA,分子量 8万,A级),聚乙烯醇(PVA,分析纯),三氯甲烷(CHCl3,分析纯),羟基磷灰石(HA,分析纯)。多功能搅拌器D-8401,激光粒度分析仪BT-9300S,扫描电子显微镜S-570,高效液相色谱仪P680。
1.2 实验方法
将 PVA水溶液加入三口烧瓶中在一定速度下搅拌,保持搅拌速度不变,取一定量的PLA/HA三氯甲烷溶液,以固定滴加速度滴加到三口烧瓶中,此时溶液释出形成两相,搅拌桨的剪切作用使有机相分散成小球形成乳状液。在固定的搅拌速度下,连续搅拌数小时后水浴加热挥发三氯甲烷,待其挥发完毕,将产品洗涤、过滤、真空干燥后再检测。成品微球用激光粒度分析仪测平均粒径,通过SEM观察分析微球表面形貌,通过对其在模拟人体液环境的磷酸盐缓冲液中的pH 值变化研究其体外降解情况,并对微球的释药性能进行研究。
2 结果与讨论
2.1 正交实验优化工艺
从课题组前期研究聚乳酸空白微球合成的过程可知,对于载药微球成球性影响较大的单因素为:PLA浓度、PVA浓度、搅拌速度及HA添加量。为了优化工艺,选择以上4个因素作为考察对象,每个因素选择3个水平列于表1,即进行正交实验。正交实验方案及其极差分析见表2。从表2可知,影响微球粒径的主次顺序依次为:搅拌速度、PLA浓度、PVA浓度、HA添加量。制备粒径约为200µm的聚乳酸微球,最佳的工艺条件组合为:搅拌速度为500r·min-1,PLA 浓 度 为 0.08g·mL-1,PVA 浓 度 为0.006g·mL-1,HA添加量为0.10g。

表1 正交设计因素水平表Tab.1 Factor-level in orthogonal-designed experiments

表2 试验方案及试验结果Tab.2 Projects and analyses of orthogonal-designed experiments
2.2 粒径分布
图1是不同搅拌速度(400、500、600、700、800r·min-1)下所对应的微球粒径区间质量分数,由图可知,搅拌速度越快,所得到的微球粒径越小,其分布也越均匀。由此要得到所需大小的微球时可以根据此粒径分布规律选择相应的搅拌速度,以便能更迅速、便捷地完成实验。在500r·min-1的转速下得到平均粒径为200µm的微球,与正交实验结果相符,大部分微球粒径处于190~230µm区间内,微球粒径分布均匀,从而有利于制造结构均一的组织材料。

图1 粒径分布Fig.1 The distribution of particle size
2.3 SEM表征
以扫描电子显微镜观察微球的整体形态和单个微球的表面状况,结果见图2、3。

图2 PLA 微球的SEM图(A)Fig.2 SEM of PLA microsphers (A)
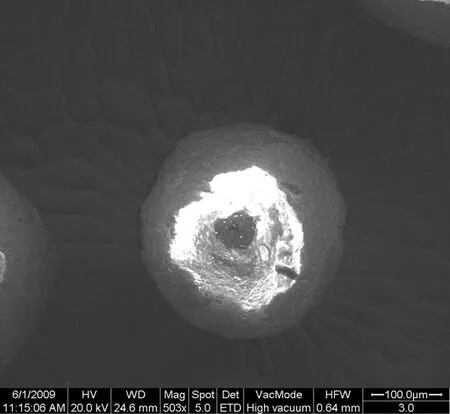
图3 PLA 微球的SEM图(B)Fig.3 SEM of PLA microsphers (B)
从SEM照片(图2)中可以看出,制备的PLA微球呈均匀圆球状,表面光滑,无粘连现象;但粒径不太均一,原因可能是机械搅拌器很难长时间完全保持高速稳定造成的。从图3可以看出,放大到一定倍数的PLA微球表面并不是完全光滑,也存在凹凸不平,原因可能是在微球制备过程中微球的表面已硬化而微球的内部没有完全硬化,内部硬化时外部塌陷所形成的皮芯结构。一些不透光的阴影应是添加的HA的结晶。部分微球表面有小孔或凹槽,这可能是合成过程中CHCl3的挥发所致,这也将成为HA向微球外溶液扩散的通道。
2.4 降解行为研究
聚乳酸类聚合物的水解主要包括吸水、酯键的断裂、可溶性齐聚物的扩散和碎片的溶解等4个过程。具体的说,当把聚乳酸材料进行体外植入或体内降解时,首先是材料吸水,从扩散的角度看,很快就会在材料的外部和内部出现水吸收不一致的情况,但由于水的扩散比酯键的水解要快得多,因此,可以认为酯键的水解在开始阶段是均匀的。随着降解的继续,就会出现材料在内部的降解要比在表面的降解快的现象。这种内部和外部降解不一致的现象被认为是由以下原因造成的,即酯键的断裂形成的可溶性低聚物在表面比在内部更容易扩散到外部媒介中,内部还来不及扩散的酸性小分子积累造成局部酸浓度过大,它们又会加速材料的降解,发生自催化效应。

图4 缓冲液pH值变化Fig.4 pH value change of buffer solution
将一定量的平均粒径为 200µm 的载药微球放在 37℃,pH值为 7.4,0.1mol·L-1的磷酸盐缓冲液中(模拟人体液环境),进行体外降解性能研究,pH值变化曲线见图 4。复合微球中的聚乳酸降解速度低于纯聚乳酸是因为HA有减缓PLA降解的作用。HA对PLA降解的抑制作用是由于HA的碱性中和了PLA降解过程中产生的酸性产物的酸性,减缓了酸对PLA的催化降解作用的结果。
另外研究发现,投入缓冲液中微球初始重量为0.1710g,降解试验进行20d后,重量为0.1660g。表面看来PLA/HA微球材料在整个降解过程中的重量并未发生明显改变。但可能因为PLA材料的内部在降解过程中会出现大量的微孔,根据毛细管效应,处于微孔内的水分很难被彻底抽干,因此材料的实际重量可能要小于测量值。
2.5 释药行为研究
国内对绿色高分子材料-聚乳酸的关注目前暂限应用于医用药物方面,也就是聚乳酸载药微球的研究,研究发现,聚乳酸载药微球能延缓药物的释放,降低药物的毒副作用;它具有靶向性,无免疫原性;另外载药微球可经多种途径给药,节省了人力、物力、财力。本课题组对聚乳酸微球做为靶向药物和缓释控释药物载体的功能也进行了研究。现将一定量的平均粒径为 200µm 的载药微球放在如上实验所用的缓冲液中进行体外药物释放性能研究,药物(HA)释放曲线见图5。
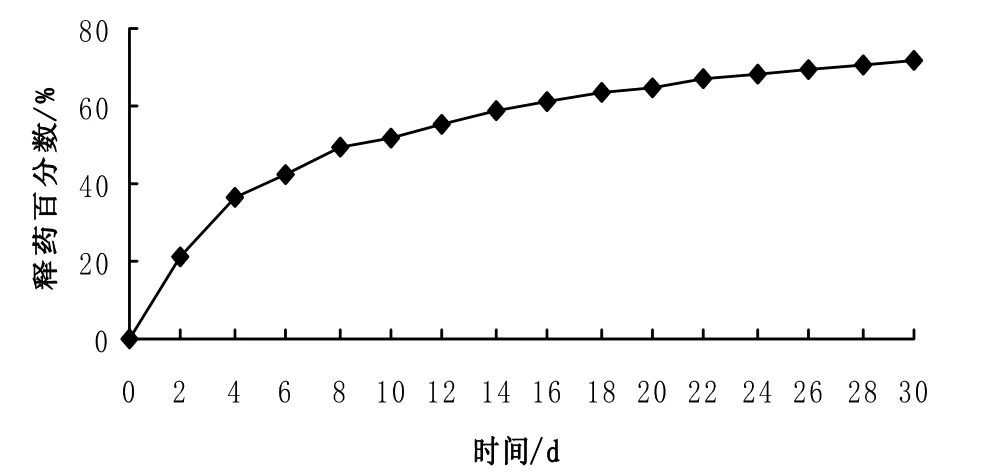
图5 PLA/HA微球的释药曲线Fig.5 Drug-releasing curve of PLA/HA microsphers
由图5可见,在前4d药物释放相对较快,之后释放趋于平稳,在30d时释药百分比为71.3%,整个过程没有显示出强烈的突释效应与释放延迟,反映出聚乳酸微球对药物具有较好的缓释及控释性能,应能满足长效安全的缓释制剂应用于疾病治疗的要求。研究证明,聚乳酸载药微球是一种极有开发前途的新型复合材料,随着微球制剂的陆续研发与上市,在不远的将来,它必将成为人类征服疾病的又一有效手段。
3 结论
以聚乳酸(PLA)作载体,羟基磷灰石(HA)为核心材料,采用溶剂蒸发法制备了聚乳酸/羟基磷灰石(PLA/HA)微球。通过正交实验摸索出制得粒径大小为200µm左右PLA/HA微球的最佳工艺方案:搅拌速度为 500r·min-1,PLA 浓度为 0.08g·mL-1,PVA浓度为 0.006g·mL-1,HA 添加量为 0.10g。微球外观呈球形无粘连,表面有少许缺陷;PLA/HA的降解速度低于纯PLA;载药微球对药物具有良好的缓释性能。
[1] 刘芳,贾德民,王迎军.聚乳酸及其复合材料在骨组织工程方面的研究进展[J].生物医学工程学杂志,2001,18(3):448-450.
[2] 邱雪宇.聚乳酸/羟基磷灰石纳米复合材料的制备与性质[D].长春:中国科学院长春应用化学研究所,2005.
[3] 强小虎.张杰.纳米羟基磷灰石/聚乳酸复合材料的性能测试[J].中国组织工程研究及临床康复,2007,11(5):911-913.
[4] 廖建国,李玉宝,王学江,等.纳米羟基磷灰石/聚碳酸酯复合生物材料[J].复合材料学报,2008,25(3):64-67.
[5] 王华林,李延红,翟林峰,等.可降解聚乳酸/羟基磷灰石杂化材料[J].高分子材料科学与工程,2006,22(3):247-249.
[6] 陆荣,郑雪芹,安晶,等.聚乳酸微球的制备及应用[J].工程塑料应用,2009,37(2):44-47.
[7] QIU X Y , HAN Y D, ZHANG X L. Preparation of nanohydroxyapatite/poly(L-lactide)biocomposite microspheres[J]. Journal of Nanoparticle Research , 2007,(9):01-908.
[8] 马光辉.微球和微囊的制备与应用研究[J].科技潮,2006,(12):36.
[9] 白雁斌,赵爱平,高发奎.聚乳酸及其共聚物载药微球的研究进展[J].高分子通报,2007,(12):34-40.
[10] 兰婷.聚乳酸微球的制备及性能研究[D].西安:西北大学,2007.
[11] HUO D J, DENG S H, LI L B, et al. Studies on the poly(lactic-co-glycolic) acid microspheres of cisplatin for lung-targeting[J]. Int J Pharm, 2005, 289(12): 63-67.
[12] CARBALLIDO A,VANRELL R, MARTINEZ I T, et al.Biodegradable ibuprofen-loaded PLGA microspheres forintraarticular administration. Effect of Labrafil addition on release in vitro[J]. Int J Pharm, 2004, 279(12):33-41.
[13] 冯晓健.复乳法制备聚乳酸微球及其体外释药性能的测定[D].南京:南京师范大学,2008.
Synthesis and Performance of PLA/HA Microspheres
LU Rong, ZHANG Feng, DING Cui-cui, LI Su-ya
(School of Materials Engineering, Yancheng Institute of Technology, Yancheng 224051, China)
Polylactic acid/hydroxyapatite (PLA/HA) composite microspheres were prepared through O/W emulsion/solvent evaporation method by choosing PLA as carrier and HA as core materials. On the basis of ensuring the quality of produced particles,the concentration of emulsifier and other factors were adjusted in a certain range to control the average particle sizes of microspheres after the confirmable factors were fixed. The best crafts to synthesize PLA/HA microspheres with the diameters of about 200µm were found through orthogonal-designed experiment: stirring rate was 500r/min, concentration of PLA was 0.08g/mL, concentration of PVA was 0.006g/mL and adding amounts of HA was 0.10g. SEM showed that the appearance of microspheres was smooth and sphere, but there were some stomas and grooves on the surface; it was found that the degradation speed of PLA/HA microspheres was lower than pure PLA through observation of their degradation behavior in buffer solution; the microspheres having good drug-releasing properties was found by researching drug-releasing rate of PLA/HA microspheres.
PLA/HA microspheres; synthesize; performance; orthogonal-designed method
R 318.08
A
1671-9905(2010)09-0004-04
江苏省生态环境材料重点实验室重点学科建设开放基金(XKY2007015)
陆荣,女,1976年生,硕士,讲师,主要从事高分子材料及生态环保材料的研究,E-mail:lurong@ycit.cn
2010-04-21
