正相HPLC-MS/MS法测定人体血浆中西酞普兰对映异构体浓度
2010-09-01梁茂植秦永平
向 瑾,余 勤,张 成,梁茂植,南 峰,秦永平
(四川大学华西医院GCP中心临床药理研究室,四川成都 610041)
正相HPLC-MS/MS法测定人体血浆中西酞普兰对映异构体浓度
向 瑾,余 勤,张 成,梁茂植,南 峰,秦永平
(四川大学华西医院GCP中心临床药理研究室,四川成都 610041)
建立了正相高效液相色谱-串联质谱 (HPLC-MS/MS)法测定人体血浆中西酞普兰(citalopram,CIT)对映异构体浓度。采用CHIRALCEL OJ-H(250 mm×4.6 mm×5μm)手性柱,利多卡因作为内标,流动相为V(正己烷)∶V(无水乙醇)∶V(二乙胺)=70∶30∶0.1的溶液,流速为0.5 mL·min-1。血浆样品在碱性条件下用V(正己烷)∶V(异丙醇)=98∶2的溶液提取浓集后,选择大气压化学电离源和多反应离子监测(MRM)模式进行测定。CIT和内标检测离子对分别为 m/z325.1→108.9和 m/z235.4→86.1。rac-CIT的线性范围为0.156~50μg·L-1,S-CIT的线性范围为0.078~25μg·L-1,标准曲线的线性良好(r> 0.99)。rac-CIT、S-CIT和 R-CIT的方法回收率分别为99.7%~101.5%,99.1%~103.3%,99.9%~100.2%;萃取回收率分别为73.5%~75.1%,73.9%~76.0%,73.1%~74.3%。各组分的日内RSD和日间RSD均小于5.0%。
西酞普兰;对映异构体;血药浓度;高效液相色谱-串联质谱(HPLC-MS/MS)
西酞普兰(citalopram,CIT)是一种选择性的5-羟色胺再摄取抑制剂。与同类药物相比, CIT对5-羟色胺的再摄取抑制性强、选择性高,对其他摄取机制、神经递质受体和酶类没有或仅有非常微弱的作用,由于其耐受性好、副作用少的特点,已成为目前治疗抑郁症的一线药物。西酞普兰分子存在一个手性中心,临床常以消旋体(rac-CIT)给药,而国内外的药理研究已经表明,右旋西酞普兰(S-CIT)的抗抑郁作用比左旋西酞普兰(R-CIT)至少强100倍[1]。OJ-H手性柱为纤维素类手性柱,由于水能溶解纤维素及其衍生物,故流动相一般采用正相系统。本实验选择大气压化学电离源和多反应离子监测(MRM)模式,建立测定西酞普兰对映异构体血浆浓度的正相HPLC-MS/MS法,可用于西酞普兰对映异构体血浆浓度的测定和药代动力学研究。
1 实验部分
1.1 仪器与色谱条件
SIL-HTc型高效液相色谱仪:日本岛津公司产品;API 3000三重四极杆串联质谱仪:美国 Applied Biosystems公司产品。CHIRALCEL OJ-H手性柱(250 mm×4.6 mm×5μm), phenomenex氰基预柱(4 mm×3 mm×5μm),柱温为室温,流动相为V(正己烷)∶V(无水乙醇)∶V(二乙胺)=70∶30∶0.1的溶液,流速为0.5 mL·min-1。离子源为大气压化学电离源(APCI),离子源温度350℃,碰撞活化气(CAD) 9 kV,雾化气 (NEB)流速4 L·min-1,气帘气(CUR)流速7 L·min-1。正离子MRM模式监测,西酞普兰和内标利多卡因的检测离子对分别为m/z325.1→108.9和 m/z235.4→86.1,离子去簇电压(DP)分别为45 V和33 V,离子对碰撞活化电压(CE)分别为42 V和27 V。
1.2 试剂与试药
氢溴酸西酞普兰化学对照品和草酸艾司西酞普兰(S-CIT)对照品:纯度99.5%,均由成都市科伦药物研究所提供;利多卡因化学对照品:购自山西大同制药厂;甲醇、正己烷和异丙醇:均为色谱纯,TEDIA公司产品;其余试剂均为分析纯。
1.3 标准溶液配制
精密称取6.25 mg(相当于 rac-CIT 5 mg)氢溴酸西酞普兰,置于100 mL容量瓶中,用甲醇定容至刻度,即得50 mg·L-1rac-CIT储备液,临用前以甲醇稀释 rac-CIT标准系列工作液,分别为 250、200、100、50、25、12.5、6.25、3.125、1.562和0.781μg·L-1;精密称取3.2 mg(相当于S-CIT 2.5 mg)草酸艾司西酞普兰,置于100 mL容量瓶中,用甲醇定容至刻度,即得25 mg·L-1S-CIT储备液,临用前以甲醇稀释S-CIT标准系列工作液,分别为125、100、50、25、12.5、6.25、3.125、1.562、0.781和 0.391 μg·L-1;精密称取6.2 mg(相当于利多卡因 5 mg)盐酸利多卡因,置于100 mL容量瓶,用甲醇定容至刻度,即得内标储备液(50 mg·L-1),临用前以甲醇稀释为4μg·L-1的内标工作液。
1.4 样品预处理
取500μL血浆,加入50μL内标工作液和100μL 1 mol·L-1氢氧化钠溶液,混匀后加入3 mLV(正己烷)∶V(异丙醇)=98∶2的萃取剂,漩涡萃取 10 min,低温离心 10 min(16 ℃, 3 000 r·min-1),转移上层有机相于干净尖底试管中,置于40℃水浴中,通空气流挥干,残留物溶于100μL流动相,进样40μL。由药物与内标的峰面积比对药物浓度进行加权(1/c2)线性回归。
rac-CIT的浓度以 R-CIT和 S-CIT的峰面积之和与内标峰面积之比,通过 rac-CIT标准曲线计算;S-CIT的浓度以 S-CIT的峰面积与内标峰面积之比,通过 S-CIT标准曲线计算;RCIT的浓度为rac-CIT与S-CIT的浓度之差。
2 结果与讨论
2.1 检测方法的选择
CIT同时具有紫外和荧光吸收,一般说来,荧光检测灵敏度较紫外高。陈国珍等[2]指出:许多共轭芳香族化合物,激发时发生π→π跃迁,其荧光光谱受溶剂极性的影响较大。由于这些分子受激发时,其电子激发态比基态具有更大的极性,随着溶剂极性的增大,对激发态比基态产生更大的稳定作用,因此π→π跃迁所需的能量差小,且跃迁几率增加,荧光光谱随着溶剂的极性增大而向长波方向移动,强度也会增加。但本实验发现,在浓度相同的情况下,采用紫外检测时药物的响应比荧光检测高20多倍。这是由于OJ-H手性分析柱的特殊要求,流动相采用低极性的正己烷/无水乙醇系统,CIT在正相溶剂系统中进行π→π跃迁,所需的能量差增大,且跃迁几率减小,强度也就大大减小。虽然其紫外响应较荧光响应高,但仍不能满足药动学测定的需要,故最终采用HPLC-MS/MS法测定西酞普兰对映异构体血药浓度。
2.2 离子源的确定
本实验比较了电喷雾离子源(ESI)和大气压化学电离源(APCI),结果显示,在相同流速下,采用ESI源,药物响应只是采用APCI源的20%左右。这可能因为流动相为正相,ESI源不利于CIT的离子化。在不分流的条件下,ESI源的流速不能超过0.3 mL·min-1,此时CIT消旋体达到基线分离所需的保留时间为30 min; APCI源流速可达2 mL·min-1,当流速为0.5 mL·min-1时,CIT消旋体达到基线分离的保留时间大大缩短(tR<15 min),故本研究采用APCI离子源。有文献[3]报道正相 HPLC-MS/MS法易发生爆炸,本研究将离子源温度设定为350℃,提高了正相HPLC-MS/MS法的安全性。
2.3 离子对的选择
本实验采用正相HPLC-MS/MS法,流动相采用低极性的正己烷/无水乙醇系统,故药物的解离程度将直接影响测定灵敏度。国外学者常在柱后添加甲酸,醋酸铵以提高正相 HPLCMS/MS条件下药物的响应[4-5]。本实验在进行针泵扫描时,也考察了添加甲酸、醋酸铵对药物离子化的影响,结果显示,柱后添加甲酸未能提高CIT的响应,添加醋酸铵也未出现预期的m/z342([M+NH4]+),故未采用柱后添加的方法。CIT和内标的二级质谱图示于图1。

图1 西酞普兰(a)和内标(b)的MS2扫描质谱图Fig.1 MS2spectra of citalopram(a)and internal standard(b)
2.4 流动相的优化
在手性分离过程中,一些强碱、强酸类物质容易吸附在手性色谱柱上,从而造成色谱峰形展宽和拖尾,这些吸附一般存在于填料上的活性点。为了避免这种情况,可以在流动相中加入一些添加剂,这些物质比待分析样品更容易吸附在填料上,这样填料上的活性点对待分析样品而言就被屏蔽掉了。由于西酞普兰是弱碱性药物,故需要在流动相中加一定量的碱性添加剂,实验最后选定二乙胺作为碱性添加剂。
随着流动相中醇比例的增加,药物的保留时间减少,当醇的比例为30%时,R-CIT和S-CIT能达到基线分离,R-CIT和 S-CIT的保留时间分别是12.8 min和14.2 min,故最终确定流动相为V(正己烷)∶V(无水乙醇)∶V(二乙胺)= 70∶30∶0.1的溶液,流速为0.5 mL·min-1,柱温为室温。
2.5 血浆样品预处理条件的选择和优化
实验考察了在不同浓度氢氧化钠溶液(0.1、0.5、1 mol·L-1)中,CIT和内标的萃取回收率,通过实验发现,随着碱浓度的增加,萃取回收率逐渐增大,且高浓度碱液条件下,萃取挥干后的残渣复溶溶液较澄清,故确定在1 mol·L-1氢氧化钠的碱性条件下萃取。
国外学者对人体血浆中的 CIT进行研究时,预处理多采用2次萃取[6-7],且萃取剂体积较大。本研究在碱性条件下对萃取剂的筛选发现:正己烷的萃取回收率最低,不到50%;乙酸乙酯和乙醚萃取挥干后的残渣复溶后,溶液较混浊;二氯甲烷萃取时的萃取回收率不稳定;用V(正己烷)∶V(异丙醇)=98∶2的溶液萃取时,样品基线噪声较小,色谱峰的响应高,回收率恒定,故选择含2%异丙醇的正己烷作为本研究的萃取剂。
2.6 方法学验证
2.6.1 特异性考察 分别取空白血浆、空白血浆加标样、受试者给药后收集的血浆样品,按上述血浆样品处理方法及检测条件进行定量分析,其色谱图示于图2。结果表明,血浆中的内源性杂质不会干扰R-CIT、S-CIT及其内标的测定。

图2 空白血浆(a)和空白血浆加S-CIT对照品(b)、空白血浆加 rac-CIT对照品(c)和给药后血浆(d)色谱图Fig.2 Chromatograms of blank plasma(a),blank plasma withS-CIT(b), blank plasma withrac-CIT(c)and sample plasma(d)
2.6.2 标准曲线 以药物与内标的峰面积比为横坐标(x),血浆药物浓度为纵坐标(y)进行线性回归 (1/c2),rac-CIT 在 0.156~ 50 μg·L-1范围内,回归方程为:y=0.214 3x+ 0.001 8(r=0.999 2);S-CIT在 0.078~25 μg·L-1范围内,回归方程为:y=0.305 7x-0.003 2(r=0.999 2)。
2.6.3 精密度、方法回收率和萃取回收率 配制rac-CIT、S-CIT和R-CIT高、中、低3个浓度质控样品,按1.4方法操作,分别在同一天内连续测定5次,连续测定3天,计算日内、日间精密度和方法回收率,均符合生物样品分析要求;取空白血浆配制高、中、低三种浓度的质控样品,按1.4方法操作,同时配制绝对进样量相当于各浓度质控样品100%含量的对照品工作液直接进样,以药物峰面积比计算药物的萃取回收率,符合生物样品分析要求。在经过预处理的空白血浆基质中加入rac-CIT、S-CIT和 R-CIT高、中、低3个浓度对照品溶液,记录进样得到的峰面积作为分子,以相应对照品溶液直接进样得到峰面积作为分母,二者相比计算得基质效应,结果符合生物样品分析要求。以上结果列于表1。
2.6.4 血浆样品稳定性 配制rac-CIT、S-CIT和 R-CIT高(浓度分别为40、20、20μg·L-1)、中(浓度分别为2.50、1.25、1.25μg·L-1)、低(浓度分别为0.312、0.156、0.156μg·L-1)的质控样品,分别于-30℃冰箱保存,考察样品长期稳定性、反复冻融、室温放置、重复进样及萃取物稳定性实验。实验结果表明,血浆样品4 h内重复进样、室温放置4 h、萃取物放置8 h、-30℃保存30天及反复冻融2次,与0时刻比较其分析物浓度无明显变化,结果列于表2。
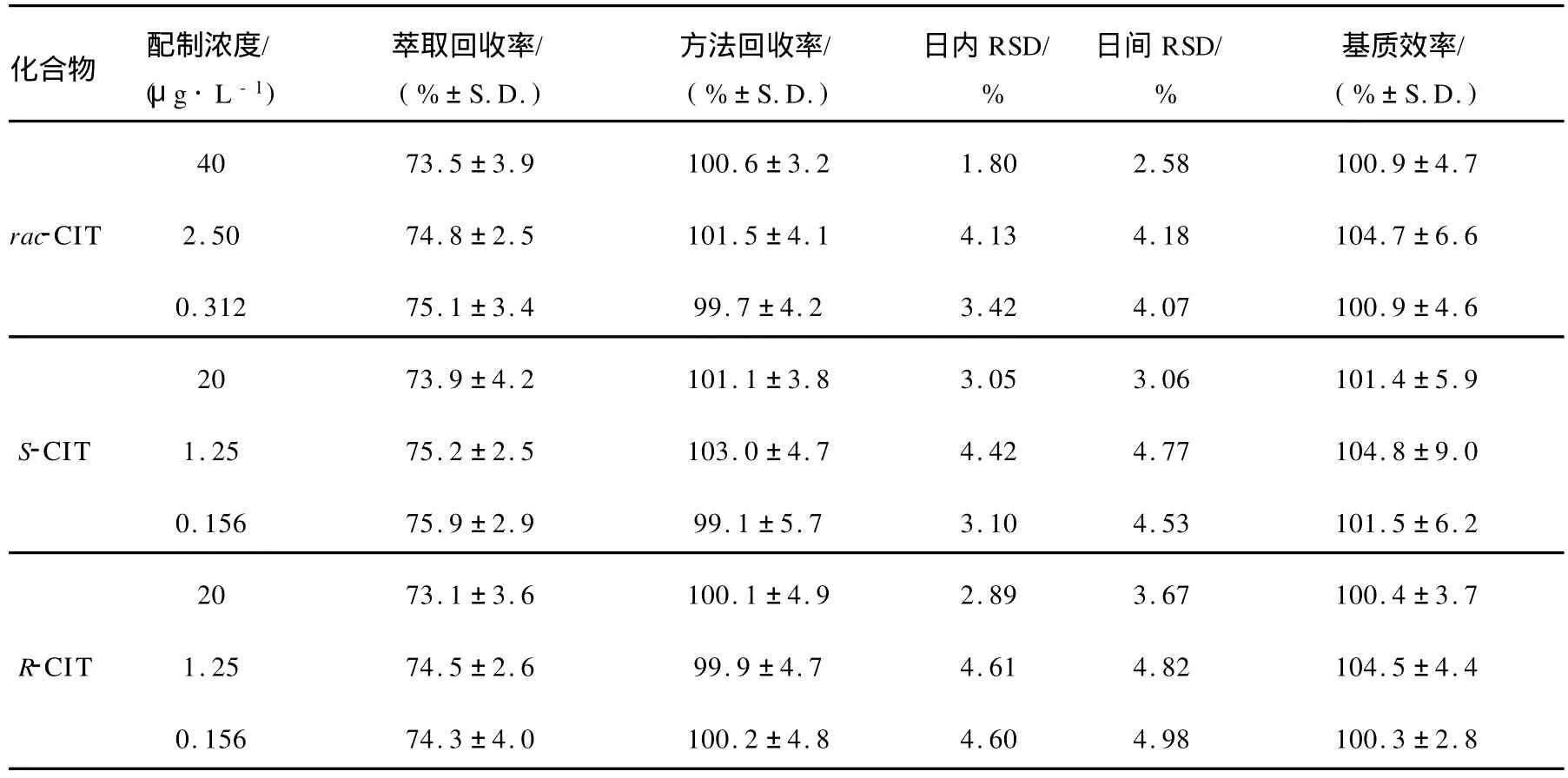
表1 西酞普兰对映异构体的精密度、方法回收率和萃取回收率实验结果Table 1 Results of precision,method recovery and extraction recovery of citalopram enantiomers
3 方法应用
10名男性健康受试者单次口服20 mg氢溴酸西酞普兰片后,用本法测定其体内西酞普兰对映体的浓度,血药浓度-时间曲线图示于图3。结果表明,该方法可用于西酞普兰对映异构体药代动力学、生物利用度及临床血药浓度的测定。

图3 血药浓度-时间曲线Fig.3 Mean concentration-time curve of citalopram enantiomers
[1]杜 瑜,李焕德.抗抑郁新药西酞普兰的药代动力学[J].中国临床药理学杂志,2005,21(4): 307-310.
[2]陈国珍,黄贤智,许金钧,等.荧光分析法[M].北京:科学出版社,1990:75-81.
[3]SONIA M Z,HIERRO I D,FAJARDO M,et al. Chiral separation of kgycidol enantiomers by normal-phase high-performance liquid chromatography coupled to atmospheric pressure chemical ionization mass spectrometry[J].Analytica Chimica Acta,2006,566:185-192.
[4]CYNTHIA M S,CARMEN F M.Determination of chiral sulfoxides in plasma by normal-phase liquid chromatography-atmospheric pressure chemical ionization mass spectrometry[J].Journal of Chromatography A,2002,964:161-168.
[5]LINDMARK B,AHNOFF M,PERSSON B A. Enantioselective determination of felodipine in human plasma by chiral normal-phase liquid chromatography and electrospray ionisation mass spectrometry[J].Journal of Pharmaceutical and Biomedical Analysis,2002,27:489-495.
[6]TOURNEL G,HOUDRET N,HEDOUIN V,et al. High-performance liquid chromatographic method to screen and quantitate seven selective serotonin reuptake inhibitors in human serum[J]. Journal of Chromatography B,2001,761(2): 147-158.
[7]OL E VO,KRISTIAN L.Studies on the stereoselective metabolism of citalopram by human liver microsomes and cDNA-expressed cytochrome P450 enzymes[J].Journal ofChromatography B, 1996,675:83-88.
Determination of Citalopram Enantiomers in Human Plasma with Normal Phase HPLC-MS/MS
XIANGJin,YU Qin,ZHANG Cheng,LIAN G Mao-zhi,NAN Feng,QIN Yong-ping
(Institute of Clinical Pharmacology,GCP center,West China Hospital of Sichuan University,Chengdu610041,China)
A normal phase high performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS)method for the determination of citalopram(CIT)enantiomers concentration in human plasma was established.CHIRALCEL OJ-H column(250 mm×4.6 mm×5μm)was used.The mobile phase consisted ofn-hexane,alcohol and diethylamine (V(n-hexane)∶V(alcohol)∶V(diethylamine)=70∶30∶0.1).The flow rate of mobile phase was 0.5 mL·min-1.The analytes were determined using atmospheric pressure chemical ionization source and multiple reaction monitoring(MRM)detection mode,which was adopted to detect the concentration of CIT in positive mode.Lidocaine was used as internal standard.CIT and the internal standard are monitored atm/z325.1→108.9 andm/z 235.4→86.1,respectively.Calibration curves are linear in range from 0.156 to 50μg·L-1forrac-CIT,from 0.078 to 25μg·L-1forS-CIT and both the coefficient correlation were more than 0.99.Forrac-CIT,S-CIT andR-CIT,the relative recoveries are 99.7%—101.5%,99.1%—103.3%,99.9%—100.2%;the extraction recoveries are 73.5%—75.1%,73.9%—76.0%,73.1%—74.3%,respectively.The inter-day and intra-day RSDs of the determinations of all species are less than 5.0%.
citalopram;enantiomer;plasma concentration;high performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS)
O 657.63
A
1004-2997(2010)04-0214-06
2009-08-27;
2010-03-06
向 瑾(1981~),女(汉族),四川人,助教,从事临床药代动力学研究。E-mail:xiangjintoday@163.com
余 勤(1969~),女(汉族),四川人,副教授,从事临床药代动力学研究。E-mail:sunny9996@tom.com
