盐酸多巴胺注射液细菌内毒素检查方法的研究
2010-08-29叶青王伟迪丽努尔沙比托夫新疆维吾尔自治区食品药品检验所乌鲁木齐市830004新疆医科大学第五附属医院乌鲁木齐市8300
叶青,王伟,迪丽努尔·沙比托夫(.新疆维吾尔自治区食品药品检验所,乌鲁木齐市830004;.新疆医科大学第五附属医院,乌鲁木齐市8300)
盐酸多巴胺注射液为肾上腺素受体及多巴胺受体激动药,临床上主要用于抗休克。《中国药典》2005年版二部中对盐酸多巴胺注射液无热原或细菌内毒素检查项目[1],但盐酸多巴胺注射液作为临床常用急救药物,是以静脉注射的方式进入人体,临床静脉用药中细菌内毒素污染可引起发热、寒战、昏迷甚至死亡等副反应,美、日、欧等药典中对静脉注射用注射液均规定有细菌内毒素或热原检查项目。为了有效控制药品中细菌内毒素的含量,确保临床用药的安全,笔者按照《中国药典》2005年版二部细菌内毒素检查法,对盐酸多巴胺注射液进行了细菌内毒素检查法的研究。
1 材料
电热恒温水浴箱(上海医疗器械七厂);微型旋涡混合器(上海精科实业有限公司);所使用容器和用具于250℃干烤1 h以上,备用。
细菌内毒素工作标准品(批号:2007-4,效价:每支150 EU)、细菌内毒素检查用水(BET水,批号:w2006-12,规格:每支10 mL)均来源于中国药品生物制品检定所;鲎试剂(TAL,湛江安度斯生物有限公司,批号:0612062;福州新北生化工业有限公司,批号:06012012,灵敏度均为0.25 EU·mL-1,规格均为0.1 mL);盐酸多巴胺注射液(上海禾丰制药有限公司,批号:6E11003、6E11043、6E11059;江苏亚邦强生药业有限公司,批号:060310、061024、060814,规格均为20 mg·2 mL-1)。
2 方法与结果
2.1 细菌内毒素限值(L)的确定[1]
根据公式:L=K/M,其中K为按规定的给药途径,人用每千克体质量每小时最大可接受的内毒素剂量,注射剂为5 EU·kg-1·h-1;M为人用每千克体质量每小时最大剂量。由于本品具有剂量依赖性,作用时间的长短与用量不相关,且休克患者个体差异较大,静滴速度和时间需根据血压、心率、尿量等情况而定,故剂量选为20 mg,稀释后静滴[2],中国人平均体质量按60 kg计,计算限值为L=15 EU·mg-1,与《美国药典》(USP32)中规定该药品的L为16.67 EU·mg-1没有明显差异,故最终确定限值为15 EU·mg-1。
2.2 鲎试剂灵敏度复核
根据鲎试剂标示灵敏度,用BET水将细菌内毒素工作标准品制备成2倍稀释浓度的一系列内毒素溶液:2λ、1λ、0.5λ、0.25λ。按照《中国药典》2005年版二部[1]规定,进行鲎试剂的灵敏度复核,结果2批鲎试剂经用细菌内毒素工作标准品检查,λc均在0.5λ~2λ范围内,均符合规定,可用于试验。
2.3 最大有效稀释倍数(MVD)的确定[1]
根据公式MVD=cL/λ,其中c为供试品溶液的浓度10 mg·mL-1,L为盐酸多巴胺注射液的内毒素限值15 EU·mg-1,λ为鲎试剂标示灵敏度,目前市售鲎试剂灵敏度λ通常在0.5~0.03 EU·mL-1之间,则对应的最大有效稀释倍数依次为300、600、1200、2500、5000倍。
2.4 干扰预试验[1,3]
为确定盐酸多巴胺注射液对该方法的影响,首先进行供试品干扰预试验。初步摸索可知盐酸多巴胺注射液对细菌内毒素检查有较强的抑制作用,由于盐酸多巴胺注射液的pH值为3.0~4.5,故将样品原液用无内毒素污染的1 mol·L-1的NaOH溶液调节pH至7.0左右(6.0~8.0范围内),用BET水分别稀释至300、600、1200、2500、5000倍,将此系列浓度溶液记为供试品阴性对照管(NPC)。同时制备含有2λ浓度细菌内毒素的上述浓度溶液,记此系列溶液为供试品阳性对照管(PPC)。取灵敏度为0.25 EU·mL-1的2个不同厂家的鲎试剂,分别与上述NPC和PPC进行反应,每一浓度平行做2管,并设阳性(PC)与阴性(NC)对照。结果见表1(“+”为阳性反应结果,“-”为阴性反应结果)。

表1 干扰预试验结果Tab 1Results of preliminary interference test
预试验结果表明,当盐酸多巴胺注射液稀释至600倍时,对2个鲎试剂厂家的试剂的反应均无干扰作用,故选择600倍作为正式干扰试验稀释倍数。
2.5 干扰试验
为了最终确认是否存在干扰因素的影响,进行以下干扰试验。取6批盐酸多巴胺注射液分别调节pH至7.0后,用BET水分别稀释至600倍,按《中国药典》2005年版二部附录中的“细菌内毒素检查供试品干扰试验”项进行试验[1],结果见表2。
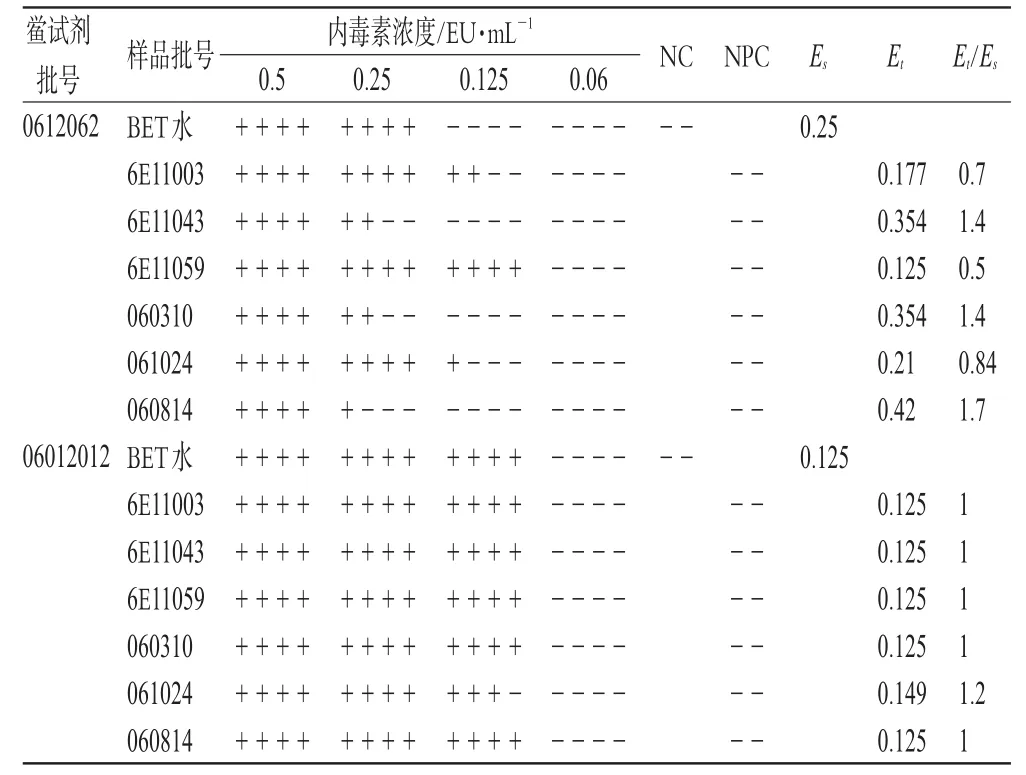
表2 干扰试验结果Tab 2Results of interference test
表2结果表明,细菌内毒素在2个系列中反应终点浓度的几何平均值(Es、Et)在0.5λ~2λ之间,且Et/Es均在0.5~2.0范围之内,确认供试品溶液在调节pH值后,稀释至600倍(浓度为0.0167 mg·mL-1)对鲎试剂与细菌内毒素的凝集反应没有干扰作用,可进行细菌内毒素检查。
2.6 样品细菌内毒素检查
按《中国药典》细菌内毒素检查法,使用2批灵敏度为0.25 EU·mL-1的不同厂家的鲎试剂,分别对6批供试品在pH值调至7.0、浓度稀释至0.0167 mg·mL-1后进行细菌内毒素检查,并同时设立样品的自身阳性对照管,细菌内毒素检查结果见表3。
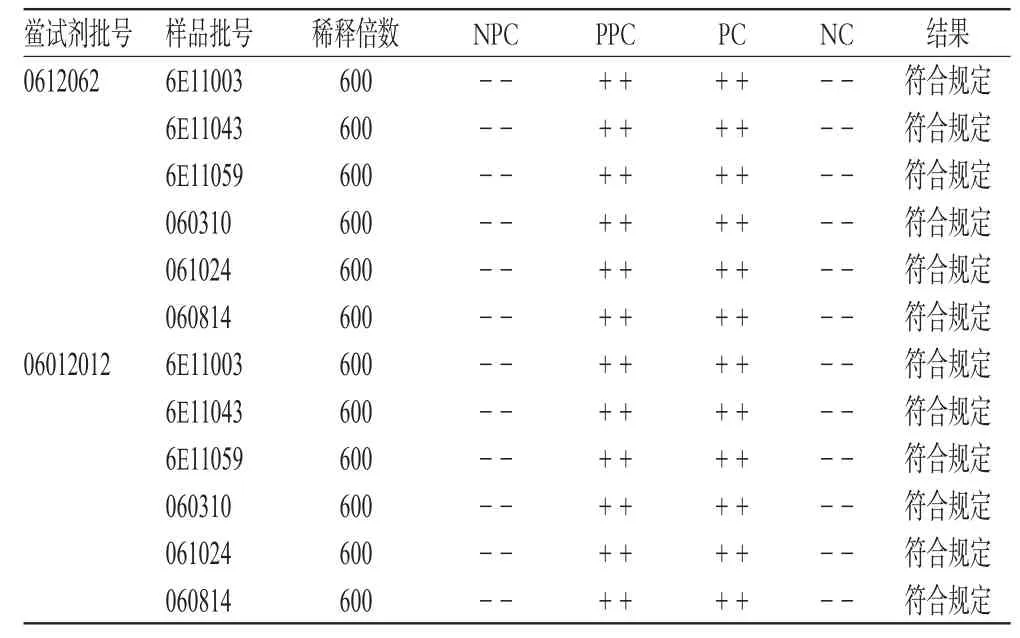
表3 6批样品中的细菌内毒素检查结果Tab 3Results of endotoxin detection of sample
表3结果表明,6批盐酸多巴胺注射液可使用灵敏度为0.25 EU·mL-1的鲎试剂进行检验,且内毒素含量小于15 EU·mg-1。
3 讨论
由于不同厂家生产的鲎试剂的抗干扰能力存在差别,为保证试验结果的可靠性,本试验选择2个厂家生产的鲎试剂对样品进行干扰试验。结果发现,样品对鲎试剂凝集反应的干扰性质为抑制作用,仅通过稀释的方法不能排除干扰;因盐酸多巴胺注射液的pH值范围在3.0~4.5之间,超出了鲎试剂本身具有的缓冲能力,按照《中国药典》2005年版[1]的规定,供试品溶液的pH值一般要求在6.0~8.0的范围内,故将样品pH值调至7.0左右,浓度稀释至0.0167 mg·mL-1后,再使用2个厂家的鲎试剂对2个企业生产的6批样品进行干扰试验,结果Et/Es均在0.5~2.0范围之内,确定样品在有效浓度范围内。样品对鲎试剂与细菌内毒素的凝集反应虽有抑制性干扰作用,但可以通过调节pH值和稀释的办法排除。结果表明,将限值定为15 EU·mg-1时,盐酸多巴胺注射液用细菌内毒素检查法控制产品质量是可行的。
[1]国家药典委员会编.中华人民共和国药典(二部)[S].2005年版.北京:化学工业出版社,2005:附录85~88.
[2]统一药品说明书及批准文号专项工作小组编.国家药品标准化学药说明书内容汇编[M].2002:5~101.
[3]刘春,赵毓梅.马来酸氯苯那敏注射液的细菌内毒素检查[J].中国药房,2009,20(25):1990.
