基因芯片检测输血传播病毒方法的实验研究
2010-08-21李志士刘铁梅
李志士,刘铁梅
(1.长春中医药大学附属医院,吉林长春 130021;2.吉林大学中日联谊医院输血科,吉林长春 130033)
基因芯片检测输血传播病毒方法的实验研究
李志士1,刘铁梅2
(1.长春中医药大学附属医院,吉林长春 130021;2.吉林大学中日联谊医院输血科,吉林长春 130033)
目的建立基因芯片快速检测经输血传播病毒核酸的方法,进而探讨该方法用于检测临床标本的可行性。方法通过PCR获得TTV病毒ORF1基因的DNA片段,克隆,从重组质粒扩增DNA片段,并点到玻璃载体上,制成芯片。与TTV病毒、甲型肝炎病毒、乙型肝炎病毒及戊型肝炎等病毒的PCR产物进行杂交,以检测探针的特异性。结果该基因芯片探针仅与TTV毒株的PCR产物杂交呈阳性,与对照病毒的PCR产物杂交呈阴性。敏感性试验显示,用该方法检测了27份疑似TTV临床病料,22份阳性;而用PCR法扩增TTV ORF1基因确诊为阳性的只有19份。结论利用基因芯片检测TTV的PCR产物,特异性和敏感性强,可作为TTV临床标本检测方法。
经输血传播病毒;基因芯片;检测
(Chin J Lab Diagn,2010,14:0887)
输血传播病毒(TTV)最早由Nishizawa等1997年从1例不明原因的输血后非甲-庚型肝炎患者血清中发现[1]。TTV是已知的环病毒科中唯一感染人类的病毒[1]。目前检测TTV感染所采用的方法是血清巢氏PCR法。本研究通过PCR法扩增TTV核酸最保守部分ORF1基因的DNA片段,克隆,从重组质粒扩增DNA片段,并点到玻璃载体上,制成芯片,检测TTV的PCR产物。对芯片探针的基因序列分析证明其核苷酸序列具有高度的保守性,理论上可用于TTV不同血清型的检测。
1 材料与方法
1.1 材料
肝组织与血清标本长春地区的TTV阳性患者。肝穿刺活检或手术切除的肝组织标本立即用10%中性福尔马林固定,常规石蜡包埋切片。采用经高压灭菌处理的一次性带盖试管,手术或肝穿刺前空腹抽取静脉血10 ml,离心分离血清,分装后-30℃保存备用。
1.2 仪器与试剂
MicroGrid TAS型芯片点样仪(BioRobotics公司)、384孔板、Personal 4100A型芯片扫描仪(GenePix公司)、Biofuge stratos台式高速离心机(Kendro公司)、GenePix4.1软件(GenePix公司)。主要试剂Taq DNA聚合酶购自上海生工;PCR产物纯化试剂盒购自v-gene生物科技有限公司;dNTP购自Promega公司;、pMD18-T Vector购自大连宝生物工程有限公司;鲑鱼精DNA购自Sigma公司,高纯度病毒核酸提取试剂盒(High Pure Viral Nucleic Acid Kit,Roche Molecular Biochemicals产品)。
1.3 引物设计 分析GenBank上登录TTV多个毒株ORF基因保守序列,寡核苷酸引物用Oligo,version 4.1设计,并在GenBank中分析序列的匹配情况。设计好的引物由宝生物技术有限公司(大连)合成, 其中1号序列1A引物5'端进行HEX修饰(表1)。
1.4 用于点样DNA片段的制备
DNA的抽提 采用高纯度病毒核酸提取试剂盒(High Pure Viral Nucleic Acid Kit,Roche Molecular Biochemicals产品),参照说明进行。分别使用 2、3、4、5号引物进行PCR扩增、电泳分析并回收DNA片段,分别进行pMD18-T Vector重组连接,将DNA片段的连接产物转入DH5α感受态细胞,在含有X2Gal、IPTG、Amp的L2琼脂平板培养基上挑选白色菌落进行筛选。参照碱裂解法抽提质粒DNA[4]。进行DNA片段序列测定分析,序列测定由宝生物工程(大连)有限公司完成。通过质粒PCR,无水乙醇沉淀,获得高浓度捕捉DNA。
1.5 制备芯片
分别提取上述4种DNA片段的重组质粒,用特异性引物2、3、4、5分别对这4种DNA片段的重组克隆质粒进行PCR扩增。为排除载体序列对体系的干扰,PCR产物需经切胶回收,纯化,然后将纯化产物定量,以100 ng/μ L的浓度按图1进行点样,其中芯片列阵中A号位点为阳性坐标探针,其序列为:5'-cy3-ggtcactcgttacgaacgc-3',5'端使用cy3进行荧光修饰,2/3/4/5为编号2、3、4、5引物相对应的PCR产物,0号为空白对照,芯片点样完毕,经80℃干烤2 h,完成基因芯片的制备。
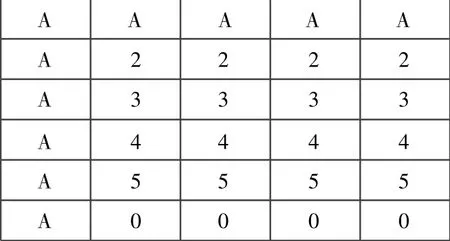
图1 探针在芯片上的点样位置
1.6 样品处理和杂交
采用高纯度病毒核酸提取试剂盒提取病毒基因组织DNA,参照说明进行。使用带有荧光标记的1号引物对基因组DNA进行PCR反应,制备探针,经纯化和浓度测定,-20℃避光保存。基因芯片经95℃变性,加入25 μ L预杂交液,44℃预杂交1 h。加入25μ L杂交液,杂交液含探针(终浓度为2 ng/μ L),42℃杂交8 h,芯片洗涤后以基因芯片扫描仪扫描分析,出现明显可见的杂交信号(斑点)判为阳性。
1.7 基因芯片的验证及临床样品的检测
依照上述样品处理和杂交方法,对TTV病毒、甲型肝炎病毒、乙型肝炎病毒及戊型肝炎等病毒阳性样品及27份疑似TTV临床病料进行PCR反应,产物检测标记探针同制备的芯片进行杂交分析。杂交程序以上述规范方法进行,扫描分析后以BMP格式图像判定检测结果。
2 结果
2.1 探针DNA片段的克隆及鉴定结果
根据实验设计,应用 PCR方法对TTV病毒ORF1基因片段进行扩增,获得了4个芯片点样用DNA片段及重组DNA片段质粒。PCR产物电泳(图2)鉴定可以看出,均得到了与目的片段相符的条带。基因片段大小在180-200 bp。
2.2 基因芯片的制备结果
用特异性引物2、3、4、5分别对这4种DNA片段的重组克隆质粒进行PCR扩增,PCR产物需经切胶回收,纯化,然后将纯化产物定量,以100 ng/μ L的浓度进行点样,芯片点样完毕后,编号,经80℃干烤2 h,完成基因芯片的制备。试验设计基因芯片为6×5阵列,其中阵列第一排与第一列为阳性坐标探针,第二、三、四、五排为TTV检测探针,第六排为阴性对照,图3为芯片点样后阳性坐标探针扫描结果。

图2 PCR检测结果
2.3 阳性样品处理和杂交
使用编号为1的引物对已知阳性TTV病毒进行PCR扩增,之后与芯片进行杂交,结果显示,实验所设计探针同已知阳性TTV病毒进行PCR产物可特异性杂交,制备的芯片可检测出TTV病毒ORF1基因片段。(见图4)

图3 基因芯片的制备结果

图4 阳性样品检测结果
2.4 基因芯片的验证及临床样品的检测
对TTV病毒、甲型肝炎病毒、乙型肝炎病毒及戊型肝炎等病毒阳性样品及27份疑似TTV临床病料进行PCR反应,产物检测标记探针同制备的芯片进行杂交分析。结果显示,芯片可以对TTV病毒进行特异性检测,针对甲型肝炎病毒、乙型肝炎病毒及戊型肝炎等病毒检测时没有出现假阳性结果。应用制备的芯片对长春地区27份疑似TTV临床病料进行检测,22份阳性;而用PCR法扩增TTV ORF1基因确诊为阳性的只有19份。表明此方法的敏感性高于普通PCR检测方法。
3 讨论
本研究进行了TTV核酸诊断基因芯片的制备及其检测技术的研究,克隆和鉴定了TTV ORF1基因DNA片段,成功制备了TTV核酸诊断基因芯片,并进行了制备基因芯片的检验研究;建立了基因芯片诊断TTV核酸的检测技术。该检测技术可以灵敏特异地对TTV病毒进行检测,具有检测灵敏性好、特异性高和芯片可重复检测的优点。
1997年日本学者Nishizawa首次报道分离出TTV,国内学者随后也相继报道了相关人群中TTV的感染情况。业已证实TTV是一种单链DNA病毒,基因全长约3.7 kb,有2个开放读码框架(ORF)。目前,临床上TTV诊断主要依据PCR方法,但其灵敏性还有一定的局限性。上世纪九十年代出现的DNA芯片技术则具备可以对成百上千、甚至上万个基因进行同时检测的优势,具有高通量和并行化特点[2,3]。目前该技术已经被广泛应用于基因表达、疾病诊断、基因多态性分析、发现新基因及药物筛选等研究领域,特别是在疾病诊断方面已获得许多成功[4-6]。应用基因芯片技术可以在基因水平同时确定多个病原遗传物质的存在,提供一种处理一次样品诊断鉴诊断的新方法,随着新技术方法的不断出现普及,基因芯片检测方法将会在临床检测中不断应用[7,8]。本研究,在基因芯片载体上检测TTV病毒ORF1 DNA片段,实验证明,这一思路是可行的,由于DNA芯片技术则具备可以对成百上千、甚至上万个基因进行同时检测的优势,在此基础之上可以在芯片平台上不断增加探针,进而可以将甲型肝炎病毒、乙型肝炎病毒及戊型肝炎等病毒的特异性探针集成在一张芯片上,建立高通量的肝炎病毒检测方法。使临床肝炎病毒的检测变得更加方便。
[1]Nishizawa T,Okamoto H,Konishi,et al.A novel DNA virus(TTV)asso-ciated with elevated transaminase levels in post transfusion hepatitis of unknown etiology[J].B iophys Rescommun,1997,241(1):922.
[2]Pease A C,Solas D,Sullivan E J,Cronin M T,Holmes C P,Fodor SP A.Light-generated oligonucleotide arrays for rapid DNA sequence analysis[J].Proceedings of the National Academy of Sciences USA,1994,91:5022.
[3]Schena M,Shalon D,Davis R W,Brown P O.Quantitativemonitoring of gene expression patterns with a complementary DNA microarray[J].Science,1995,270:467.
[4]Bowtell D D L.Options available-from start to finish-for obtaining expression data by microarray[J].Nature Genetics,1999,21:25.
[5]Duggan,D J,BittnerM,Chen Y D,Meltzer P,Trent J M.Expression profiling using cDNA microarrays[J].Nature Genetics,1999,21:10.
[6]Debouck C,Goodfellow P N.DNA microarrays in drug discovery and development[J].Nature Genetics,1999,21:48.
[7]Favis R,Day J P,Gerry N P,PhelanC,Narod S,Barany F.Universal DNA array detection of small insertions and deletions in BRCA1 and BRCA2[J].Nature Biotechnology,2000,18:561.
[8]Shalon D,Smith S J,Brown P O.A DNA microarray system for analyzing complex DNA samples using two-color fluorescent probe hybridization[J].Genome Research,1996,6(7):639.
Detection of transfusion transmitted virusgene chip method of experimental study
LI Zhi-shi1,LIUTie-mei2.(1.The Affiliated Hospital of Changchun University of Traditional Chinese Medicine,Changchun130021,China;2.China-Japan Union Hospital,Jilin University,Changchun130033,China)
ObjectiveTo establish the gene chipmethod of rapid detection of TTV DNA,and then explore the method used to detect the feasibility of clinical samples.MethodsTTV virus OR F1 gene PCR to obtain the DNA fragments,cloning,DNA fragments amplified from the recombinant plasmid,and point to the glass carrier,made of silicon.And TTV virus,hepatitis A virus,hepatitis B virus and hepatitis E virus like PCR products were hybridized to detect the probe specificity.ResultsThe results of the gene-chip probe only with TTV strains positive for PCR product of hybridization with the control virus and organizations PCR product of hybridization were negative.Sensitivity tests showed thatUsing thismethod to detect clinical disease,27were suspected of TTV material,22 were positive;but with the TTV ORF1 gene was amplified by PCR confirmed positive,only 19 copies.ConclusionThe detection of TTV DNA microarray of the PCR product specificity and sensitivity of strong,repeatable,can be used as clinical samplesTTV detection methods.
transfusion transmitted virus;gene chip;Detection
Q78
A
1007-4287(2010)06-0887-04
2009-05-19)
