甲基化特异性PCR检测PRAME基因启动子低甲基化30例及其临床应用*
2010-08-14朱照辉姚冬明王雅丽肖高飞
朱照辉,林 江,钱 军△ ,姚冬明,钱 震,王雅丽,肖高飞
(江苏大学附属人民医院:1.血液科;2.中心实验室;3.检验科,江苏 212002)
黑色素瘤优先表达抗原(preferentially expressed antigen of melanoma,PRAM E)是肿瘤相关抗原,在多种肿瘤细胞中高度表达,可作为一种肿瘤分子标志物用于微小残留病(minimal residual disease,MRD)监测[1-2]。Christina等[3]研究发现,PRAME基因启动子区低甲基化可能是其表达调控机制之一。本实验室建立了一种检测PRAM E基因低甲基化的EvaGreen荧光染料实时定量甲基化特异性PCR(RQ-MSP)法,并对急性髓系白血病(AML)患者进行了检测,证实该方法可用于AML患者初诊标本检测,并可用于随访标本MRD的监测。
1 资料与方法
1.1 一般资料 选择18例(对照组)骨髓标本,其中11例取自正常捐献者,7例取自缺铁性贫血(IDA)患者。30例(AML组)患者骨髓标本来自本院血液科住院患者,诊断按FAB标准分类。未甲基化阳性对照为重亚硫酸氢盐修饰的AML患者的骨髓DNA,用去离子水作为阴性对照,甲基化阳性对照为经甲基转移酶(M.SssI)处理后再行重亚硫酸氢盐修饰的正常人骨髓DNA。
1.2 单个核细胞分离和基因组DNA制备 按本实验室常规方法提取骨髓单个核细胞;依据基因组 DNA提取试剂盒(Gentra)和DNA修饰试剂盒(Chemicon公司)操作指南提取基因组 DNA,进行DNA重亚硫酸氢盐修饰,-80℃保存备用。
1.3 方法
1.3.1 定性MSP 按参照文献[4]合成引物,PRAME基因未甲基化(U)MSP上游引物序列 5′-GTT GTA AGG ATG TTT TGA ATT GA-3′,下游引物 序列 5′-CCT ACA CCA CTA CCT AAA CCA TC-3′,扩增片段169 bp。参照基因 ALU 的上游引物序列 5′-TTA GGT ATA GTG GTT TAT ATT TGT AAT TTT AGT A-3′,下游引物序列5′-ATT AAC TAA ACT AAT CTT AAA CTC CTA ACC TCA-3′,扩增片段 110 bp。MSP反应在Icycler梯度仪(伯乐公司)进行,25μL反应体系包括10×PCR缓冲液2.5μL、2.5 mmol/L三磷酸脱氧核苷酸(d NTP)2.0μL、10 pmol/μL 引物 0.5μL、1 u热启动 Taq DNA酶(Takara公司,日本)、重亚硫酸氢盐修饰后的基因组DNA 80 ng。反应条件为95℃预变性5 min,94℃30 s、60℃30 s、72℃30 s共 40个循环,72℃延伸 7 min。扩增产物经2%琼脂糖凝胶电泳成像分析(Gene Genius凝胶成像仪,Syngene公司,英国)。

表1 RQ-MSP检测不同浓度PRAME基因与ALU基因质粒结果
1.3.2 阳性模板制备 将1例AML患者的MSP扩增产物经T 4DNA连接酶(Promega公司)克隆入 PGEM-T载体,扩增纯化重组载体、测序鉴定(上海基康),并将其定量,最后从5×107copy/μL开始进行10倍稀释,建立阳性模板梯度,4℃储存备用。
1.3.3 RQ-MSP PRAM E基因与ALU基因反应程序和反应条件相同。25μL反应体系包含DNA80 ng、10×缓冲液2.5 μL、dNTP(10 mmol/L)0.5 μL 、Mg Cl2(25 mmol/L)2.0 μL、10 pmol/μL引物 2.0μL(ALU 引物为 1.0μL)、20×EvaGreen(BIOTIUM 公司)1.2μL、50×ROX0.5μL、Taq酶1.0 u(MBI公司)。PC R反应在 PE7300(美国ABI公司)扩增仪上进行。反应条件为预变性95℃5 min,95℃ 30 s、62℃30 s、72℃30 s扩增40循环;扩增产物熔解曲线分析程序为 95℃15 s、40℃60 s、90℃ 15 s、60℃15 s。应用参照基因 ALU计算PRAME基因启动子未甲基化水平的相对量,计算公式如下:NP RAME=(EPRAME)△C TP RAME(对照标本)/(EALU)△C TALU(对照标本),其中E为PCR扩增效率(E=10-1/slope),△CT为对照样本与待测标本中PRAM E或 ALU基因扩增的循环阈值(CT值)的差异;对照选自PRAME与ALU基因的CT值差异最小的1例正常献髓者。
1.4 统计学处理 应用SPSS13.0软件进行统计学数据分析,组间比较应用Mann-Whitney U检验,以 P<0.05为差异有统计学意义。
2 结 果
2.1 RQ-MSP特异性 RQ-MSP扩增产物的熔解曲线分析揭示不同浓度的PRAME未甲基化阳性模板扩增产物均为单一峰,其Tm值为82.6℃,而PRAM E基因甲基化阳性模板、未经重亚硫酸氢盐修饰的正常基因组DNA和去离子水则未显示峰;并且凝胶电泳结果显示未甲基化阳性模板扩增产物可见一约170 bp左右条带,而甲基化阳性模板和去离子水扩增结果为阴性(图1)。
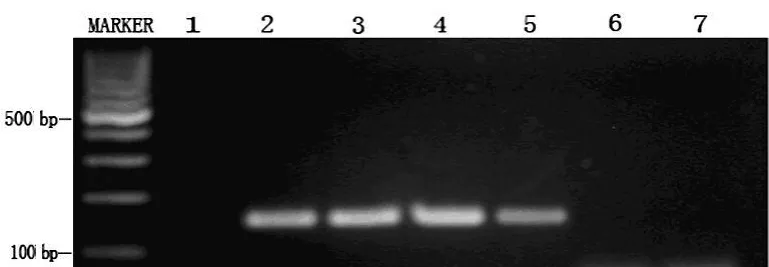
图1 PRAME基因RQ-MSP扩增产物凝胶电泳
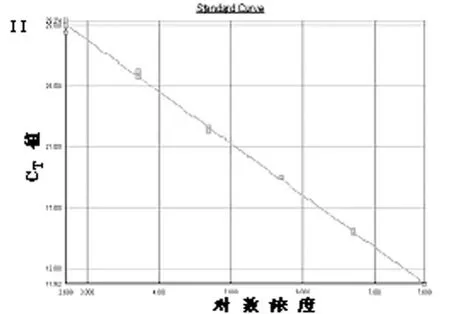
图2 PRAME质粒RQ-MSP标准曲线
2.2 RQ-MSP灵敏度、重复性和扩增效率 对不同浓度PRAM E未甲基化 DNA质粒和ALU质粒分别扩增8次,PRAM E质粒最大灵敏度达 50 copy/μL,重复性不好,5×107~5×102copy/μL重复性良好,见表1。变异系数(CV)为0.59%~1.53%。分别于第1、2、3周扩增PRAME质粒评价其不同时间的重复性,CV值为0.66%~3.35%,见表2。5×107~5×102copy/μL的 PRAM E质粒荧光扩增曲线,其标准曲线的斜率为-3.39,相关系数为0.998,PCR扩增效率(E)为1.97。
2.3 RQ-MSP检测AML组PRAM E基因未甲基化水平 对照组检测发现PRAME基因启动子未甲基化水平较低,见表3。而AM L组中,PRAME基因启动子未甲基化含量则明显增高,两组间PRAME基因启动子未甲基化含量差异有统计学意义(P=0.002)。

表2 不同时间RQ-MSP检测PRAM E质粒的结果
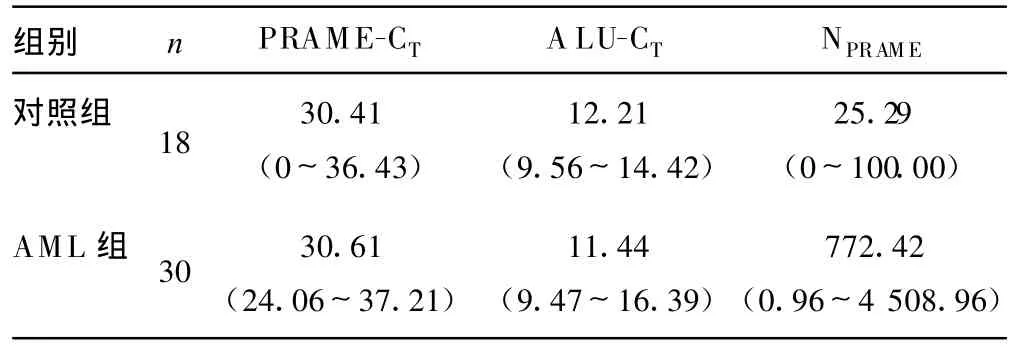
表3 标本中PRAME基因RQ-MSP检测结果[中位(范围)]
3 讨 论
PRAME基因在AM L患者中呈高水平表达,可能通过维甲酸信号通路参与调节细胞增殖[5]、分化和凋亡,其表达量与DNA甲基化程度之间存在可逆关系,提示DNA低甲基化在PRAME基因表达中起着重要的调控作用[6],检测PRAM E基因低甲基化有助于疾病早期诊断,并为化疗提供预测指标。
基因组DNA甲基化包括高甲基化和低甲基化,目前标准MSP法广泛应用于检测基因组DNA甲基化,它避免了限制性核酸内切酶酶切技术操作复杂、技术难度大、酶切不彻底、不能反映整个CpG岛的甲基化状态等缺点,但是只能定性检测有无甲基化的存在,无法进行定量分析。实时荧光定量PCR建立与目的片段一样的标准品,保证目的片段与标准品的扩增效率一致,减小实验误差[7],具有快速准确、敏感度高、重复性好和无需PCR后处理等优点,已被广泛应用于核酸定量研究。Toyooka等[8]建立的RQ-MSP法克服了 MSP的缺点,能定量检测目的基因甲基化量,在此基础上,本研究建立了以EvaGreen为荧光染料的RQ-MSP检测PRAME基因未甲基化技术,结果显示 RQ-MS P具有良好的重复性、特异性和灵敏性。
本研究初步检测两组PRAM E基因启动子低甲基化含量,结果表明两者差异有统计学意义,AM L组PRAM E基因启动子区低甲基化水平明显高于对照组,文献报道[9-11],30%~64%AML患者存在PRAME基因高水平表达,提示AML患者PRAM E基因低甲基化改变可能与其发病相关。
本研究揭示RQ-MSP能够准确检测PRAME基因启动子区的低甲基化水平,并且可用于肿瘤患者初诊标本和化疗后随访标本的M RD检测。
[1]Steinbach D,Hermann J,Viehmann S,etal.Clinicalimplication of PRAM E gene expression in childhood acute myeloid leukemia[J].Cancer Genet Cytogenet,2002,133(1):118.
[2]Spanakia A ,Perdikogianni C ,Linardakis E ,et al.Quantitative assessment of PRAME expression in diagnosis of childhood acute leukemia[J].Leuk Res,2007,31(5):639.
[3]Christina A ,Ortmann,Eisele L,et al.Aberranthypomethylation of the cancer-testis antigen PRAM E correlates with PRAME expression in acute myeloid leukemia[J].Ann Hematol,2008 ,87(10):809.
[4]Roman-Gomez J,Jimenez-Velasco A ,Agirre X,et al.Epigenetic regulation of PRAM E gene in chronic myeloid leukemia[J].Leuk Res,2007,31(11):1521.
[5]Epping M T,Wang L,Edel MJ,et al.The human tumor antigen PRAME is a dominant repressor of retinoic acid receptor signaling[J].Cell,2005 ,122(6):835.
[6]Schenk T ,S tengel S ,Goellner S ,et al.Hypomethylation of PRAME is responsible for its aberrant overexpression in human malignancies[J].Genes Chromosomes Cancer,2007,46(9):796.
[7]罗勇军,刘昕.实时荧光定量PCR标准品的制备及应用[J].重庆医学 ,2005 ,34(3):414.
[8]Toyooka KO ,Toyooka S,Maitra A ,et al.Establishment and validation of real time polymerase chain reaction method for CDH1 promoter methylation[J].Am J Pathol,2002 ,161(2):629.
[9]Goellner S ,S teinbach D,Schenk T ,et al.Childhood acute myelogenous leukaemia:Association between PRAM E,apoptosis-and MDR-related gene expression[J].Eur J Cancer,2006,42(16):2807.
[10]Tajeddine N,Millard I,Gailly P,et al.Real-time RT-PCR quantification of PRA-M E gene expression for monitoring minimal residual disease in acute myeloblastic leukaemia[J].Clin Chem Lab Med ,2006 ,44(5):548.
[11]Paydas S,Tanriverdi K ,Yavuz S,et al.PRAM E m RNA levels in cases with acute leukemia:clinical importance and future prospects[J].Am J Hematol,2005,79(4):257.
